БІОХІМІЯ - Підручник - Остапченко Л. І. - 2012
Розділ 1. БУДОВА Й РЕАКЦІЙНА ЗДАТНІСТЬ БІООРГАНІЧНИХ СПОЛУК
1.3. Окремі класи біоорганічних сполук та їхнє біологічне значення
1.3.4. Біоорганічні сполуки азоту
До азотовмісних похідних вуглеводнів належать нітросполуки й аміни, в яких атоми водню заміщені на NO2- і NH2-групи відповідно, та аміди - продукти заміщення ОН-групи в карбоксилі карбонових кислот на NH2. Нітросполуки (R-NO2) поділяються на аліфатичні (насичені - нітроалкани, ненасичені - нітроалкени) та ароматичні (нітроарени). У нітросполук атом азоту й обидва атоми кисню перебувають у стані sр2-гібридизації та електронна будова нітрогрупи є резонансною структурою з граничними формами:
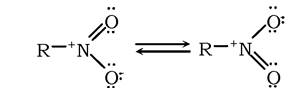
У результаті відновлення нітросполук утворюються первинні аміни:![]() . Продуктами відновлення нітроалканів є алканаміни:
. Продуктами відновлення нітроалканів є алканаміни:![]() У результаті відновлення ароматичних сполук (реакція Зініна) утворюється анілін і його похідні. Проміжними продуктами реакції є нітрозо-сполуки (містять нітрозогрупу N=О) і гідроксиламін:
У результаті відновлення ароматичних сполук (реакція Зініна) утворюється анілін і його похідні. Проміжними продуктами реакції є нітрозо-сполуки (містять нітрозогрупу N=О) і гідроксиламін:
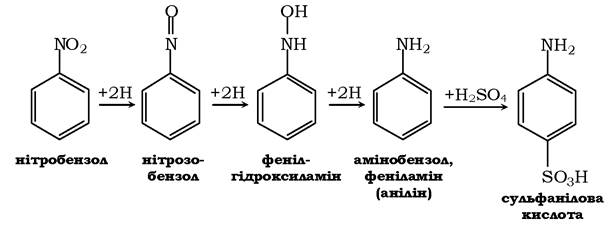
Аміни поділяються на первинні (RNH2), вторинні (R2NH) і третинні (R3N). За хімічною природою радикалів (R) аміни поділяються на аліфатичні (R - нециклічний), ароматичні (R - похідне бензолу) та аліфатично-ароматичні. В окрему групу виділено діаміни - сполуки з двома аміногрупами. У свою чергу, аліфатичні, ароматичні, аліфатично-ароматичні і діаміни можуть бути і первинними, і вторинними, і третинними. Діаміни широко розповсюджені в організмах, наприклад, путресцин (бутандіамін-1.4) - Н2-(СН2)4-KН2 і кадаверин (cadaver - труп; пентандіамін- 1.5) - Н2-(СН2)5-KН2, що накопичуються при гнитті тканин, а також спермін - Н2-(СН2)3-Н-(СН2)4-Н-(СН2)3-Н2, який бере участь у регуляції реплікації ДНК. Основними властивостями амінів є їхня взаємодія з кислотами з утворенням амонієвих солей, реакції алкілування та ацилювання, продуктами яких є заміщені аміди карбонових кислот, реакції заміщення в ароматичному кільці амінів, зокрема синтез сульфанілової кислоти з аніліну. Ця кислота є структурним компонентом сульфаніламідів - антимікробних засобів, до яких належить широко відомий стрептоцид - амід сульфанілової кислоти. Механізм бактеріостатичних ефектів сульфаніламідних препаратів полягає в конкурентному гальмуванні бактеріальних ферментів, субстратом яких є параамінобензойна кислота, а продуктом - фолієва кислота (вітамін Вс), необхідна для росту бактерій. Параамінобензойна кислота є вихідною речовиною і для синтезу анестетиків - анестезину, новокаїну, лідокаїну тощо.
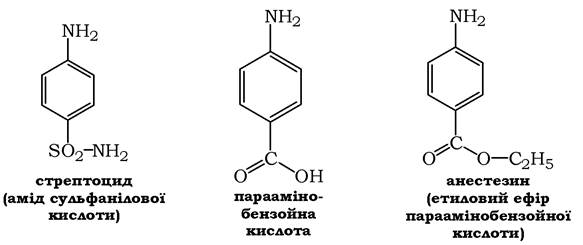
Анестезуюча дія цих речовин зумовлена блокуванням натрієвих каналів постсинаптичної мембрани, що припиняє проведення збудження.
Аміди кислот (R-CO-NH2) можна розглядати як продукти заміщення ОН-групи в карбоксилі карбонових кислот на NН2-групу або як результат заміщення атому водню в молекулі аміаку на ацильну групу. Реакції амідування є вельми важливими в біохімічних процесах, прикладом чого є утворення амінокислоти глутаміну з глутамінової кислоти:

Амінокислоти ковалентно зв'язуються за допомогою заміщеного амідного зв'язку (див. табл. 1.1). Утворення пептидного зв'язку в результаті реакції нуклеофільного заміщення аміногрупою гідроксильних груп у молекулах природних амінокислот розглядається в розд. 5.