БІОХІМІЯ - Підручник - Остапченко Л. І. - 2012
Розділ 12. МЕТАБОЛІЗМ ВУГЛЕВОДІВ
12.2.Глюконеогенез
Процес біосинтезу D-глюкози з невуглеводних попередників називається глюконеогенезом. Субстратами глюконеогенезу є лактат, піруват, гліцерол, глюкогенні амінокислоти, проміжні метаболіти циклу Кребса. Включення цих субстратів у метаболічний шлях глюконеогенеза здійснюється через піруват, а також оксалоацетат і дигідроксіацетонфосфат. Глюконеогенез відбувається головним чином у печінці, а також незначною мірою в нирках, мозку, скелетних м'язах, міокарді та слизовій оболонці кишечнику.
Головною метою глюконеогенезу є забезпечення нормального рівня глюкози в крові під час тривалого голодування та інтенсивного фізичного навантаження.
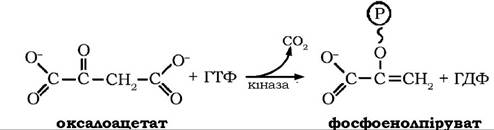
У реакціях цього метаболічного шляху піруват перетворюється у глюкозу, і хоча глюкогенез включає сім оборотних реакцій гліколізу, він не є поверненням гліколізу. У гліколітичному розщепленні глюкози є три етапи, на яких відбувається значне зниження вільної енергії субстрату. Тому ці реакції, що каталізуються гексокіназою, фосфофруктокіназою і піруваткіназою, є практично необоротними. У глюконеогенезі замість цих необоротних етапів гліколізу проходять також фактично необоротні реакції з іншою стехіометрією і напрямком, і каталізуються вони іншими ферментами (рис. 12.11).
Перший із цих етапів - перетворення пірувату у фосфоенолпіруват - відбувається в мітохондріях, де за дії піруваткарбокси- лази піруват карбоксилюється з утворенням оксалоацетату.
У карбоксилюванні пірувату простетична група ферменту - біотин - функціонує як переносник карбоксильної групи:
![]()
Реакція проходить у дві стадії. Карбоксильна група спочатку активується за рахунок гідролізу молекули АТФ, а потім переноситься на піруват. Піруваткарбоксилаза є регуляторним ферментом, активність якого контролюється її алостеричним модулятором - ацетил-KoA. Оскільки зв'язування біотину з СО2 можливо тільки у присутності ацетил-KoA, у разі відсутності останнього фермент практично неактивний. Продукт реакції оксалоацетат є також і проміжним метаболітом циклу Кребса, тому піруваткарбоксилазна реакція є по суті анаплеротичною, тобто компенсуючою в разі потреби нестачу субстратів для інших реакцій, наприклад циклу трикарбо- нових кислот, або біосинтезу амінокислот.
Таким чином, у разі високого співвідношення АТФ/АДФ у мітохондріях оксалоацетат бере участь у реакціях синтезу глюкози. Якщо співвідношення АТФ/АДФ стає низьким, оксалоацетат включається в цикл Кребса.
У процесі глюконеогенеза оксалоацетат оборотно перетворюється в малат: спочатку відновлюється за участю НАД-залежної мітохондріальної малатдегідрогенази, далі транслокується із мітохондрії в цитоплазму за допомогою дикарбоксилатної транспортної системи, де реокиснюється цитоплазматичною формою малатдегідрогенази:
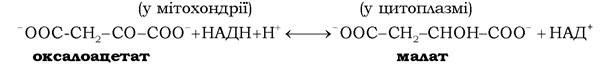
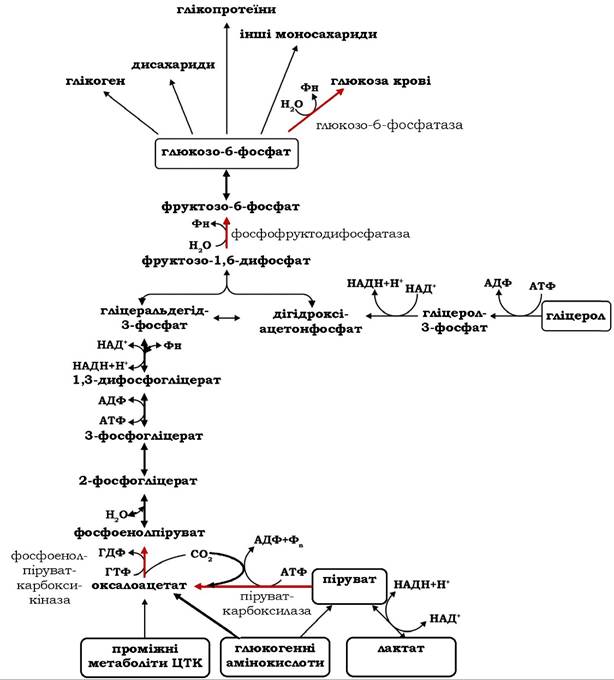
Рис. 12.11. Шлях глюконеогенезу
Наступні реакції біосинтезу глюкози відбуваються в цитоплазмі. Оксалоацетат за дії фосфоенолпіруваткарбоксикінази декарбоксилюється й одночасно фосфорилюється за рахунок ГТФ з утворенням фосфоенолпірувату:
Мg2+-залежна фруктозодифосфатаза є регуляторним ферментом глюконеогенезу, алостеричними модуляторами її активності є АТФ, цитрат (активатор) і АДФ, АМФ (інгібітор).
Після ізомеризації фруктозо-6-фосфату за дії фосфоглюкоізомерази на глюкозо-6-фосфат, останній в обхідній реакції глюконеогенезу гідролізується глюкозо-6-фосфатазою до D-глюкози:
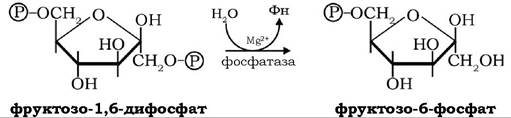
Сумарне рівняння цього обхідного етану глюконеогенезу:
![]()
Далі високоенергетична сполука фосфоенолпіруват у реакціях глюконеогенезу, які є оборотними відповідним реакціям гліколізу, перетворюється у фруктозо-6-фосфат. Причому в реакції перетворення 3-фосфогліцерату в 1,3-дифосфогліцерат витрачається одна молекула АТФ (рис. 12.11).
На наступному необоротному етапі гліколізу замість фосфофруктокіназної реакції в глюконеогенезі йде реакція, яка каталізується фруктозодифосфатазою:
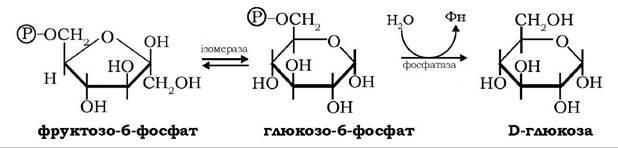
Остання фосфатазна реакція досить інтенсивно проходить у печінці, звідки глюкоза може вивільнятися в кров і надходити в інші тканини, де вона фосфорилюється й використовується або в гліколітичному розщепленні (мозок, м'язи), або в синтезах глікогену, глікопротеїнів, дисахаридів, інших моносахаридів (нирки, молочні залози, кишечник та ін.).
Таким чином, сумарне рівняння процесу глюконеогенезу, враховуючи необхідність двох молекул пірувату для синтезу однієї молекули глюкози, має такий вигляд:
![]()
Отже, на синтез глюкози з пірувату і на забезпечення необоротності процесу витрачається енергія шести високоенергетичних фосфатних зв'язків від чотирьох молекул АТФ і двох молекул ГТФ. Крім того, у відновних реакціях витрачається ще дві молекули НАДН, тобто за енергетичними затратами глюконеогенез значно випереджає гліколіз (дві молекули АТФ).
Основним субстратом для глюконеогенеза є лактат. У процесі інтенсивного м'язового скорочення (спринтерский біг, плавання, боротьба тощо) в умовах гіпоксії швидкість утворення пірувату і НАДН у ході глікогенолізу переважає їхнє окиснення в циклі трикарбонових кислот і дихальному ланцюгу. Продовження гліколізу в активних м'язах залежить від швидкості реокиснення НАДН у реакції відновлення пірувату, який каталізується лактатдегідрогеназою:
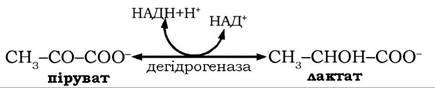
Обидві сполуки легко надходять із м'язів, що скорочуються, у кров і переносяться в печінку, де в умовах низького співвідношення НАДН/НАД+ лактат реокиснюється лактатдегідрогеназою печінки на піруват. Останній шляхом глюконеогенезу перетворюється на глюкозу, яка дифундує з печінки у кров і поглинається м'язами, які активно скорочуються. Таким чином, здійснюється цикл перетворень: глюкоза → піруват → лактат → піруват → глюкоза в м'язах і печінці, який називається циклом Корі (рис. 12.12).
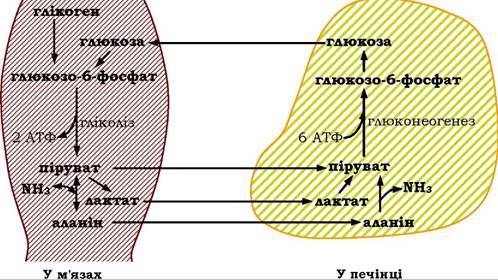
Рис. 12.12. Обмін метаболітами між скелетними м'язами і печінкою (цикл Корі)
Субстратами глюконеогенезу є також більшість глюкогенних амінокислот, які вивільняються в процесі розпаду м'язових та інших білків, наприклад аланін, глутамат, аспартат, що дезамінуються з утворенням відповідних кетокислот: пірувату, α-кетоглутарату та оксалоацетату. Фактичними субстратами глюконеогенезу є й інші проміжні метаболіти циклу трикарбонових кислот, що перетворюються в циклі в оксалоацетат, а також гліцерол, який залучається на шлях синтезу глюкози через дегідроксіацетонфосфат за допомогою гліцеролкінази та гліцеролфосфатдегідрогенази:
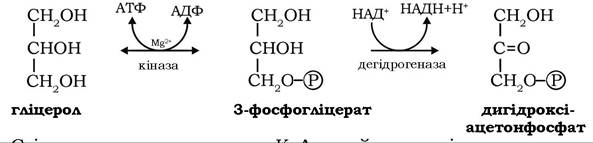
Слід зауважити, що ацетил-КоА, який в організмах тварин не може бути субстратом для синтезу глюкози через відсутність шляху зворотного перетворення в піруват, у клітинах рослин і багатьох мікроорганізмів набуває такої здатності завдяки перетворенням його в реакціях гліоксилатного циклу (рис. 12.13).
Особливо важливе значення глюконеогенез має в організмі жуйних тварин, у рубці яких головний компонент рослинної їжі целюлоза розщеплюється до глюкози, яка майже повністю зброджується бактеріальними ензимами до органічних кислот, головним чином лактату, а також ацетату, пропіонату, бутирату та ін.
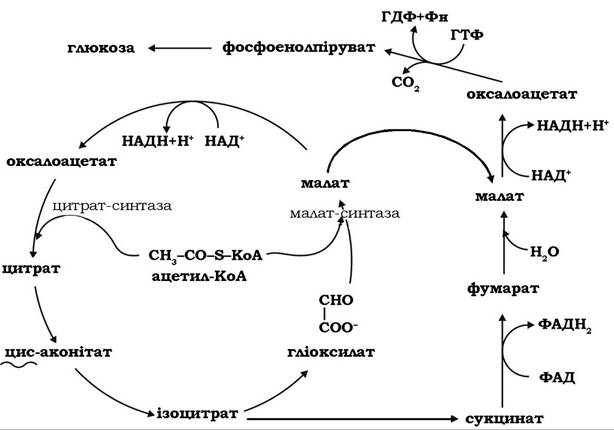
Рис. 12.13. Гліоксилатний цикл
Лактат усмоктується епітеліальними клітинами рубця і переноситься з кров'ю до печінки, де в реакціях глюконеогенезу перетворюється у глюкозу. Таким чином, організми жуйних тварин (корови, наприклад) практично повністю є залежними від глюконеогенезу, який постачає енергетичний субстрат у вигляді глюкози. Пропіонат та інші органічні кислоти також можуть включатися в глюконеогенез різними метаболічними шляхами через проміжні метаболіти циклу Кребса.
Синтез лактози - найважливішого для ссавців дисахариду - відбувається в секреторних клітинах молочних залоз за такою схемою:
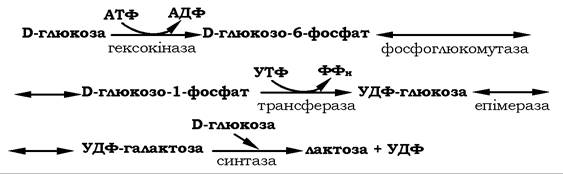
Завершальна стадія цього процесу здійснюється за участю двох білків, які складають лактозосинтазну систему. Один із цих білків - білок А - є ферментом, що каталізує перенесення галактозильного залишку від УДФГал на N-ацетилглюкозамін:
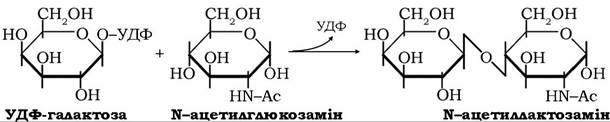
Другий білок лактозосинтазної системи - білок В, відомий як α-лактальбумін молока, котрий синтезується в молочних залозах під впливом гормонів лактації, модулює специфічність білка А таким чином, що акцептором галактозильних залишків стає не N-ацетилглюкозамін, а D-глюкоза. Отже, продуктом сумісної дії білків лактосинтетазної системи є вільна лактоза: