СОВРЕМЕННАЯ БОТАНИКА - П. РЕЙВН - 1990
РАЗДЕЛ II. ЭНЕРГИЯ И ЖИВЫЕ КЛЕТКИ
ГЛАВА 7. ФОТОСИНТЕЗ
Световые реакции
Роль пигментов
Первый этап преобразования световой энергии в химическую — это поглощение света. Пигмент представляет собой соединение, которое поглощает видимый свет. Некоторые пигменты поглощают свет любой длины волны и поэтому кажутся черными. Другие — свет только определенной длины волны, а остальной пропускают или отражают. Хлорофилл — это пигмент, который обусловливает зеленый цвет листьев; он поглощает в основном фиолетовые и синие лучи, а также красный свет, при этом отражая зеленый (поэтому он и кажется зеленым).
Спектр поглощения хлорофилла представлен на рис. 7-5 (спектр поглощения характеризует долю энергии поглощенного света в зависимости от длины волны).
Доказательство того, что хлорофилл — это основной пигмент, участвующий в фотосинтезе, заключается в сходстве его спектра поглощения со спектром действия фотосинтеза (рис. 7-6). Спектр действия определяет относительную эффективность различных длин волн света для таких светозависимых процессов, как фотосинтез, цветение, фототропизм (изгибание растения по направлению к свету). Сходство спектра поглощения пигмента и спектра действия процесса считается доказательством того, что именно данный пигмент обеспечивает осуществление этого процесса (рис. 7-7).
Рис. 7-5. Спектр поглощения хлорофилла а, измеренный на спектрофотометре. Лун света определенной длины волны направляется на исследуемый объект, и регистрируется процент света, поглощенного пигментом в опытном образце по сравнению с исходным, контрольным. При этом с помощью специального зеркала половина света отражается, а другая — пропускается. Фотоэлектрическая ячейка, соединенная с электронным устройством, регистрирует процент поглощения света любой длины волны
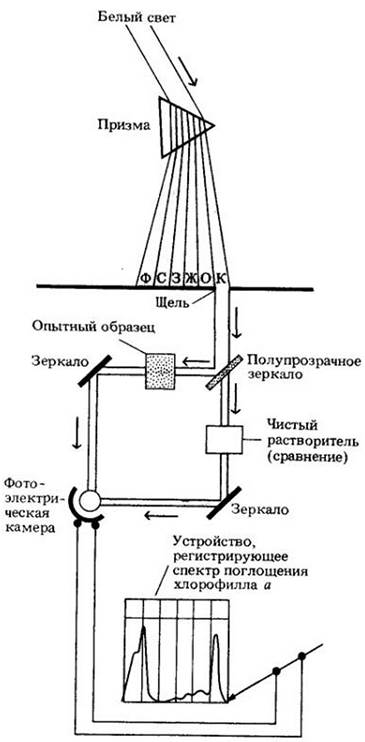
Рис. 7-6. Результаты опытов, проведенных Т. В. Энгельманом в 1882 г., позволили выявить спектр действия фотосинтеза у нитчатой водоросли. Энгельман, как и современные исследователи, определял скорость выделения О2, чтобы измерить скорость фотосинтеза. Однако в то время не было достаточно чувствительного прибора для определения кислорода. В качестве индикатора концентрации кислорода он выбрал бактерии, которые нуждаются в нем. Ученый заменил в световом микроскопе зеркало и диафрагму, используемые для освещения объекта, на «микроспектральный аппарат», который дает тонкие лучи света различной длины волны. Затем Энгельман поместил аппарат под микроскоп над стеклом с препаратом. Нитчатую водоросль он расположил параллельно спектру. Бактерии, нуждающиеся в кислороде, концентрировались в основном в том участке тела водоросли, на который падал свет, соответствующий красной и фиолетовой зонами спектра. Можно видеть, что спектр действия фотосинтеза в опытах Энгельмана соответствует спектру поглощения хлорофилла (см. рис. 7-5). Ученый сделал заключение, что фотосинтез зависит от света, поглощаемого хлорофиллом. Это прекрасный пример эксперимента, который ученые называют «элегантным», поскольку он был не только блестяще, но и просто выполнен и дал окончательный ответ на интересующий исследователя вопрос

Рис. 7-7. Верхняя кривая показывает спектр действия фотосинтеза, а нижние кривые — спектры поглощения в хлоропласте хлорофиллов а и b и каротиноидов. Совпадение спектров свидетельствует о том, что свет, поглощаемый хлорофиллами а и b и каротиноидами, используется при фотосинтезе
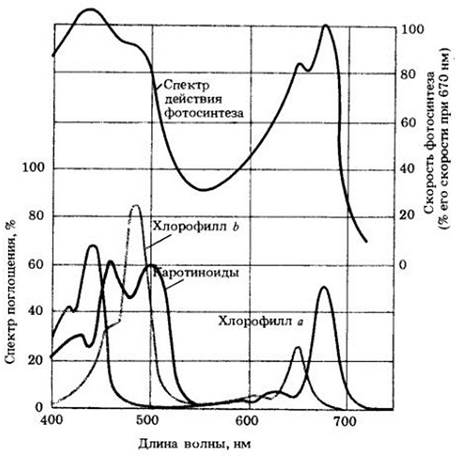
Когда пигменты поглощают свет и электроны поднимаются на более высокий энергетический уровень, дальнейшие события могут развиваться следующим образом: (1) энергия электрона рассеивается в виде тепла; (2) немедленно выделяется в виде световой энергии большей длины волны (это явление называют флуоресценцией, однако, когда происходит испускание света с некоторой задержкой, то данное явление называют фосфоресценцией) или (3) энергия запасается в форме химических связей, что и происходит в процессе фотосинтеза.
Если выделить молекулы хлорофилла и осветить их, они флуоресцируют. Иными словами, молекулы пигмента поглощают световую энергию, поэтому электроны немедленно поднимаются на более высокий энергетический уровень, а затем спускаются на более низкий, при этом выделяя большую часть поглощенной энергии в виде света. Свет, поглощенный изолированными молекулами хлорофилла, нс может преобразоваться в какую-либо другую форму энергии, полезную для живых систем. Хлорофилл способен преобразовать энергию света в химическую только в комплексе с определенными белками, находящимися в тилакоидах.
Фотосинтетические пигменты
Пигменты, которые участвуют в процессе фотосинтеза, — это хлорофиллы, каротиноиды и фикобилины.
Обнаружено несколько форм хлорофилла, которые различаются по молекулярной структуре. Хлорофилл а (рис. 7-8) характерен для всех фотосинтезирующих эукариот и цианобактерий. Полагают, что это основной пигмент, участвующий в процессах фотосинтеза у данных организмов.
Сосудистые растения, мхи, зеленые и эвгленовые водоросли содержат и хлорофилл b. Это вспомогательный пигмент, который расширяет спектр поглощения света в процессе фотосинтеза.
Когда молекула хлорофилла b поглощает свет, то возбужденный электрон передаст свою энергию хлорофиллу а, который затем в процессе фотосинтеза преобразует ее в энергию химических связей. Поскольку хлорофилл b поглощает свет других длин волн, нежели хлорофилл а, то тем самым расширяется диапазон длин волн, которые могут использоваться для фотосинтеза (рис. 7-7). Содержание хлорофилла b в листьях зеленых растений составляет в целом 1/4 общего количества хлорофилла.
У некоторых групп водорослей, в основном бурых и диатомовых, вместо хлорофилла b функционирует хлорофилл с. Фотосинтезирующие бактерии (не цианобактерии) нс могут использовать электроны воды и поэтому не выделяют кислород. Они содержат либо бактериохлорофилл (пурпурные бактерии), либо хлоробиум-хлорофилл (зеленые серные бактерии). Хлорофиллы b и с, а также фотосинтетические пигменты бактерий — это химические вариации основной структуры, показанной на рис. 7-8.
Рис. 7-8. Хлорофилл а — это большая молекула, содержащая в центре порфиринового кольца магний. К кольцу присоединена длинная, нерастворимая углеводородная цепь, которая служит своеобразным якорем для закрепления молекулы во внутренних мембранах хлоропласта. Хлорофилл Ь отличается от хлорофилла а тем, что содержит группу -СНО на месте группы -СН3, которая на рисунке окрашена. Чередование одиночных и двойных связей (в этом случае называемых сопряженными) характерно для порфиринового кольца не только хлорофиллов, но и всех остальных пигментов. Обратите внимание на сходство между молекулой хлорофилла, представленной здесь, и молекулой цитохрома (рис. 6-9)
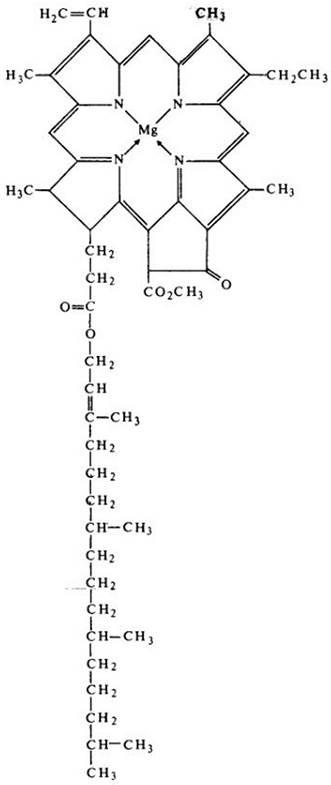
В преобразовании энергии участвуют и другие типы пигментов — каротиноиды и фикобилины. Энергия, поглощенная вспомогательными пигментами, должна быть перенесена на хлорофилл а; заменить его в процессе фотосинтеза данные пигменты не могут.
Каротиноиды — это красные, оранжевые или желтые жирорастворимые пигменты, обнаруженные в хлоропластах и у цианобактерий. Подобно хлорофиллам, каротиноиды хлоропластов погружены в тилакоидные мембраны. В хлоропластах обычно присутствуют две группы каротиноидов — каротины и ксантофиллы (последние в отличие от каротинов содержат кислород). Бета-каротин, обнаруженный в растениях, служит основным источником витамина А, необходимого человеку и животным (рис. 7-9). В зеленых листьях каротиноиды маскируются большим количеством хлорофилла.
Рис. 7-9. Группа родственных каротиноидов. Расщепление молекулы бета- каротина в указанном участке приводит к образованию двух молекул витамина А. Окисление витамина А дает ретиналь — пигмент, участвующий в зрении. У каротиноидов сопряженные связи расположены в углеродных цепях. Зеаксантин — пигмент, обусловливающий желтую окраску зерен кукурузы
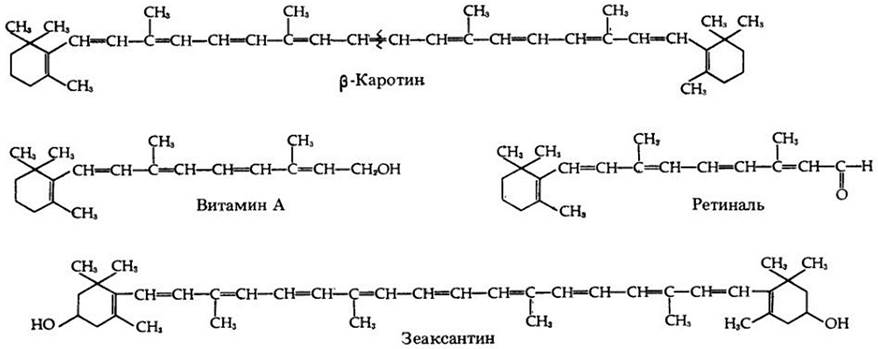
Фикобилины характерны для цианобактерий и хлоропластов красных водорослей. В отличие от каротиноидов фикобилины растворяются в воде.
Фотосистемы
В хлоропластах (рис. 7-1) хлорофилл и другие пигменты, погруженные в тилакоиды, собраны в функциональные единицы, называемые фотосистемами (рис. 7-10). Каждая фотосистема содержит около 250 — 400 молекул пигментов.
Рис. 7-10. Внутренняя поверхность тилакоида; препарат получен методом замораживания-скалывания. Полагают, что частицы, погруженные в мембраны, представляют собой структурные единицы фотосистем, участвующие в световых реакциях

Все пигменты фотосистемы могут поглощать фотоны (частицы световой энергии, см. приложение 1 к этой главе), но только одна молекула хлорофилла данной фотосистемы может использовать поглощенную энергию в фотохимических реакциях. Эта молекула хлорофилла называется реакционным центром фотосистемы, а другие молекулы пигментов называются антенными, поскольку они, подобно антеннам, собирают свет.
Световая энергия, поглощенная молекулой пигмента, переносится на другую молекулу, пока не достигнет реакционного центра, где локализована специальная молекула хлорофилла а. Когда эта молекула поглощает световую энергию, электроны поднимаются на более высокий энергетический уровень и переносятся на молекулу акцептора, вызывая поток электронов. Таким образом, молекула хлорофилла окисляется и становится положительно заряженной.
Имеются доказательства существования двух типов фотосистем. В фотосистеме I реакционный центр образован специфической молекулой хлорофилла а и обозначается как Р700 (Р означает пигмент, от англ. pigment; 700 — оптимум поглощения, нм). Реакционный центр фотосистемы II тоже образован специфической молекулой хлорофилла а и обозначается Р680(оптимум поглощения — при 680 нм).
В целом обе фотосистемы работают синхронно и непрерывно. Однако, как будет показано ниже, фотосистема I может функционировать отдельно.
Модель световых реакции
Рис. 7-11 иллюстрирует совместную работу двух фотосистем. Согласно данной модели, энергия света входит в фотосистему II, где утилизируется реакционным центром Р680 либо непосредственно, либо через молекулы пигментов. Когда Р680 возбуждается, его возбужденные энергизованные электроны (парами) переносятся на молекулу акцептора (возможно. хинона), обозначаемого Q из-за его способности гасить (от англ. quench) потерю энергии на флуоресценцию возбужденного Р680. Затем происходит реакция, которая на сегодня недостаточно хорошо изучена. Молекула Р680, потерявшая свои электроны, может заменить их электронами молекулы воды. Когда электроны воды идут к Р680, молекула воды диссоциирует на протоны и кислород. Это светозависимое окислительное расщепление молекул воды называют фотолизом. Ферменты, осуществляющие фотолиз воды, локализованы на внутренней стороне мембраны тилакоидов. Таким образом, фотолиз воды участвует в создании градиента протонов через мембрану. Марганец — важнейший кофактор ферментов, обеспечивающих выделение кислорода.
Рис. 7-11. Нециклический поток электронов и фотофосфорилирование. Эта зигзагообразная схема (Z-схема) показывает путь потока электронов от воды (внизу слева) к NADP(вверху справа) и энергетические взаимоотношения. Чтобы поднять энергию электронов от воды до уровня, необходимого для восстановления NADP до NADPH2, электроны должны высвобождаться дважды (коричневые линии) под действием фотонов света, поглощаемого фотосистемами I и II. После этого высокоэнергетические потоки электронов спускаются по путям, указанным черными стрелками. Процесс фотофосфорилирования ADP с образованиен АТР сопряжен с потоком электронов в электронотранспортной цепи, связывающей фотосистему II с фотосистемой I (рис. 7-12). Ферредоксин является донором электронов для восстановления NADP до NADPH2. Кроме того, ферредоксин выполняет и другие функции в хлоропласте: он отдает свои электроны ферментам, участвующим в биосинтезе аминокислот и жирных кислот
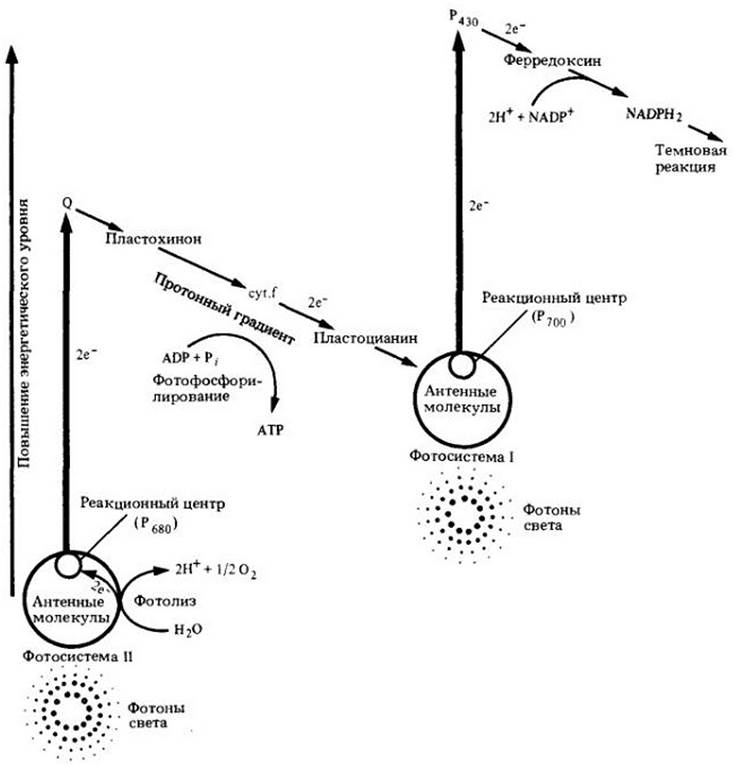
Электроны «спускаются» по электронотранспортной цепи к фотосистеме I. Компоненты этой цепи световых реакций напоминают компоненты электронотранспортной цепи дыхания; все состав входят цитохромы, белки, содержащие железо и серу, хиноны, а также хлорофилл и белок пластоцианин, содержащий медь. Электронотранспортная цепь между фотосистемами организована так, что АТР может образовываться из ADP и Рi, причем этот процесс аналогичен окислительному фосфорилированию, происходящему в митохондриях. В хлоропластах этот процесс называется фотофосфорилированием (рис. 7-12).
Рис. 7-12. Иллюстрация гипотезы хемиосмотического сопряжения как механизма фотофосфорилирования. Согласно гипотезе, протоны «накачиваются» через тилакоидную мембрану из стромы (внешняя среда) внутрь (тилакоидное пространство) с помощью переносчиков электронов, определенным образом расположенных в мембране. Концентрация протонов в тилакоидном пространстве увеличивается частично за счет расщепления воды, частично в результате окисления пгастохинона (PQ) на внутренней стороне мембраны. Когда протоны идут обратно по градиенту из тилакоидного пространства в строму, ADP фосфорилируется до АТР с помощью АТР-синтетазы. На каждые три протона, которые проходят через АТР-синтетазу, синтезируется одна молекула АТР. PC — пластоцианин; Fd — ферредоксин
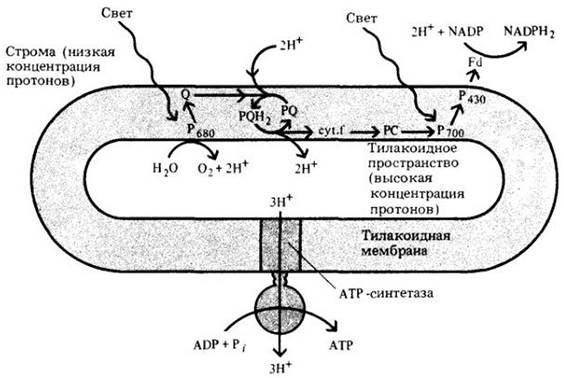
В фотосистеме I энергия света передаст электроны от Р700 на электронный акцептор Р430, который, вероятно, представляет собой железосерный белок. Следующий электронный переносчик — ферредоксин («фер» означает железо, а «редоксин» подчеркивает участие в окислительно-восстановительных реакциях) — это железосерный белок, но отличающийся от Р430. Ферредоксин затем передает свои электроны на кофермент NADP, который восстанавливается до NADPH2; при этом окисляется молекула Р700. Электроны молекулы Р700замещаются электронами фотосистемы II.
Таким образом, на свету электроны перемещаются от воды к фотосистемам II и I и NADP. Этот однонаправленный поток электронов от воды к NADP называется нециклическим потоком электронов; образование АТР, которое при этом происходит, называется нециклическими фотофосфорилированием.
Изменение свободной энергии (∆G) для реакции
Н2О + NADP —> NADPH2 + 1/2О2
составляет 51 ккал/моль. Энергия, эквивалентная 1 моль фотонов света с длиной волны 700 нм (эквивалент 1 моль фотонов называется Эйнштейном, Э), равна 40 ккал/Э. Необходимо четыре фотона для переброски двух электронов на уровень NADPH2, т. е. 160 ккал. Примерно одна треть энергии запасается в форме NADPH2. Общий энергетический выход нециклического потока электронов (идет 12 пар электронов от Н2О до NADP) составляет 12 АТР и 12 NADPH2.
Циклическое фотофосфорилирование
Как уже упоминалось, фотосистема I может работать независимо от фотосистемы II (рис. 7-13). В этом процессе, называемом циклическим потоком электронов, электроны передаются от Р700 на Р430 при освещении фотосистемы I. Вместо того чтобы идти к NADP, электроны идут по «запасному пути», связанному с I и II фотосистемами, и затем возвращаются в реакционный центр фотосистемы I. При этом образуется АТР; поскольку синтез АТР сопряжен с циклическим потоком электронов, его называют циклическими фотофосфорилированием. Предполагают, что это самый примитивный механизм, и, очевидно, он имеет место у некоторых фотосинтезирующих бактерий. Эукариотические клетки тоже способны синтезировать АТР при циклическом переносе электронов. Однако при этом не происходит разложения Н2О, выделения О2 и образования NADPH2.
Рис. 7-13. Циклическое фотофосфорилирование происходит только в фотосистеме I; АТР образуется из ADP так же, как показано на рис. 7-12, но кислород при этом не выделяется и NADP не восстанавливается
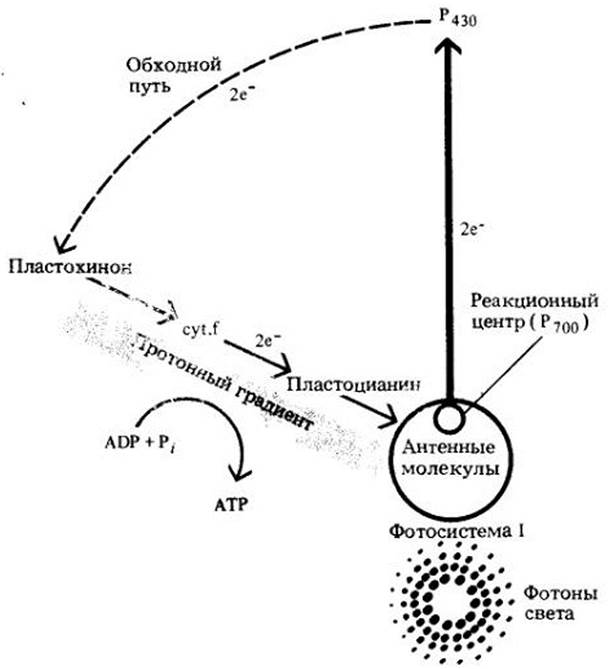
Полагают, что циклический транспорт электронов и фотофосфорилирование происходят в том случае, когда клетка с избытком снабжается восстановителем в форме NADPH2, но при этом требуется дополнительный АТР для других метаболических реакций.