БОТАНИКА ТОМ 2 - ФИЗИОЛОГИЯ РАСТЕНИЙ - 2007
6. ФИЗИОЛОГИЯ ОБМЕНА ВЕЩЕСТВ
6.13. Синтез аминокислот
Растения синтезируют все без исключения протеиногенные аминокислоты (см. рис. 1.11) самостоятельно, среди прочих — важные для человека ароматические аминокислоты (фенилаланин, тирозин, триптофан), а также валин, лейцин и изолейцин. Углеродные скелеты поставляются фотосинтезом. Вполне возможно (но еще не доказано!), что все аминокислоты синтезируются в хлоропластах, в дополнение к этому многие, вероятно, возникают и в других компартментах (например, глицин — в пероксисомах, серин — в митохондриях в процессе фотодыхания, см. рис. 6.75).
Основываясь на происхождении углеродных скелетов, аминокислоты можно поразделить на несколько групп (рис. 6.106): пируватное, 2-оксоглутаратное и оксалоацетатное семейства; 2-фосфогликолатное, шикиматное семейства и отдельно — гистидин, который образуется из рибозо-5- фосфата. Синтез глицина и серина из 2- фосфогликолата в процессе фотодыхания уже обсуждался (см. рис. 6.75), как и образование цистеина из серина (через образование О-ацетилсерина — см. рис. 6.90). Биосинтез гистидина в растениях не до конца изучен, но восходит к рибозо-5- фосфату. Остальные аминокислоты происходят частично либо полностью из 3-фосфоглицерата через образование фосфоенолпирувата. Образование пирувата или оксалоацетата из фосфоенолпирувата и возникновение оксалоацетата из пирувата в митохондриях обсуждалось ранее в связи с другой темой (см. рис. 6.79; 6.92; 6.94). Из оксалоацетата в митохондриях через образование цитрата может синтезироваться 2- оксоглутарат (см. рис. 6.94), но экспортированный в цитоплазму цитрат также может, как уже было сказано, превратиться в 2-оксоглутарат (см. 6.10.3.4).
6.13.2. Ароматические аминокислоты
Благодаря особому значению для метаболизма растений, который заключается не только в удовлетворении потребности в аминокислотах в процессе синтеза белков, три ароматические аминокислоты (триптофан, фенилаланин и тирозин) находятся под пристальным вниманием ученых. Биосинтетический путь, который начинается с фосфоенолпирувата и эритрозо-4- фосфата (см. рис. 6.106), был назван по характерному промежуточному метаболизму шикиматным путем. Шикиматный путь есть у растений, грибов и бактерий (но не у животных), у растений он локализован в пластидах. В шикиматном пути возникают дополнительно промежуточные продукты для биосинтеза большого числа других растительных соединений. Этот метаболический путь представляет собой некую «границу» между первичным и вторичным обменом веществ.
Рис. 6.106. Синтез углеродных скелетов различных семейств аминокислот в процессе ассимиляции CO2
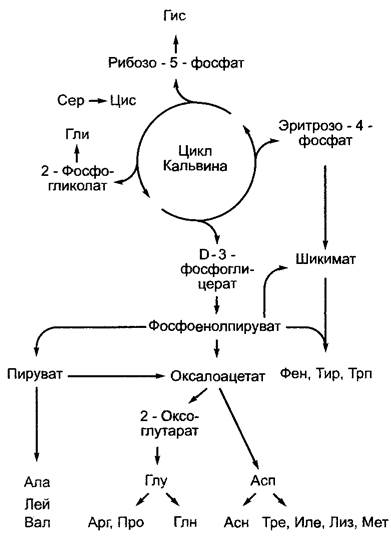
Эритрозо-4-фосфат является промежуточным продуктом цикла Кальвина и окислительного пентозофосфатного цикла, фосфоенолпируват синтезируется в процессе гликолиза и импортируется в хлоропласты Последовательность реакций представлена на рис. 6.107.
Рис. 6.107. Последовательность реакций шикиматного пути биосинтеза ароматических аминокислот фенилаланина, тирозина, триптофана
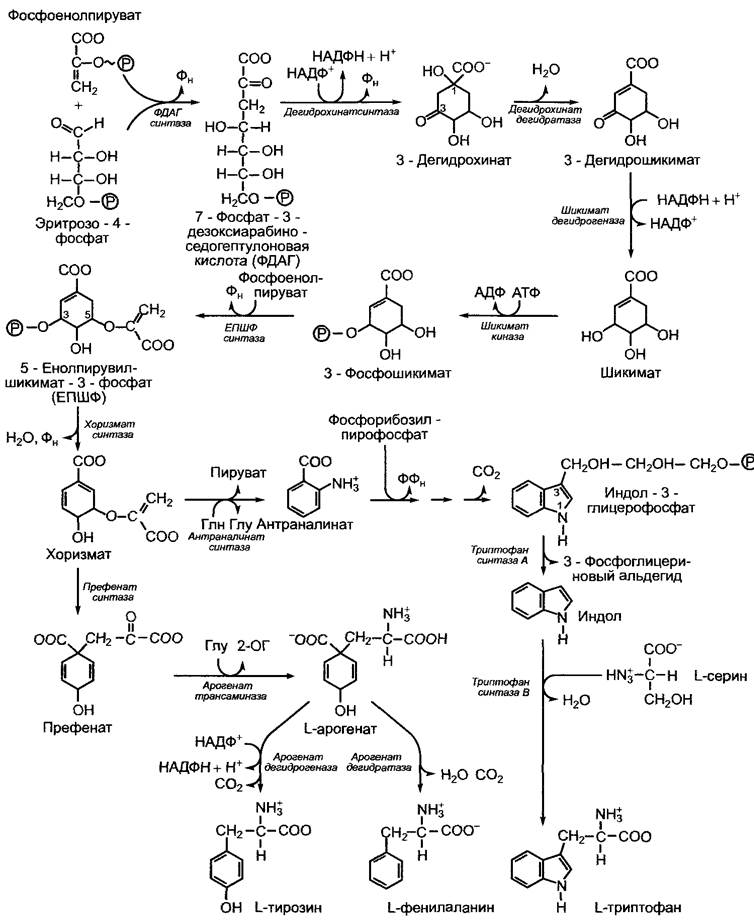
Фермент 5-енолпирувилшикимат-3-фосфатcинтаза (ЕПШФ-синтаза) является белком-мишенью для самого распространенного в мире гербицида глифосфата (N-фосфонометилглицина, рис 6 108), который представляет собой сильный конкурентный ингибитор, препятствующий присоединению фосфоенолпирувата к каталитическому центру. Тем не менее растения погибают не от недостатка ароматических аминокислот, а от накопления в тканях (особенно в меристемах) токсичной шикимовой кислоты.
На примере шикиматного пути можно очень хорошо показать регуляцию разветвляющихся путей обмена веществ конечными продуктами (рис. 6.108).
Рис. 6.108. Регуляция активности ферментов шикиматного пути с помощью продуктов реакций. Роль шикиматного пути в качестве поставщика предшественников для большого числа других метаболических путей в дополнение к синтезу белков здесь не показана. Глифосат (N-фосфонометилглицин) — гербицид, сильный конкурентный ингибитор фермента З-фосфо-5-енол- пирувилшикимат (ФЕПШ)-синтазы
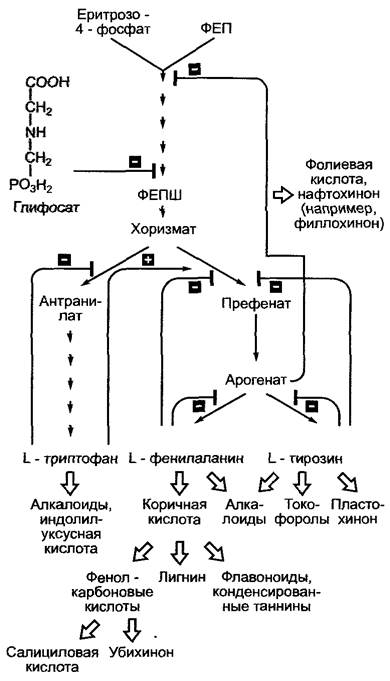
Триптофан тормозит свой собственный синтез и стимулирует синтез тирозина и фенилаланина. Фенилаланин или тирозин соответственно ингибируют свой собственный синтез. Таким образом удается избежать накопления ненужной аминокислоты, в то время как остальные продолжают синтезироваться.
6.13.3. Непротеиногенные аминокислоты и производные аминокислот
Наряду с 20 протеиногенными аминокислотами в растениях имеется более 400 других, непротеиногенных, аминокислот, которые часто (но не всегда) образуются из протеиногенных (рис. 6.109, А). Сюда также часто (но опять же не всегда) относят синтезирующиеся из аминокислот в результате декарбоксилирования биогенные амины (рис. 6.109, Б). Непротеиногенные аминокислоты могут служить транспортными и запасными метаболитами для восстановленного азота: так, например, упоминавшийся выше цитруллин (см. рис. 6.91) у Веtulасеае и Juglandасеае одновременно является промежуточным продуктом в биосинтезе аргинина. Транспортную и запасающую функции выполняет также канаванин бобовых (см. рис. 6.109, А). Одновременно это вещество, которое составляет порой до 10 % и более веса сухого вещества семени и содержит до 50 % связанного азота, представляет собой защитное вещество, токсичное для растительноядных животных. Токсичное действие канаванина основано на его структурном сходстве с L-аргинином (см. рис. 1.11). В результате в организме растительноядного животного может синтезироваться неправильный белок, так как аминоацил-тРНК-синтетаза животных, в отличие от растительной, не отличает L-аргинин от его аналога. В результате преобразований в организме животного из канаванина возникает к тому же нейротоксическая, непротеиногенная аминокислота каналин. Личинки жука Сагуedes brasiliensis, единственным источником питания которых являются семена бобовых, могут обезвреживать каналин, превращая его посредством восстановительного дезаминирования в гомосерин (см. рис. 6.109, А), естественное промежуточное соединение в биосинтезе треонина.
Рис. 6.109. Примеры растительных непротеиногенных аминокислот и их метаболизма (А); синтез биогенных аминов посредством декарбоксилирования аминокислот (В)
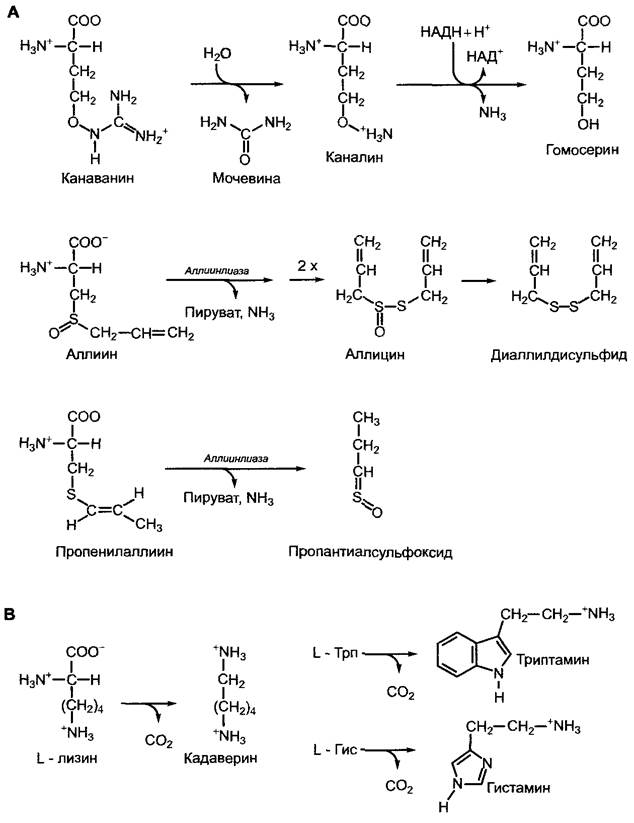
Непротеиногенные аминокислоты лука (Allium сера) и чеснока (Allium sativum) — пропенилаллиин и соответственно аллиин (см. рис. 6.109, А) — являются производными цистеина и предшественниками веществ, защищающих растение от потребления травоядными животными. При повреждении клеток, которые запасают в вакуолях аллиин (чеснок) и пропенилаллиин (лук), эти соединения расщепляются ферментом аллиинлиазой на пируват, аммиак и луковые масла. Аллицин и пропантиалсульфоксид являются сильными отпугивающими веществами (пропантиалсульфоксид — фактор, обусловливающий свойство лука вызывать слезотечение!) с одновременным бактерицидным действием (подавление развития бактерий в поврежденной ткани!), диаллилдисульфид отвечает за возникновение характерного запаха лука.
Многие биогенные амины появляются в результате декарбоксилирования из гомологичных им аминокислот; например, кадаверин — из лизина, триптамин — из триптофана, гистамин — из гистидина (см. рис. 6.109, Б). Биогенные амины могут быть биосинтетическими предшественниками алкалоидов (см. 6.16.3), триптамин является исходным веществом для синтеза фитогормона индолил-3-уксусной кислоты (см. 7.6.1.2), а гистамин наряду с серотонином и ацетилхолином входит в состав содержимого жгучих волосков (см. рис. 3.15) крапивы, вызывая зуд и болезненную реакцию ткани (образование волдырей) на коже позвоночных животных. Это сильнодействующее вещество предохраняет растение данной систематической группы от поедания животными (защита от растительноядных животных, см. 9.4.1)!