БОТАНИКА ТОМ 2 - ФИЗИОЛОГИЯ РАСТЕНИЙ - 2007
6. ФИЗИОЛОГИЯ ОБМЕНА ВЕЩЕСТВ
6.7. Ассимиляция сульфатов
Растение поглощает серу в форме сульфата SO24-, степень окисления +VI) и восстанавливает его до сульфида (S2-, степень окисления -II). Эти реакции проходят преимущественно в хлоропластах и нуждаются в продуктах фотосинтеза (АТФ, ферредоксин), однако у высших растений она может протекать и в корневой системе, где ее внутриклеточная локализация еще недостаточно ясна. В отличие от азота, который постоянно встраивается в органические соединения только в восстановленной форме, сера может быть вовлечена в синтез определенных органических соединений и в окисленной форме, например, в синтез сульфолипидов (см. 1.5.2, рис. 1.21), глюкозинолатов (см. 6.16.4) и сульфатированных флавоноидов. Однако преобладающая часть серы используется в виде сульфида. Сера степени окисления -II присутствует в аминокислотах и белках, восстановителе глютатионе, в некоторых коэн- зимах и железосерных центрах окислительно-восстановительных белков (например, ферредоксина, см. рис. 6.56). К ассимиляции сульфатов способны только бактерии, грибы и зеленые растения, в то время как животные должны получать восстановленные соединения серы с пищей.
Восстановление сульфата проходит, так же как восстановление нитрата, в 2 этапа:
![]()
Вопреки бытовавшим предположениям, не только у грибов и бактерий, но также и у зеленых растений при этом промежуточный сульфит (SО2-3) образуется в свободной форме, а затем восстанавливается до сульфида (S2-) (рис. 6.90).
Рис. 6.90. Фотосинтетическая ассимиляция сульфата: GSН — восстановленный глутатион; GSSG — окисленный глутатион (см. рис. 6.62)
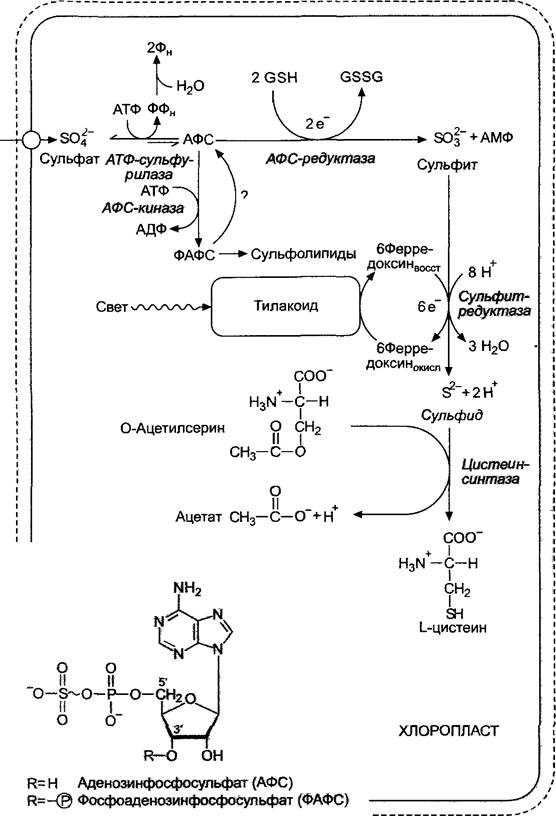
Последовательность реакций метаболизма начинается с образования активированного сульфата из АТФ и сульфата:
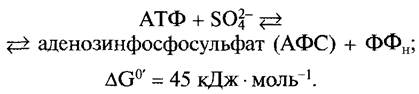
Равновесие этой сильноэндергоничной реакции смещено в сторону исходных веществ. Благодаря сопряжению (см. 6.1.5) двух экзергоничных реакций
ФФН + Н2O = 2ФН ∆G0′ = -33,5 кДж • моль-1
и
АФС + АТФ = ФАФС + АДФ G0' = -25 кДж • моль-1
общая реакция активации сульфата становится экзергоничной:
SO2-4 + 2АТФ = ФАФС + 2Фн+ АДФ G0' - = -13, 5 кДж • моль-1.
В равновесной реакции наряду с преобладающим ФАФС (З'-фосфоаденозин- фосфосульфат, рис. 6.90) присутствует очень мало АФС. Активация сульфата до АФС и ФАФС заключается в появлении фосфоангидридной связи (G0' = -71 кДжмоль • 1). В этой форме сульфатная группа может легко восстановиться. Отвечающий за это фермент в основном реагирует с АФС, поэтому ФАФС играет роль резерва активного сульфата. АФС-редуктаза переносит 2 электрона на серу в АФС с высвобождением сульфита (SO2-3). Электроны поставляются восстановленным глютатионом. Сульфит в результате поступления 6 электронов без заметных промежуточных этапов восстанавливается до сульфида (см. рис. 6.90), электроны поставляются ферредоксином. Реакция обладает не только формальным сходством с восстановлением нитрита: сульфитредуктаза похожа на нитритредуктазу также строением и выполняет перенос 6 электронов с помощью того же FеS4-сирогем-кофактора.
Получившийся сероводород используется непосредственно для синтеза цистеина. Высокое сродство к субстрату цистеин- синтазы гарантирует то, что сероводород не будет накапливаться в клетке. Реакция протекает с тиолизом акцепторной SН-молекулы О-ацетилсерина, поэтому фермент также называется О-ацетилсерин(тиол)- лиазой (или О-ацетилсеринсульфгидразой), он содержит в качестве простетической группы пиридоксальфосфат. Цистеин служит исходным продуктом в биосинтезе метионина и других низкомолекулярных тиолов, таких, как, например, глютатион или фитохелатин (см. 6.2.2.4). По современным данным, источником кислото-лабильной серы в железосерных центрах (см. рис. 6.56) является цистеин.