Фізіологія людини - Вільям Ф. Ґанонґ 2002
Дихання
Функції легень
Механіка дихання
Вдихання та видихання
Легені та грудна стінка мають еластичну будову. У нормі між ними є тільки тонкий прошарок рідини. Легені легко ковзають по грудній стінці, однак протидіють відділенню від неї, як, наприклад, два зволожені кусники скла легко ковзають один по одному, проте роз’єднати їх доволі складно. Тиск у просторі між легенями і грудною стінкою (внутрішньоплевральний тиск) є субатмосферним (див. рис. 34-3). Легені під час дихання розтягуються, наприкінці кожного видихання зусилля легень віддалитись від грудної стінки урівноважені здатністю грудної стінки відхилитись у протилежному напрямі. У випадках розгерметизації грудної клітки (наприклад, отвір у грудній стінці) легені колапсують (спадаються); коли вони втрачають свою еластичність, то грудна стінка розширюється і стає бочкоподібною.
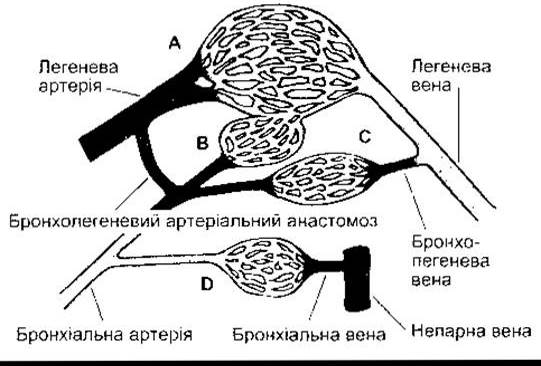
Рис. 34-5. Співвідношення між бронхіальним та легеневим кровопостачанням. Легеневі артерії створюють легеневу мережу капілярів. Бронхіальна артерія А забезпечує кров’ю мережу капілярів В, С, D. Мережа В - це бронхіальні капіляри, що забезпечують бронхіоли, які анастомозують з легеневими капілярами і впадають у легеневі вени. Мережа С - бронхіальні капіляри, що проходять до більшості бронхів; ці судини утворюють бронхолегеневі вени, які переходять у легеневі вени. Мережа капілярів D - це бронхіальні капіляри, що забезпечують кров’ю часткові та сегментарні бронхи. Вони утворюють справжні бронхіальні вени, які впадають у непарну або міжреберні вени. Ділянки, позначені темним кольором, мають низький вміст О2 (відтворено за дозволом з Murray JF: The Normal Lung. Saunders, 1986).
Акт вдихання є активним процесом. Скорочення дихальних м’язів збільшує об’єм грудної порожнини. Внутрішньоплевральний тиск в основі легень, який звично становить близько -2,5 мм рт. ст. (щодо атмосферного) на початку вдихання, знижується до -6 мм рт. ст. Легені переходять у стан більшого об’єму. Тиск у дихальних шляхах стає дещо негативним, і повітря надходить до легень (рис. 34-6). Наприкінці вдихання від моменту, коли сили розтягнення легень та грудної стінки втрачають урівноваженість, сила розтягнення легень спрямовує грудну стінку в положення видихання. Тиск у дихальних шляхах стає незначно позитивним, і повітря виходить з легень. У цілому дихальні м’язи в акті видихання не задіяні, тому його вважають пасивним процесом. Тільки на початку вдихання простежується скорочення деяких дихальних м’язів, що уповільнює видихання.
Сильне зусилля вдихання може знизити внутрішньо- плевральний тиск до -30 мм рт. ст. і більше, зумовлюючи значний ступінь наповнення легень. Якщо вентиляція збільшується, то об’єм видихання легень теж збільшується шляхом скорочення експіраторних м’язів і зменшення об’єму внутрішньогрудного простору.
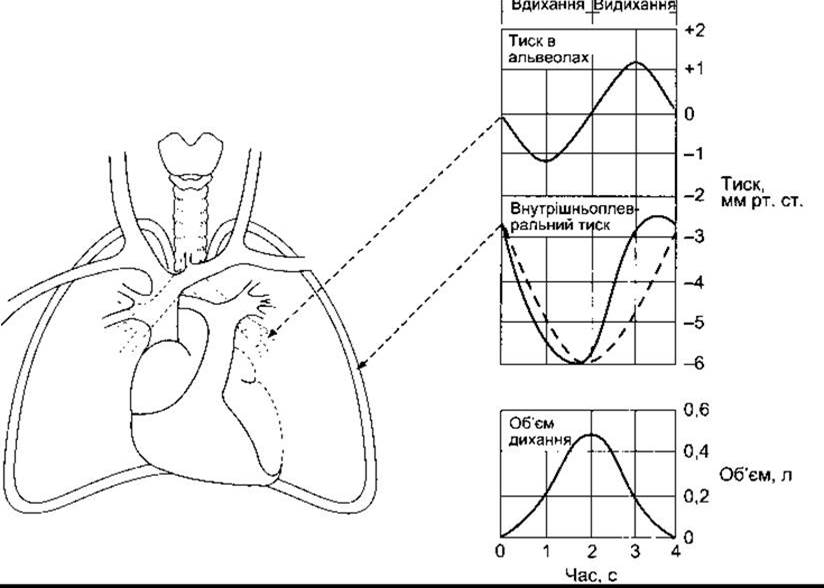
Рис. 34-6. Зміни внутрішньоплеврального (внутрішньогрудного) та внутрішньолегеневого тисків щодо атмосферного тиску під час вдихання та видихання. Зверніть увагу: якби не було повітряної та тканинної резистентності, то внутрішньоплевральний тиск відображала б штрихова лінія, тоді як справжня крива тиску зміщена ліворуч унаслідок цих резистентностей (див. також рис. 34-15).
Легеневі об’єми
Об’єм повітря, що надходить до легень під час кожного вдихання (або об’єм повітря, що виходить з легень під час кожного видихання) називають дихальним об’ємом. Об’єм повітря, який можна вдихнути під час максимального вдихання понад дихальний об’єм, називають резервним об’ємом вдихання.
Об’єм повітря, який можна видихнути під час максимального видихання понад дихальний об’єм, називають резервним об’ємом видихання.
Об’єм повітря, що залишається в легенях після максимального видихання, є залишковим. На рис. 34-7 показані легеневі об’єми за умов норми та їхні комбінації. Простір повітроносних шляхів, заповнений газом, який не переходить у кров легеневих судин, називають об’ємом мертвого простору.
Життєва ємність - це найбільший об’єм повітря, який можна вдихнути після максимального вдихання, часто він є клінічним показником функції легень, даючи корисну інформацію як про силу дихальних м’язів, так і про інші аспекти акту дихання. Частина життєвої ємності, яку видихають під час першої секунди форсованого видихання (FEVr з англ. forced expiration volume - об’єм форсованого видихання першої секунди) (рис. 34-8) дає важливу додаткову інформацію. Інколи життєва ємність є в межах норми, a FEV1 знижується завдяки підвищеному опору дихальних шляхів, наприклад, під час бронхоспазму в разі бронхіальної астми. Об’єм повітря, який вдихають за 1 хв (легенева вентиляція, хвилинний дихальний об’єм), у нормі сягає 6 л (500 мл кожного вдихання х 12 вдихань/хв). Максимально можлива вентиляція (ММВ), яку часто називають максимальною дихальною ємністю, є тим найбільшим об’ємом газу, який може ввійти в легені або вийти з них за 1 хв у разі максимально напруженого дихання. У нормі ММВ становить 125-170 л/хв.
Дихальні м’язи
Рух діафрагми спричинює зміну внутрішньогрудного об’єму в межах 75%. Охоплюючи дно грудної порожнини, діафрагма нависає над печінкою і рухається донизу під час вдихання як поршень. Хода руху діафрагми виносить від 1,5 до 7,0 см під час глибокого вдихання (рис. 34-9). Діафрагма складається з трьох частин: реберної, що створена волокнами, дотичними до зв’язок хребців; центрального сухожилля, до якого прикріплені волокна реберної частини; ніжки діафрагми. Центральне сухожилля водночас є внутрішньою частиною перикарда. Волокна ніжок охоплюють з обох боків стравохід і можуть перетискати його в разі скорочення. Оскільки реберна частина та ніжки діафрагми іннервовані різними волокнами діафрагмального нерва, то, відповідно, можуть скорочуватись незалежно. Наприклад, під час блювання та відригування внутрішньочеревний тиск збільшується завдяки скороченню реберних волокон. У період, коли волокна ніжок розслаблені, відбувається переміщення вмісту шлунка в стравохід. Значення волокон ніжок діафрагми в акті ковтання описане в Розділі 26.
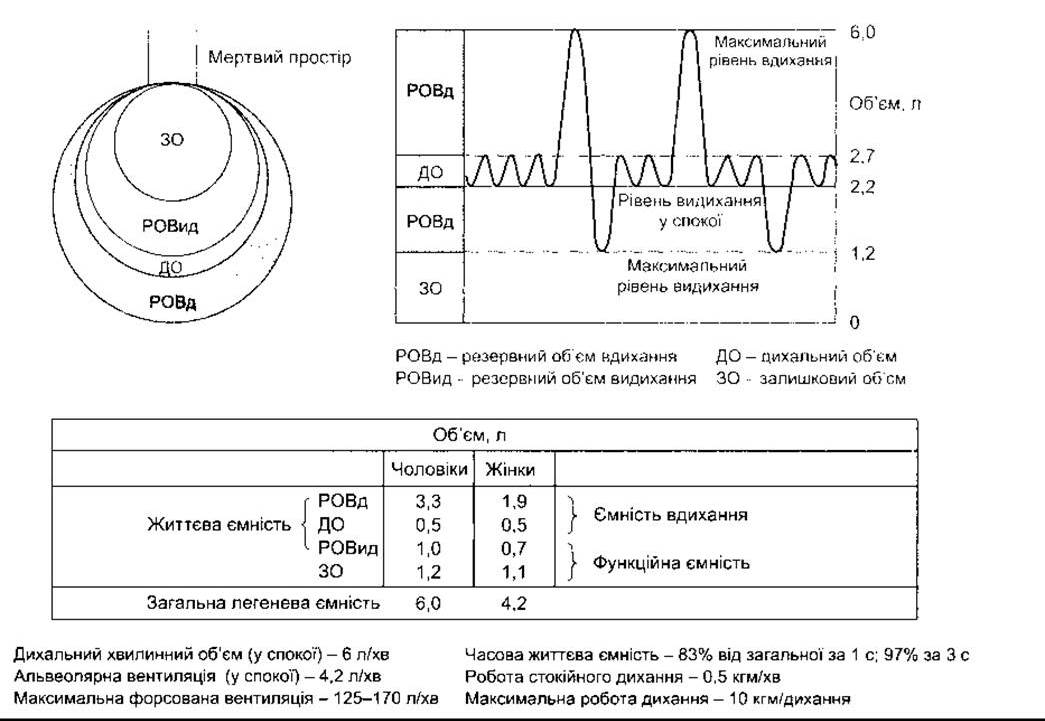
Рис. 34-7. Об’єми легень та деякі динамічні показники дихання. Діаграма вгорі праворуч відтворює покази спірометра у часі.
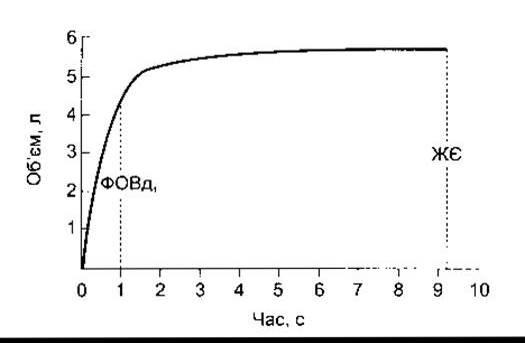
Рис. 34-8. Об’єм газу, що його вдихає нормальний дорослий чоловік під час форсованого вдихання, демонструючи ФОВд1 і життєву ємність (ЖЄ) (відтворено за дозволом з Crapo RO: Pulmonary-function testing. N Engl J Med 1994;331:25. Massachusetts Medical Society, 1994).
Іншими важливими інспіраторними м’язами (вдихання) є зовнішні міжреберні м’язи, які проходять косо, вперед і вниз від ребра до ребра. Точка опори ребер міститься на хребті, тому під час скорочення міжреберних м’язів піднімаються ребра, розташовані нижче. Це штовхає грудину допереду та збільшує передньо-задній діаметр грудної клітки. Поперечний діаметр теж збільшується, однак не настільки. Як діафрагма, так і зовнішні міжреберні м’язи в змозі самотужки підтримувати достатню вентиляцію легень. Перетин спинного мозку над третім шийним сегментом призводить до фатальних наслідків, якщо не задіяна штучна вентиляція легень, тоді як перетин нижче п’ятого шийного сегмента - ні, бо діафрагмальний нерв, що відходить від шийних сегментів С3-С5, залишається неушкодженим. Навпаки, у хворих з білатеральним паралічем діафрагмального нерва, проте зі збереженням іннервації міжреберних м’язів дихання затруднене, та достатнє для підтримання життя. Драбинчасті й грудинно-ключично-соскоподібні м’язи шиї є допоміжними м’язами вдихання і допомагають підняти грудну клітку в разі посиленого дихання. Зменшення внутрішньогрудного об’єму та посилене вдихання простежуються під час скорочення експіраторних м’язів (видихання). Внутрішні міжреберні м’язи діють саме так, тому що проходять косо вниз і назад від ребра до ребра й штовхають реберну клітку донизу під час скорочення. Скорочення м’язів передньої черевної стінки теж допомагає видиханню, тягнучи грудну клітку донизу і всередину, а в разі збільшення внутрішньогрудного тиску ще й піднімаючи діафрагму.

Рис. 34-9. Рентґенографія грудної клітки у випадку максимального видихання (ліворуч) і максимального вдихання (праворуч). Штрихова біла лінія відображає межі легень у разі максимального видихання (відтворено за дозволом з Comroe JH Jr: Physiology of Respiration, 2nd ed. Year Book Medical Publishers, 1974).
Голосова щілина
Під час вдихання дещо скорочуються відвідні м’язи гортані. Це приводить до відведення голосових зв’язок та відкривання голосової щілини. Під час ковтання привідні м’язи рефлекторно скорочуються, голосова щілина закривається, що попереджує потрапляння їжі, рідин чи блювотиння у легені. У хворих, що втратили свідомість або перебувають під анестезією, закриття голосової щілини може бути неповним, тому блювотиння може досягти трахеї і спричинити запальну реакцію легень (аспіраційна пневмонія).
М’язи гортані іннервовані гілками блукаючого нерва. Якщо відвідні м’язи паралізовані, то виникає інспіраторний стридор. Якщо ж паралізовані привідні м’язи, то їжа і рідина мають змогу потрапити в трахею, спричинюючи аспіраційну пневмонію та набряк легень. Двобічна ваготомія в шийному відділі спинного мозку, проведена на експериментальних тваринах, зумовлює повільний розвиток фатальної легеневої недостатності та набряк легень. Набряк легень настає у кінцевій стадії аспірації, проте інколи виникає в разі трахеотомії, проведеної перед ваготомією.
Тонус бронхів
У цілому гладкі м’язи бронхіальної стінки допомагають диханню. Бронхи під час вдихання розширюються, а під час видихання звужуються. Розширення (бронходилатацію) регулює симпатична, а звуження (бронхоконстрикцію) - парасимпатична іннервація. Стимулювання чутливих рецепторів дихальних шляхів подразниками та хімічними речовинами (такими як сульфурдіоксид) зумовлює рефлекторну бронхоконстрикцію через холінергічну іннервацію. Холодне повітря теж спричинює бронхоконстрикцію; подібно діють і фізичні вправи, бо форсоване дихання, що характерне для них, супроводжується охолодженням дихальних шляхів. У додаток, м’язи бронхів оберігають бронхи від кашлю. Зафіксовано циркадний ритм тонусу бронхів з максимальною схильністю до констрикції близько 6 год ранку та властивістю до максимальної дилатації о 18 год вечора. Як зазначено вище, бронходилатацію зумовлює ВІП. З іншого боку, речовина Р спричинює бронхоконстрикцію, подібно до дії аденозину через вплив на А - рецептори (див. Розділ 4), як і інші цитокіни та модулятори запалення. Роль цих субстанцій у патогенезі астми розглянута в Розділі 37, однак значення їх у фізіології регулювання бронхіального тонусу остаточно не з’ясоване.
Еластичність легень і грудної стінки
Зв’язок між рухом легень і грудної клітки можна розглянути на прикладі живих об’єктів. В експерименті ніздрі обстежуваному закривають спеціальною прищіпкою, і людина дихає тільки ротом через спірометр, у якому є спеціальний клапан для вимірювання тиску. Як тільки людина вдихне деякий об’єм повітря, клапан спрацьовує і перекриває подальше його надходження. Потім відбувається записування тиску повітря в дихальних шляхах; дихальні м’язи в цьому разі розслаблені. Записування тиску повторюють під час кожного вдихання і видихання різних об’ємів повітря. Криву співвідношення тиску в дихальних шляхах до об’єму повітря називають кривою релаксації тиску (рис. 34-10) для всієї дихальної системи. За об’єму газу в легенях наприкінці кожного видихання тиск дорівнює нулю (об’єм релаксації, що дорівнює об’єму функцій- ного залишкового простору). Тиск позитивний у разі більшого об’єму повітря в легенях і негативний у випадку меншого. Співвідношення зміни об’єму легень до зміни тиску в дихальних шляхах (AV/AP) відображає здатність легень і грудної клітки до розтягу (еластичність). У нормі ця залежність простежується за такого тиску, коли крива релаксації найкрутіша, а об’єм наближається до 0,2 л/см Н2О. Важливе значення в цьому разі має об’єм повітря в легенях. Наприклад, особи з одною легенею мають приблизно половину AV за деякого АР. Співвідношення дещо збільшується у випадку вимірювань під час видихання, на відміну від вдихання. Тому інформативніше вивчати криву тиск-об’єм під час усього акту дихання. Крива зміщується донизу і праворуч (еластичність зменшується) унаслідок легеневої недостатності та інтерстиційного легеневого фіброзу (рис. 34-11) і догори та ліворуч (еластичність зростає) у разі емфіземи (див. Розділ 37). Отже, це співвідношення є статистичним мірилом взаємодії легень і грудної стінки. Резистентність легень і грудної стінки зумовлена різницею тисків та залежить від об’єму потоку повітря. Вимірювання її є динамічнішим і залежить від опору повітря в дихальних шляхах.
Поверхневий натяг альвеол
Еластичність легень суттєво залежить від поверхневого натягу плівки рідини, що вкриває стінку альвеол. Значення цієї складової за різних дихальних об’ємів можна виміряти в разі видалення легень з тіла експериментальних тварин та почергового наповнення їх фізіологічним розчином і повітрям, одночасно вимірюючи внутрішньоплевральний тиск. Оскільки фізіологічний розчин знижує поверхневий натяг альвеол до нуля, то крива тиск-об’єм визначить тільки еластичність легеневої тканини (рис. 34-12). Крива, отримана внаслідок надування легень повітрям, сумарно визначає еластичність легеневої тканини та поверхневий натяг альвеол. Різниця між двома кривими значно зменшується зі збільшенням легеневих об’ємів. Поверхневий натяг альвеол є також меншим, ніж очікуваний поверхневий натяг у випадку застосування водно-повітряної суміші.
Сурфактант
Зниження поверхневого натягу зі зменшенням об’єму альвеол зумовлене наявністю сурфактанту (речовини ліпідної природи) у рідині, що покриває поверхню альвеол. Сурфактант - це суміш дипальметилфосфатидилхоліну (ДПФХ) та інших ліпідів і білків (табл. 34-2). Якби поверхневий натяг у разі зменшення об’єму альвеол під час видихання не знижувався, то згідно з законом Лапласа альвеоли просто б колабували (див. Розділ 30). В альвеолах, як у сферичних структурах, сила тиску розтягнення відповідає подвійній силі натягу, поділеній на радіус (Р=2Т/r). Якщо Т не зменшується під час зменшення r, то сила напруження перевищує тиск розтягнення. Отже, сурфактант дає змогу уникнути набряку легень. З’ясовано, що без сурфактанту тиск поверхневого натягу альвеол знизився б до 20 мм рт. ст., унаслідок чого розпочалась би вільна трансудація плазми і крові в альвеоли. Фосфоліпіди складаються з гідрофільної «головної» частини і двох паралельних гідрофобних «хвостових» частин з жирних кислот (див. Розділ 1). Хвостовими частинами вони спрямовані у просвіт альвеол. Поверхневий натяг альвеол прямо пропорційний до концентрації сурфактанту в одиниці площі. Молекули фосфоліпідів відштовхуються одна від одної зі збільшенням об’єму альвеол під час вдихання та зі збільшенням поверхневого натягу. І навпаки, ці ж молекули щільно об’єднуються, якщо поверхневий натяг зменшується під час видихання.
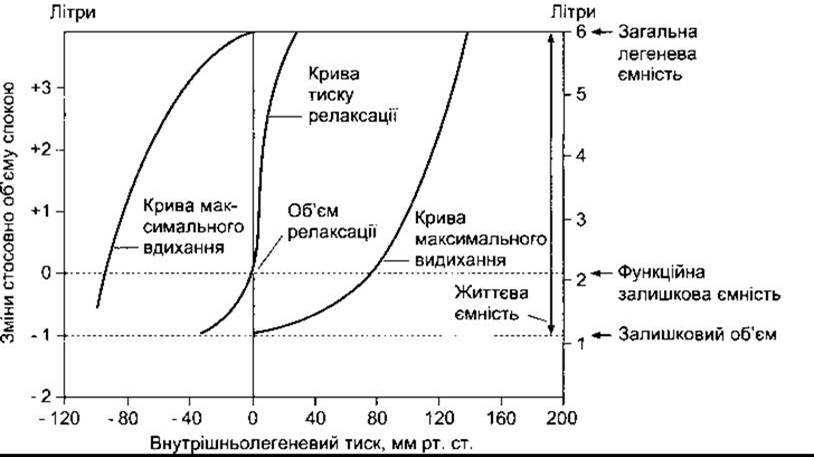
Рис. 34-10. Взаємозв’язок між внутрішньоплевральним тиском та об’ємом. Середня крива є кривою тиску релаксації дихальної системи, тобто крива статичного тиску, отримана для різного ступеня роздутих чи стиснутих легень; внутрішньолегеневий тиск (тиск еластичного натягу) вимірюють, коли дихальні шляхи закриті. Об’єм релаксації визначає точка, коли натяг грудної клітки і легень урівноважений. Нахил кривої відповідає натягу легень та грудної стінки. Криві максимального вдихання та видихання свідчать про тиск у дихальних шляхах, який утворюється під час максимального вдихання та видихання.
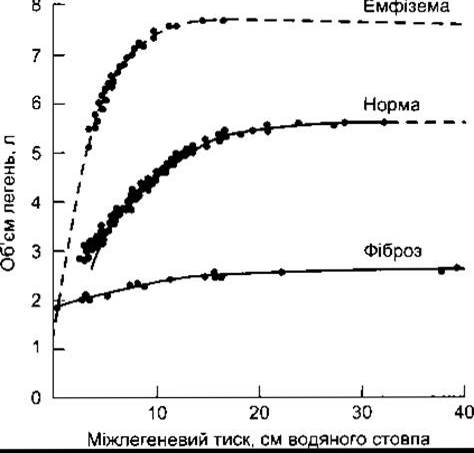
Рис. 34-11. Криві статичних співвідношень тиск-об’єм для видихання у нормальних осіб та осіб з тяжкою емфіземою і легеневим фіброзом (модифіковано та відтворено за дозволом з Pride NB, Maćkiem PT: Lung mechanics in disease. In: Handbook of Physiology. Section 3, The Respiratory System. Vol. Ill, part 2. Fishman AP [editor]. American Physiology Society, 1986).
Сурфактант виробляють альвеоцити типу II (рис. 34- 13). Типові пластинчасті тільця, - мембранозв’язані органели, - містять веретена фосфоліпідів, які утворюються в цих клітинах і секретуються в просвіт альвеол шляхом екзоцитозу. Ліпідні трубочки, які називають тубулярним мієліном, формуються з використаних тілець, а сам тубулярний мієлін утворює плівку фосфоліпідів. Деякі протеїноліпідні комплекси сурфактанту синтезуються в альвеолоцитах типу II шляхом ендоцитозу і рециклізують.
Будова фосфоліпідної плівки сурфактанту значно зумовлена наявністю білків, провідну роль у цьому відіграють чотири унікальні білки SP-A, SP-B, SP-C, SP-D. Наприклад, SP-А є великим глікопротеїном, що містить у структурі домен, подібний за будовою до колагену. Він виконує різноманітні функції, у тім числі регулює синтез та секрецію сурфактанту альвеоцитами типу II за механізмом зворотного зв’язку. Білки SP-B і SP-С менші, вони сприяють утворенню мономолекулярної плівки фосфоліпідів. Подібно до SP-A, SP-D теж є глікопротеїном, хоча функція його ще не визначена. Однак SP-A і SP-D належать до групи білків, задіяних у формуванні вродженого імунітету.
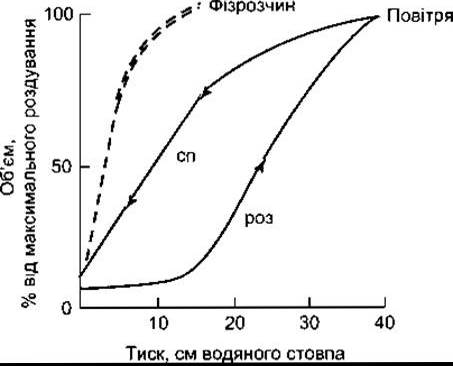
Рис. 34-12. Зв’язок тиск-об’єм у легенях кота після видалення їх з організму. Повітря - легені роздуті повітрям (роз) і без повітря (сп). Фізіологічний розчин - легені роздуті фізіологічним розчином і без нього (відтворено за дозволом з Morgan ТЕ: Pulmonary surfactant. N Engl J Med 1971 ;284:1185).
Сурфактант відіграє важливу роль під час народження людини. Хоча плід виконує дихальні рухи внутрішньоутробно, та все-таки легені до пологів колабовані. Після народження дитина робить декілька потужних рухів вдихання, і легені розправляються. Сурфактант оберігає легені від повторного колапсу. Дефіцит сурфактанту є важливою причиною респіраторного дистрес-синдрому новонароджених (РДСН; хвороби гіалінових мембран) - важкого захворювання легень, яке виникає у немовлят, народжених перш, ніж почала діяти їхня система сурфактанту. Поверхневий натяг легень у таких немовлят настільки високий, що в багатьох ділянках альвеоли зазнали спадіння (ателектаз). Додатковим фактором формування РДСН є затримка рідини в легенях. У пренатальному періоді епітеліальні клітини легень виділяють рідину, у якій міститься Cl-. Під час народження відбувається абсорбція цими клітинами Na+ через натрієвий канал епітеліальних клітин (NaEK), і рідина повторно абсорбується з Na+. Довготривала недорозвинутість NaEK спричинює легеневі аномалії в разі РДСН.
Призначення в інгаляціях тільки фосфоліпідів дає незначний ефект у випадку лікування РДСН. Однак сьогодні можна використати для інгаляцій синтетичний сурфактант або сурфактант, добутий з бичачих легень. Їхнє застосування під час пологів з профілактичною і замісною метою значно знизило важкість перебігу РДСН та, на жаль, не знизило частоти хронічних легеневих захворювань у немовлят, які вижили.
Таблиця 34-2. Склад сурфактанту
Складова |
Вміст, % |
Дипальмітолфосфатидилхолін |
62 |
Фосфатидилгліцерин |
5 |
Інші фосфоліпіди |
10 |
Нейтральні ліпіди |
13 |
Білки |
8 |
Вуглеводи |
2 |
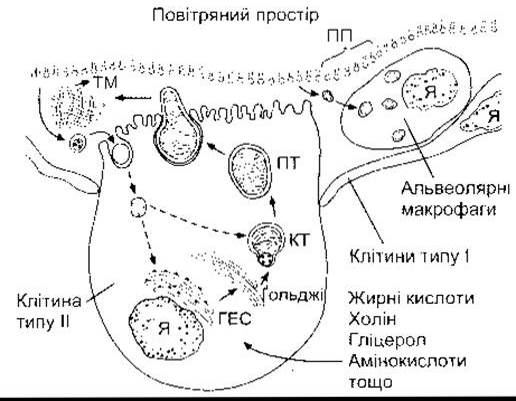
Рис. 34-13. Утворення і метаболізм сурфактанту. Пластинчасті тільця (ПТ) утворені альвеолоцитами типу II і секретовані екзоцитозом. Вивільнений з пластинчастих тілець матеріал перетворюється у тубулярний мієлін (ТМ) і є ймовірним джерелом фосфоліпідної поверхневої плівки (ПП). Частину сурфактанту поглинають альвеолярні макрофаги, проте більшість - ендоцитоз альвеолоцитами типу II; Я - ядро; ГЕС - ґранулярна ендоплазматична сітка; КТ - композитні тільця (відтворено за дозволом з Wright JR: Metabolism and turnover of lung surfactant Am Rev Respir Dis 1987; 136:426).
Сформованість системи сурфактанту часто спричинює виникнення часткових (сегментарних) ателектазів у пацієнтів, які зазнали кардіохірургічного втручання з використанням штучної вентиляції легень та зупинкою самостійного дихання. Крім того, дефіцит сурфактанту є чинником деяких патологій, що супроводжуються непрохідністю головного бронха, оклюзією однієї легеневої артерії чи довготривалою інгаляцією 100% О2. Виявлено зменшення вмісту сурфактанту в легенях курців. Цікаві результати дослідження щодо надлишку ліпідів і білків сурфактанту в експериментальних мишей з нокаутом гена GM- CSF. Значення GM-CSF в гемопоезі описане у Розділі 27. Важливо, що патологічні зміни, виявлені в легенях мишей з нокаутом гена, подібні до змін у легенях людей з легеневим альвеолярним протеїнозом.
Робота під час дихання
Завдяки роботі дихальних м’язів еластичні тканини грудної стінки і легень розтягуються (еластична робота). Під час руху нееластичних тканин (віскозна резистентність) дихальними шляхами проходить повітря (табл. 34-3). Оскільки добуток тиску на об’єм (г/см2 х см3 = г х см) має те саме значення, що й робота (сила х відстань), то роботу під час дихання визначають за допомогою кривої релаксації тиску (рис. 34-10 і 34-14). Нарис. 34-14 загальна еластична робота, що відповідає вдиханню, є в ділянці АВСА. Зазначимо, що крива тиску релаксації всієї дихальної системи відмінна тільки для легень. Ділянка ABDEA відображає фактичну еластичну роботу, затрачувану на збільшення об’єму самих легень. Значення еластичної роботи, витраченої на наповнення всієї дихальної системи, менше порівняно з затраченим на наповнення тільки легень, тому частково ця робота відбувається завдяки еластичній енергії, збереженій у грудній стінці. Еластична енергія грудної клітки (ділянка AFGBA) дорівнює енергії, яку отримують легені (ділянка AEDCA).
Таблиця 34-3. Складові роботи дихання під час спокійного вдихання і внесок кожної у відсотках

Резистентність тертя під час руху повітря порівняно мала в разі спокійного дихання, однак зі зміною об’єму легень у період вдихання й видихання та зміною внутрішньоплеврального тиску ця резистентність суттєво змінюється (див. рис. 34-6). Ось чому гістерезисна крива відрізняється від прямої лінії залежності тиску від об’єму легень (рис. 34-15). На схемі зона AXBYA відображає роботу, витрачену на подолання резистентності дихальних шляхів і легеневої тканини. Енергія, затрачувана на рух повітря в дихальних шляхах, збільшується в разі турбулентності руху під час швидкого дихання порівняно з тим, коли повітряний потік ламінарний. Загальна робота дихання в спокої є в межах від 0,3 до 0,8 кгм/хв. Вона суттєво зростає у випадку фізичного навантаження, проте в будь-якому разі кожна особа витрачає під час фізичного навантаження на саме дихання лише 3% від усієї затрачуваної енергії. Робота, потрібна для дихання, значно зростає за таких хворіб, як емфізема, астма, набуті вади серця із задишкою та ортопное. Співвідношення еластичності до напруги у дихальних м’язах майже таке, як у скелетних та серцевому м’язах, і коли м’язи перерозтягнуті, то вони скорочуються з меншою силою, їхня втома та недостатність (нагнітальна недостатність) супроводжуються неадекватною вентиляцією легень (див. Розділ 37). З невідомих причин амінофілін збільшує силу скорочення діафрагми людини, тому його використовують для лікування недостатності вентиляції легень.
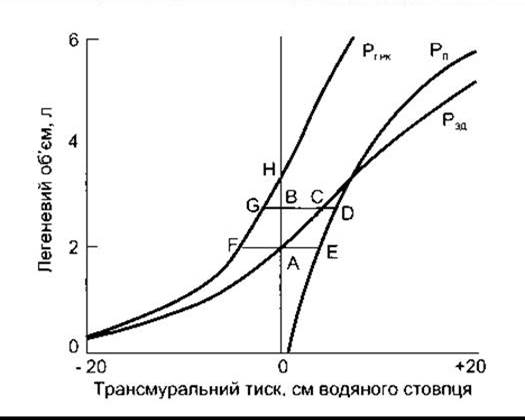
Рис. 34-14. Крива тиску релаксації у загальній дихальній системі (Р ) і криві релаксації тиску для легень (Рл) та в грудній клітці (Р ). Трансмуральний тиск для легень визначено як внутрішньолегеневий мінус внутрішньоплевральний, для стінки грудної клітки - як внутрішньоплевральний мінус зовнішній (барометричний), для загальної дихальної системи - як внутрішньолегеневий мінус барометричний тиск (модифіковано з Mines AH: Respiratory Physiology, 3rd ed. Raven Press).
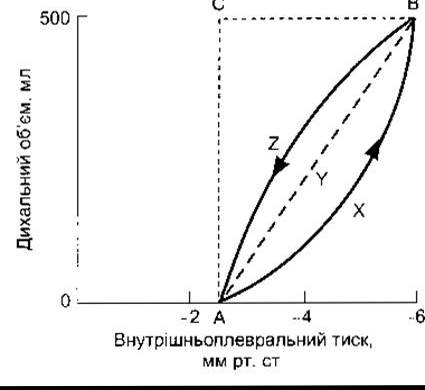
Рис. 34-15. Схематичне зображення змін тиску та об’ємів під час спокійного вдихання (лінія АХВ) та видихання (лінія BZA). AYB - лінія натягу.
Відмінності вентиляції та кровопостачання у різних частинах легень
У вертикальному положенні вентиляція одиниці об’єму легень ліпша в базальних відділах, а не у верхівці. Причина полягає в тому, що на початку вдихання внутрішньоплевральний тиск менш негативний у базальній частині легень порівняно з верхівкою (рис. 34-16). Якщо різниця між внутрішньолегеневим та внутрішньоплевральним тиском стає меншою, ніж на верхівці, то легені менше розтягуються. І навпаки, якщо легені розтягуються більше, то максимальний об’єм легені зростає. З огляду на жорсткість легень збільшення їхнього об’єму на одиницю супроводжується меншим підвищенням тиску, ніж тоді, коли легені були попередньо більше розтягнуті і вентиляція збільшується в базальній частині легень. Кровопостачання теж більше у цій ділянці порівняно з верхівкою (див. нижче). Зміна кровоплину від верхівки до базальних відділів є значиміша від відповідних змін вентиляції легень. Тому співвідношення вентиляції-перфузії є менше в основі легень і більше на верхівці. Деякі відмінності вентиляції та перфузії від верхівки до основи легень приписують земному тяжінню. Ці зміни нівельовані в положенні лежачи, і маса легень у положенні стоячи робить внутрішньоплевральний тиск нижчим у базальному відділі. Проте нещодавні космічні польоти засвідчили невідповідність вентиляції та кровопостачання в різних частинах легень, що простежуються в стані невагомості у космонавтів. Очевидно, є ще й досі невідомі факти, які також беруть участь у створенні такої відмінності.
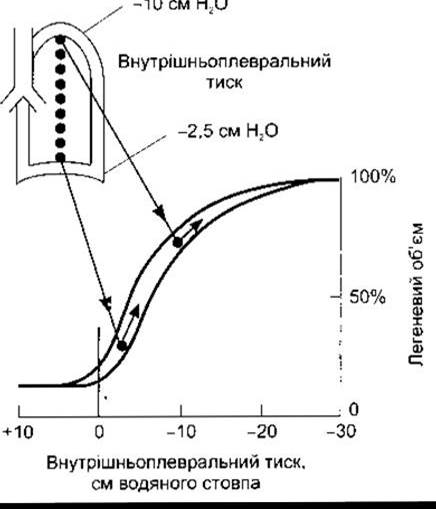
Рис. 34-16. Внутрішньоплевральні тиски у положенні стоячи та їхній вплив на вентиляцію. Зверніть увагу, оскільки внутрішньоплевральний тиск є атмосферним, то більший від’ємний внутрішньоплевральний тиск на верхівці утримує легені у більш розтягнутому положенні на початку вдихання. Подальше збільшення об’єму на одиницю збільшення внутрішньо- плеврального тиску менше, ніж на початку, бо розширення легень є важчим (відтворено за дозволом з West JB: Ventilation/Blood Flow and Gas Exchange, 3rd ed. Blackwell, 1977).
З’ясовано, що в разі дуже малих об’ємів легень, особливо після форсованого видихання, внутрішньоплевральний тиск в основі легень може перевищувати атмосферний тиск у дихальних шляхах, що призведе до колапсу дихальних шляхів малого діаметра, наприклад респіраторних бронхіол (закриття дихального шляху). У старших людей та пацієнтів з хронічними легеневими захворюваннями еластичні властивості легень послаблені, що веде до зниження внутрішньоплеврального тиску. Тому перекриття дихального шляху може виникнути в основі легень у положенні стоячи і без форсованого видихання за об’ємів, більших від залишкової функційної ємності легень.
Клінічне значення впливу гравітації на вентиляцію виявляється у поліпшенні артеріальної оксигенації у хворих з одностороннім легеневим захворюванням, що лежать на боці здорової легені. У випадку з немовлятами ця залежність обернена, хоча й досі не з’ясовано, з яких причин.
Мертвий простір та нерівномірна вентиляція
Оскільки газообмін у дихальній системі відбувається тільки в термінальній частині дихальних шляхів, то газ, який міститься в решті дихальних шляхів, вилучений з газообміну кров’ю легеневих капілярів. У нормі об’єм цього мертвого простору приблизно відповідає масі тіла у фунтах. Наприклад, якщо людина має масу 68 кг (150 фунтів), то тільки перші 350 з 500 мл повітря вдихання надходять в альвеоли. І навпаки, з кожним видиханням перші 150 мл становить газ мертвого простору і тільки наступні 350 мл надходять з альвеол. Отже, альвеолярна вентиляція - це об’єм повітря, що надходить до альвеол за 1 хв. Звісно, альвеолярна вентиляція менша, ніж хвилинний дихальний об’єм. Зверніть увагу, що через мертвий простір поверхневе швидке дихання зумовлює меншу альвеолярну вентиляцію, ніж повільне глибоке дихання за однакових хвилинних дихальних об’ємів (табл. 34-4).
Важливо розрізняти анатомічний мертвий простір (об’єм дихальної системи, за винятком альвеол) та загальний (фізіологічний) мертвий простір (об’єм газу, який не обмінюється з кров’ю, так звана втрачена вентиляція). У здорових осіб ці два мертві простори ідентичні, проте під час хворіб частина альвеол вилучена з газообміну, а частина гіпервентильована. Об’єм газу в неперфузованих та гіпервентильованих альвеолах, потрібний для артеріалізації в альвеолярних капілярах, є частиною газового об’єму мертвого простору (неврівноваженого). Анатомічний мертвий простір можна виміряти, аналізуючи криву одиничного дихання N2 (рис. 34-17). Після звичайного вдихання особа якнайглибше вдихає чистий О2, потім видихає рівномірно так, щоб вміст N2 можна було виміряти. Початковий газ, який видихають (фаза І), - це газ, що заповнював мертвий простір і який не вміщує N2. Далі йде суміш газів мертвого простору та альвеолярного газу (фаза II), а потім альвеолярний газ (фаза III). Об’єм мертвого простору - це об’єм газу, який видихають від пікового вдихання до середини фази II (див. рис. 34-17).
Фазу III на кривій N2 одиничного акту дихання позначають як кінцевий об’єм (КО), вона проходить у фазу IV, під час якої вміст N2 у газі, що його видихають, збільшується. Показник КО - це об’єм у легенях понад залишковий, за якого дихальні шляхи зменшуються. Він залежить від частин легень, що починають змикатися, оскільки трансмуральний тиск у цих ділянках знижується (див. вище). Газ у верхніх ділянках легень більше збагачений N2, ніж газ у нижніх залежних частинах, бо альвеоли у верхніх частинах розтянуні на початку вдихання O2 (див. вище), тому N2 у НИХ менше змішується з O2. Також виявлено, що у більшості нормальних осіб крива фази III має легко позитивний нахил перед досяганням фази IV. Це свідчить, що саме під час фази III відбувається поступове пропорційне збільшення газу, що його видихають і який надходить з порівняно збагачених N2 верхніх частин легень. Характер вентиляції в легенях також можна оцінити за допомогою інгаляції радіоактивного ізотопу інертного газу ксенону (113Хе) та моніторингу органів грудної клітки з визначенням рівня радіації. Ділянки, у яких простежується низька радіоактивність, відповідають поганій вентиляції.
Таблиця 34-4. Вплив зміни частоти і глибини дихання на альвеолярну вентиляцію
Частота дихання |
30/хв |
10/хв |
Дихальний об’єм |
200 мл |
600 мл |
Хвилинний об’єм |
6 л |
6 л |
Альвеолярна вентиляція |
(200-150)х30 =1500 мл |
(600-150)х10 =4500 мл |
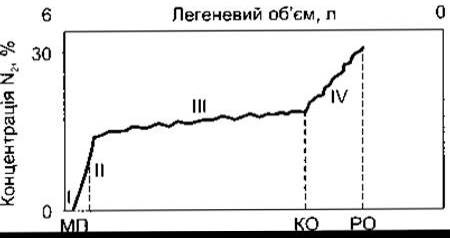
Рис. 34-17. Крива одиничного дихання N2. Після звичайного вдихання особа глибоко вдихає чистий О2, потім повільно видихає. Наведено зміни концентрації N2 y газі, який видихнули; різні фази відображені на кривій римськими цифрами; МП - мертвий простір; КО - кінцевий об’єм; РО - резервний об’єм.
Загальний мертвий простір можна обчислити з РCO2 У повітрі, яке видихають, РСO2 артеріальної крові та дихального об’єму (рівняння Бора)
![]()
де РеCO2 - експіраторний газ (який видихають); ДО - дихальний об’єм; РаCO2 - артеріальний газ; VMП - мертвий простір; РіСО2 - інспіраторне повітря (яке вдихають).
Значення РіСО2 х VMП таке мале, що ним можна знехтувати, і рівняння обчислюють для VMП. Якщо, наприклад: РЕСО2 = 28 мм рт. ст.; РаСО2 = 40 мм рт. ст.; VДО = 500 мл; то VMП= 150 мл.
За цим рівнянням можна також визначити мертвий анатомічний простір, якщо замінити РаСО2 на альвеолярний РСО2 (РАСО2), ЯКИЙ Є значенням РСО2 в останні 10 мл у експіраторному газі (див. нижче). Значення РАСО2 Є середнім для газу з різних альвеол, пропорційним до їхньої вентиляції, без урахування перфузованості. Він є протилежним до РаСО2, який урівноважений тільки з перфузованими альвеолами і, отже, в осіб з неперфузованими альвеолами більший, ніж РАСО2.
Хоча можна перебувати під водою і дихати за допомогою трубки, виведеної над поверхнею води, та зазначимо, що трубка впливає на збільшення об’єму мертвого простору. З кожним мілілітром об’єму трубки глибина вдихання буде збільшуватись на 1 мл для забезпечення однакового об’єму повітря в альвеолах. Отже, якщо об’єм трубки буде великим, то дихання може стати занадто обтяженим. Крім того, потрібні додаткові зусилля проти тиску навколишньої води для розтягнення (збільшення об’єму) грудної клітки.