Фізіологія людини - Вільям Ф. Ґанонґ 2002
Фізіологія нервових і м'язових клітин
Синаптичне і контактне передавання
Синаптичне передавання - Хімічний характер синаптичної активності
Значення
Факт, що провідність у більшості синапсів є хімічною, має важливе фізіологічне і фармакологічне значення. Нервові закінчення назвали біологічними перетворювачами, оскільки вони перетворюють електричну енергію у хімічну. В загальних рисах цей процес охоплює синтез трансмітерів, їхнє накопичення в синаптичних пухирцях і виділення під впливом нервових імпульсів у синаптичну щілину. Далі трансмітери діють на відповідні рецептори мембрани постсинаптичної клітини і швидко виходять з синаптичної щілини шляхом дифузії, метаболізму або, у багатьох випадках, унаслідок зворотного поглинання пресинаптичним нейроном. Усі ці процеси, а також післярецепторні явища в постсинаптичному нейроні, регульовані багатьма фізіологічними факторами і, принаймні теоретично, їх можна змінити за допомогою фармакологічних засобів. Отже, фармакологи можуть створювати засоби, що не тільки регулюють сомато- і вісцеромоторні функції, а й здатні впливати на емоції, поведінку та всі інші складні функції головного мозку.
Хімічний склад трансмітерів
У випадку, коли деяка сполука нерівномірно розподілена в нервовій системі, і цей розподіл відповідає розподілу її рецепторів, а також ензимів, що синтезують і катаболізують цю речовину, то можна передбачати, що ця сполука є трансмітером. Додатковим доказом слугує те, що сполука виділяється у відповідних ділянках головного мозку і що вона впливає на певні окремі нейрони у разі нанесення на їхні мембрани за допомогою мікропіпетки (мікройонофорез). Багато трансмітерів, а також ензимів, що беруть участь у їхньому синтезі і катаболізмі, ідентифіковано в нервових закінченнях головного мозку і різних інших тканинах за допомогою імуноцитохімічних методів з використанням значених антитіл. Антитіла специфічно зв’язуються з певною речовиною, і локалізацію цієї речовини визначають за позначкою методами світлової або електронної мікроскопії. Гістохімічна гібридизація in situ, яка дає змогу виявляти мРНК, що беруть участь у синтезі певних ензимів або рецепторів, теж є важливим методом дослідження.
Виявлені нейротрансмітери за хімічною структурою можна розділити на головні класи, або родини: аміни, амінокислоти, поліпептиди. Деякі становлять пурини, a NO та СО (див. нижче) - гази. Окрім того, трансмітери можуть бути похідними арахідонової кислоти. Зазначимо, що більшість цих речовин не тільки виділяються в синаптичні щілини, де чинять суто місцевий вплив. В інших умовах вони дифундують у ПКР, навколо синапсу, впливають на певній відстані від місця їхнього виділення (паракринний зв’язок; див. Розділ 1). В окремих випадках їх теж виділяють нейрони в кров’яне русло, як гормони. Дещо довільна компіляція більшості відомих або ймовірних синаптичних трансмітерів і нейромодуляторів наведена в табл. 4-1.
Рецептори
Клонування й інші відповідні сучасні молекулярно-біологічні методи дослідження дали змогу зробити важливі відкриття стосовно структури і функції рецепторів нервових трансмітерів та інших хімічних посередників. Окремі рецептори разом з лігандами описано далі в цьому розділі. Проте виникають п’ять питань, які треба з’ясувати передусім.
По-перше, детальне дослідження на сучасному рівні допомогло виявити, що для кожного ліганда є багато підтипів рецепторів. Наприклад, норадреналін діє на а1- і а2 - рецептори, і ще клоновано по три їхні підтипи. Крім того, Є ß1-, ß2- і ß3 -рецептори. Очевидно, це помножує і робить вибірковішим можливі впливи в певній клітині конкретного ліганду.
По-друге, у багатьох трансмітерів рецептори розміщені як у постсинаптичній, так і в пресинаптичній частинах. Такі пресинаптичні рецептори, або авторецептори, часто гальмують подальшу секрецію ліганду, забезпечуючи регулювання шляхом зворотного зв’язку. Наприклад, норадреналін діє на пресинаптичний а2 - рецептор, гальмуючи секрецію норадреналіну. Проте авторецептори можуть теж збуджувати виділення нервових трансмітерів.
По-третє, незважаючи на те, що лігандів і підтипів рецепторів для кожного з них багато, рецептори можна об’єднувати у великі родини відповідно до їхньої функції і структури. Багато з них є серпентиновими рецепторами, що діють через G-білки і протеїнкінази (див. Розділ 1), інші - йонними каналами. Об’єднані в групи рецептори визначених нервових трансмітерів наведені в табл. 4-2. Зазначимо, однак, що таблиця дуже спрощена. Наприклад, активування а2 -рецепторів зумовлює зменшення внутрішньоклітинної концентрації цАМФ, утім, вірогідно, що G-білки, активовані пресинаптичними а2 -рецепторами, безпосередньо діють на Са2+-канали, зумовлюючи гальмування виділення норадреналіну шляхом зменшення надходження Са2+.
По-четверте, рецептори концентруються в постсинаптичних структурах поблизу закінчень нейронів, які продукують специфічні для них нейротрансмітери. Це головно зумовлене наявністю специфічно зв’язувальних білків. Для нікотиноподібних ацетилхолінових рецепторів нервово-м’язового закінчення таким білком є рапсин, а для глютамінергічних рецепторів цю функцію виконують представники родини РВ2-зв’язувальних білків. ГАМКА-рецептори зв’язані з білком гефірином, що теж зв’язує і гліцинові рецептори. ГАМКС -рецептори зв’язані з цитоскелетом сітківки за допомогою білка МАР-1В.
По-п’яте, тривале зв’язування з лігандом робить більшість рецепторів несприйнятливими, тобто настає десенсибілізація. Є два типи десенсибілізації: гомологічна десенсибілізація, що супроводжується втратою сприйнятливості стосовно якогось певного ліганду і збереженням чутливості клітини до інших лігандів, і гетерологічна десенсибілізація, за якої клітина стає несприйнятливою до всіх лігандів. Десенсибілізація, що виникає в ß-адренергічних рецепторах, вивчена особливо детально. У разі однієї з форм такої десенсибілізації відбувається фосфорилювання карбоксильної кінцевої ділянки рецептора специфічною кіназою ß-адренергічного рецептора (ß-ARK) за участю іншого білка - ß-арестину. Бета-арестин зв’язується теж з клатрином - речовиною, що активує рецептор-залежний ендоцитоз. Крім того, десенсибілізація ß-адренергічного рецептора може відбуватися шляхом фосфорилювання в карбоксильній кінцевій ділянці за допомогою РКА (див. Розділ 1). Інтерналізація ß-адренергічних рецепторів веде до посилення деградації мРНК рецептора, унаслідок чого кількість рецепторів зменшується (регулювання пригнічення).
Зворотне поглинання
Останніми роками з’ясовано, що відбувається зворотне поглинання більшості, а можливо, і всіх, амінових та амінокислотних нейротрансмітерів з синаптичної щілини до цитоплазми пресинаптичного нейрона (рис. 4-15), тобто нейрона, в якому ці речовини продукуються. Високоафінні системи поглинання формують дві родини транспортних білків. Одна родина має 12 трансмембранних доменів і переносить трансмітер разом з Na+ і Сl-. До членів цієї родини належать транспортери норадреналіну, дофаміну, серотоніну, ГАМК, гліцину, а також проліну, таурину і попередника ацетилхоліну - холіну. Крім того, сюди ж належить і транспортер адреналіну. Інша родина складається принаймні з трьох транспортерів, що опосередковують поглинання глютамату. Ці транспортери зв’язані з котранспортуванням Na+ і К+, проте вони незалежні від транспортування Сl-. Дискусія стосовно їхньої структури триває: очевидно, вони мають 6, 8 або 10 трансмембранних доменів. Один з цих транспортерів швидше за все переносить глютамат у клітини глії, а не в нейрони (див. Розділ 2).
Крім того, є два пухирцеві моноамінові транспортери: VMAT1 і VMAT2. Хоча вони кодовані різними генами, їм властива значна гомологічність: обидва мають широку специфічність, переносячи дофамін, норадреналін, адреналін, серотонін і гістамін з цитоплазми до секреторних гранул. Обидвох їх гальмує резерпін, що пояснює стан значного виснаження пулу моноамінів, який виникає в разі застосування цього засобу. Як і члени родини мембранних транспортерів нейротрансмітерів, вони мають 12 трансмембранних доменів, проте їхня гомологія з мембранними транспортерами незначна. Є теж пухирцевий транспортер ГАМК (VGAT), що переносить ГАМК та гліцин усередину пухирців, і пухирцевий транспортер ацетилхоліну (див. нижче). Зворотне поглинання є важливим фактором часового регулювання дії нервових трансмітерів. У разі інгібування цього процесу ефект виділення трансмітера посилюється і стає тривалішим. Це має клінічне значення. Наприклад, численні ефективні антидепресанти власне є інгібіторами процесу зворотного поглинання амінових нейротрансмі терів. Уважають, що кокаїн інгібує зворотне поглинання дофаміну. Регулювання поглинань глютамату нейронами і клітинами глії теж важливе, оскільки глютамат є збуджувальним токсином, що здатний убивати клітини шляхом їхнього надмірного подразнення (див. нижче). Вірогідно, що під час ішемії й аноксії втрата кількості нейронів збільшується, оскільки відбувається інгібування зворотного поглинання глютамату.
Таблиця 4-1. Нейротрансмітери і нейромодулятори нервової системи ссавців1
Речовина |
Місце розташування |
Ацетилхолін |
М’язово-нервове закінчення, прегангліонарні автономні закінчення, постгангліонарні симпатичні закінчення потових залоз і м’язів-вазодилятаторів; багато відділів головного мозку; закінчення деяких амакринових клітин сітківки |
Аміни Дофамін |
SIF клітини симпатичних вузлів; смугасте тіло; серединне підвищення й інші частини гіпоталамуса; лімбічна система; частини нової кори; закінчення деяких інтернейронів сітківки |
Норадреналін |
Більшість постгангліонарних симпатичних закінчень; кора великого мозку; гіпоталамус, стовбур головного мозку, мозочок, спинний мозок |
Адреналін |
Гіпоталамус, таламус, навколоводопровідна сіра речовина, спинний мозок |
Серотонін |
Гіпоталамус, лімбічна система, мозочок, спинний мозок; сітківка |
Гістамін |
Гіпоталамус, інші частини головного мозку |
Збуджувальні амінокислоти Глютамат |
Кора великого мозку, стовбур головного мозку |
Аспартат |
Зорова кора |
Гальмівні амінокислоти Гліцин |
Нейрони, що опосередковують пряме гальмування в спинному мозку, стовбур головного мозку, передній мозок; сітківка |
Гамма-аміномасляна кислота (ГАМК) |
Мозочок; кора великого мозку; нейрони, що опосередковують пресинаптичне гальмування; сітківка |
Поліпептиди Речовина Р, інші тахікіни |
Закінчення первинних аферентних нейронів, що опосередковують передавання відчуття болю; багато частин головного мозку; сітківка |
Вазопресин |
Задня частка гіпофіза; довгастий мозок; спинний мозок |
Окситоцин |
Задня частка гіпофіза; довгастий мозок; спинний мозок |
КРГ |
Серединне підвищення гіпоталамуса; інші частини головного мозку |
ТРГ |
Серединне підвищення гіпоталамуса; інші частини головного мозку; сітківка |
СРГ |
Серединне підвищення гіпоталамуса |
Соматостатин |
Серединне підвищення гіпоталамуса; інші частини головного мозку; драглиста речовина, сітківка |
ГнРГ |
Серединне підвищення гіпоталамуса; навколошлуночкові органи; прегангліонарні автономні закінчення; сітківка |
Ендотеліни |
Задня частка гіпофіза; стовбур головного мозку |
Енкефаліни |
Драглиста речовина; багато інших частин ЦНС; сітківка |
Бета-ендорфін, інші похідні проопіомеланокортину |
Гіпоталамус, таламус, стовбур головного мозку; сітківка |
Ендоморфіни |
Таламус, гіпоталамус, смугасте тіло |
Динорфіни |
Навколоводопровідна сіра речовина, передньовентральна ділянка довгастого мозку, драглиста речовина |
Холецистокінін (ССК-4 і ССК-8) |
Кора великого мозку, гіпоталамус; сітківка |
Вазоактивні кишкові пептиди |
Постгангліонарні холінергічні нейрони; деякі чутливі нейрони; гіпоталамус; кора великого мозку; сітківка |
Нейротензин |
Гіпоталамус; сітківка |
Гастрин-рилізинг пептид |
Гіпоталамус |
Гастрин |
Гіпоталамус; довгастий мозок |
Глюкагон |
Гіпоталамус; сітківка |
Мотилін |
Нейрогіпофіз; кора великого мозку, мозочок |
Секретин |
Гіпоталамус, таламус, нюхова цибулина, стовбур головного мозку, кора великого мозку, перемичка, морський коник, смугасте тіло |
Кальцитонін ген-зв’язаний пептид-а |
Закінчення первинних аферентних нейронів; шляхи смаку; чутливі нерви; медіальний пучок переднього мозку |
Таблиця 4-1. Закінчення
Речовина |
Місце розташування |
Нейропептид У |
Норадренергічні, адренергічні й інші нейрони довгастого мозку, навколоводопровідна сіра речовина, гіпоталамус, автономна нервова система |
Активіни |
Стовбур головного мозку |
Інгібіни |
Стовбур головного мозку |
Ангіотензин II |
Гіпоталамус, мигдалеподібне тіло, стовбур головного мозку, спинний мозок |
FMRF амід |
Гіпоталамус, стовбур головного мозку |
Галанін |
Гіпоталамус, морський коник, середній мозок, спинний мозок |
Передсердний натрійуретичний пептид |
Гіпоталамус, стовбур головного мозку |
Пурини Аденозин |
Нова кора, нюхова кора, морський коник, мозочок |
АТФ |
Автономні вузли, повідці |
Гази |
|
NО, СО |
ЦНС |
Ліпіди Анандамід |
Морський коник, базальні ядра, мозочок |
1 Трансмітерна функція деяких поліпептидів не доведена.
Таблиця 4-2. Механізм дії вибраних нейротрансмітерів
Трасмітер |
Рецептор |
Вторинний месенджер |
Загальний вплив на канали |
Ацетилхолін |
Нікотиноподібний |
... |
↑ Na, інші малі йони |
М1, |
↑ІФ3, ДАГ |
↑ Са2+ |
|
М2 (серцевий) |
↓ Циклічна АМФ |
↑ К+ |
|
М3 |
↓ Циклічна АМФ |
||
М4 (залозистий) |
↑ ІФ3, ДАГ |
||
М6 |
↑ ІФ3, ДАГ |
||
Дофамін |
D1, D5 |
↑ Циклічна АМФ |
|
D2 |
↓ Циклічна АМФ |
↑ К+, ↓ Са2+ |
|
D3, D4 |
↓ Циклічна АМФ |
||
Норадреналін |
а1А, а1В, a1D |
↑ ІР3, ДАГ |
↓ K+ |
а2А, а2В, а2С |
↓ Циклічна АМФ |
↑ K+, 4 Ca2+ |
|
ß1 |
↑ Циклічна АМФ |
||
ß2 |
↑ Циклічна АМФ |
||
ß3 |
↑ Циклічна АМФ |
||
5НТ |
5НТ1A |
↓ Циклічна АМФ |
↑ K+ |
5НТ1В |
↓ Циклічна АМФ |
||
5HT1D |
↓ Циклічна АМФ |
↓ К+ |
|
5НТ2A |
↑ ІФ3, ДАГ |
↓ К+ |
|
5НТ2С |
↑ ІФ3, ДАГ |
||
5НТ3 |
. |
↑Na+ |
|
5НТ4 |
↑ Циклічна АМФ |
||
Аденозин |
А1 |
↓ Циклічна АМФ |
|
A2 |
↑ Циклічна АМФ |
||
Глютамат |
Метаботропний2 |
||
Іонотропний |
|||
АМПА, каїнатний |
... |
↑ Na+ |
|
NMDA |
... |
↑ K+, Ca2+ |
|
ГАМК |
ГАМКA |
... |
↑Cl- |
ГАМКВ |
↑ ІФ3, ДАГ |
↑ K+, ↓ Ca2+ |
1 Рецептори 5НТ1Е, 5HT1F, 5НТ2В, 5НТ5А, 5НТ5В, 5НТ6 та 5НТ7 теж клоновані.
2 Ідентифіковано одинадцять підтипів; усі вони зменшують концентрацію цАМФ або збільшують концентрацію ІФ3 (інозитол-3-фосфат) і ДАГ (діацилгліцерол), за винятком одного, що підвищує концентрацію цАМФ.
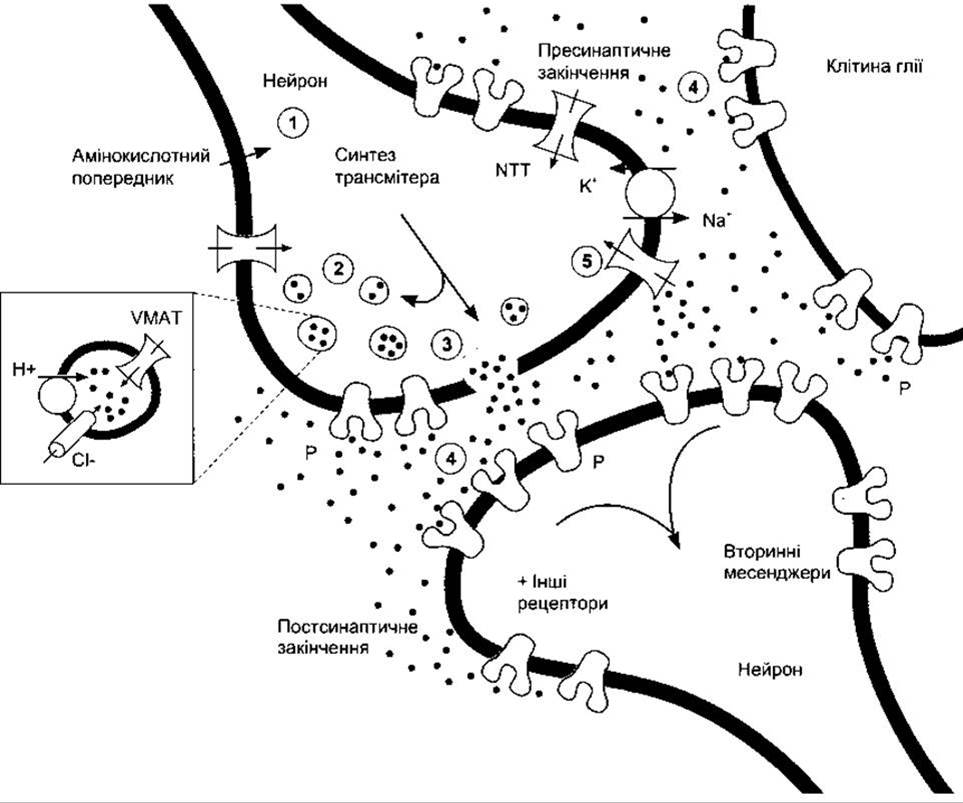
Рис. 4-15. Перетворення моноамінів, що продукуються в синаптичному контакті. У кожному нейроні, який продукує моноаміни, ці речовини синтезуються в цитоплазмі і секреторних ґранулах (1); концентрація моноамінів у ґранулах є сталою (2) завдяки двом пухирцевим моноаміновим транспортерам (VMAT). Моноамін виділяється шляхом екзоцитозу ґранул (3) і діє на рецептори (4) (Y-подібні структури, позначені як Р). Велика кількість рецепторів постсинаптичні, проте деякі пресинаптичні, а інші розміщені на клітинах глії. Врешті відбувається активне поглинання моноаміну до цитоплазми пресинаптичного нейрона (5) за допомогою моноамінового транспортера (NTT) (відтворено за дозволом з Hoffman BJ et al: Distribution of monoamine neurotransmitter transporters in the rat brain. Front Neuroendocrinol 1998; 19:187).