БИОТЕХНОЛОГИЯ РАСТЕНИЙ И БИОБЕЗОПАСНОСТЬ - А. П. Ермишин - 2015
ГЛАВА 2. МЕТОДИЧЕСКИЕ ОСНОВЫ КУЛЬТИВИРОВАНИЯ ОРГАНОВ, ТКАНЕЙ, КЛЕТОК И ПРОТОПЛАСТОВ РАСТЕНИЙ IN VITRO
Для получения культуры клеток in vitro небольшой фрагмент тканей растений (эксплантат) помещают в культуральный сосуд (пробирку, колбу и др.) на искусственную питательную среду, на которой клетки эксплантата начинают делиться, образуя каллюс. Каллюсная культура - наиболее обычный и распространенный вариант культуры клеток растений in vitro. Ее получают из эксплантатов при их культивировании на поверхности полутвердых (чаще всего агаризованных) питательных сред. При культивировании клеток в погруженном состоянии в жидких питательных средах получают суспензии клеток растений (суспензионные культуры). Использование ферментных растворов, растворяющих клеточные стенки, дает возможность получить протопласты - клетки растений, лишенные целлюлозной оболочки. Протопласты можно культивировать на жидких питательных средах или высевать суспензию протопластов на поверхность агаризованной питательной среды. Со временем протопласты восстанавливают клеточную стенку и переходят к делению, образуя каллюсную ткань. При определенных условиях каллюсные культуры, суспензии клеток способны к морфогенезу и/или соматическому эмбриогенезу, что дает возможность получать растения-регенеранты. Растения-регенеранты также могут быть получены непосредственно из эксплантатов. Их можно выращивать длительное время и размножать в культуре in vitro(культура пробирочных растений).
Работы по получению и поддержанию всех названных или отдельных видов культуры органов, тканей, клеток и протопластов растений (далее - культуры клеток растений) требуют специальных помещений, оборудования, инструментов, предполагают использование сложных питательных сред. Помещения, инструменты, лабораторная посуда и питательные среды подвергаются стерилизации с помощью различных методов. Многие работы проводятся с соблюдением правил асептики.
2.1. Помещения, оборудование и инструменты для работ с культурой клеток растений
Для проведения работ с культурой клеток растений требуются лабораторные комнаты: для мытья и стерилизации посуды и инструментов; приготовления и стерилизации питательных сред; цитологических исследований; получения, пассирования и других манипуляций с клеточными культурами; культивирования клеток растений, а также боксовая или грунтовая теплица с искусственным освещением.
В комнате для мытья посуды, как правило, имеется аквадистиллятор (аквабидистиллятор). Дистиллированная вода необходима для приготовления питательных сред, полоскания вымытой посуды, эксплантатов после их обработки стерилизующими агентами. Вымытую посуду просушивают в суховоздушном шкафу при 80-100 °С. Высокая температура также обеспечивает ее стерилизацию.
Для работ по культуре клеток растений используют: посуду стеклянную химическую различного типа и объема для приготовления питательных сред, и хранения запасных растворов, получения и манипуляций с культурами (вычленения и стерилизации эксплантатов, пассирования культур, черенкования пробирочных растений и др.); для культивирования: колбы, стаканы, чашки Петри, пробирки, мензурки, мерные цилиндры, пипетки. В последнее время широкое применение нашла разнообразная пластиковая посуда для культуры клеток растений разового использования. Однако во многих случаях удобнее и дешевле использовать стеклянную посуду.
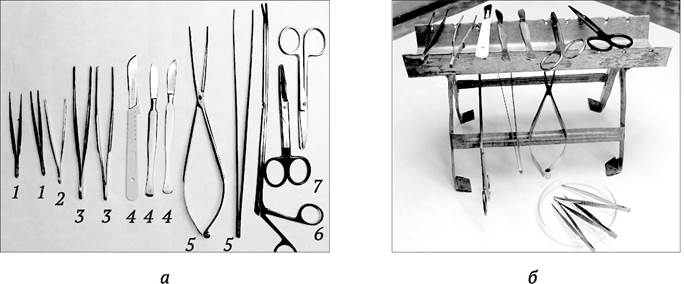
В комнате для мытья посуды нередко размещают автоклавы, которые необходимы для стерилизации питательных сред и посуды, а также отдельный суховоздушный шкаф для стерилизации инструмента. Инструменты стерилизуют при 160 °С в течение 4 ч, помещая их в металлические пеналы. Минимальный набор инструментов включает в себя: пинцеты разной длины с тупыми и острыми концами, скальпели, ножницы и щипцы медицинские (рис. 2.1, а). В процессе работы инструменты размещают на специальном штативе или стерилизованных чашках Петри, после каждой операции их погружают в 96 % спирт и прожигают в пламени спиртовки, затем охлаждают (рис. 2.1, б).
Рис. 2.1. Набор инструментов для работы с культурой клеток растений: а - набор инструментов: 1 - пинцет глазной (офтальмологический) 5-7 см с острыми концами; 2 - пинцет короткий (5-7 см) с тупыми концами; 3 - пинцеты длиной 10-14 см; 4 - скальпели хирургические; 5 - длинный пинцет; 6 - щипцы уретральные; 7 - ножницы; б - инструменты на штативе и стеклянной чашке Петри в процессе работы в ламинар-боксе
В комнате для приготовления питательных сред должны быть различные весы, лабораторный рН-метр, электроплита и водяная баня для приготовления агаризованных питательных сред (для небольших объемов можно использовать микроволновую печь), холодильник, морозильник, магнитная мешалка, вытяжной шкаф. В этой же комнате или отдельном помещении могут располагаться микроскопы (обычные и/или инвертированные), бинокулярные лупы, счетчики клеток и другое оборудование и инструменты, необходимые для цитологических исследований, манипуляций с протопластами.
Все работы, непосредственно связанные с культурой клеток растений (вычленение и стерилизация эксплантатов, пассирование культур, черенкование пробирочных растений и др.), проводят в ламинар-боксах, которые размещают в отдельном помещении или в комнате для приготовления питательных сред и проведения цитологических исследований (рис. 2.2). Ламинар-бокс (камера обеспыливания) представляет собой стол с поверхностью из нержавеющей стали, изолированный от окружающей среды сверху, сзади, слева и справа. В рабочее пространство ламинар-бокса (над столом) поступает под давлением стерильный воздух, что обеспечивает условия асептики, необходимые для работ по культуре клеток растений. Воздух засасывается в ламинар-бокс из помещения с помощью специального насоса и пропускается через фильтры грубой и тонкой очистки, которые задерживают не только частицы пыли, но и клетки микроорганизмов. Различают ламинар-боксы горизонтальные и вертикальные (в зависимости от направления движения стерильного воздуха в рабочем пространстве), в равной степени эффективные. Перед началом работы поверхность стола ламинар-бокса обеззараживают с помощью бактерицидной УФ-лампы, встроенной над поверхностью стола (в течение 30-60 мин), затем стол протирают 70 % раствором этилового спирта.
Рис. 2.2. Работы по культуре клеток растений в ламинар-боксе

В качестве культуральной комнаты обычно используют изолированное помещение, оборудованное кондиционером. В нем размещают термостаты (культивирование клеток растений в темноте). Однако во многих случаях при культивировании клеток растений требуется освещение. Для этого в простейшем случае в культуральной комнате размещают стеллажи с лампами дневного света (рис. 2.3, а). Лампы могут располагаться сверху над полками или по центру между двумя полками (культуры освещаются в этом случае в основном сбоку). Лампы включаются и выключаются автоматически в определенное время. Для культивирования клеток растений могут использоваться также различные климатические камеры с регулируемым режимом освещения, температуры и влажности (рис. 2.3, б).
Рис. 2.3. Установка для культивирования клеток растений на свету: а - стеллаж с верхним освещением культуры in vitro люминесцентными лампами; б - выращивание культуры in vitro в климатической камере с боковым освещением люминесцентными лампами специального спектрального состава

Для работ по культуре клеток растений необходима боксовая или грунтовая теплица с искусственным освещением. Во-первых, в ней могут выращиваться растения, с которых берут эксплантаты. Эксплантаты, полученные с таких растений, как правило, менее инфицированы, чем с растений, выращиваемых в поле. Кроме того, успех культивирования клеток растений и получения растений-регенерантов в некоторых случаях в значительной степени зависит от условий выращивания (температура, режим и способ освещения) растений-доноров эксплантатов (например, при получении гаплоидов в культуре пыльников). Во-вторых, теплица необходима для высадки в грунт полученных растений-регенерантов, так как их перенос в условия in vivo из пробирок требует специальной адаптации.
2.2. Питательные среды
В процессе развития методов культуры клеток растений происходило постоянное совершенствование питательных сред. В настоящее время существует большое количество питательных сред для разных задач культивирования, видов растений и типов эксплантатов. Основываясь на данных литературы, можно подобрать приемлемый вариант практически для любого вида работ. В отдельных случаях требуется оптимизация питательной среды. Для этих целей разработаны специальные подходы, в том числе основанные на использовании методов математического планирования эксперимента. Варьируя, по определенной схеме, концентрации отдельных компонентов питательной среды (прежде всего регуляторов роста), находят оптимальный вариант.
Существует ряд базовых питательных сред, которые берут за основу, а затем производят, если требуется, их оптимизацию. Наиболее часто используется среда Мурасиге и Скуга (1962). Она хорошо сбалансирована по входящим в нее компонентам и дает хорошие результаты при культивировании клеток многих видов растений (см. таблицу). Среда B-5 Гамборга (1968) больше подходит для злаковых культур, среда Nitsch (1969) - для культуры пыльников двудольных растений. Однако различные питательные среды для культуры клеток растений имеют много общего. Они должны включать все необходимые минеральные и органические элементы в концентрациях, максимально приближенных к тем, которые получают интактные растения для нормального роста и развития в условиях in vivo.
Состав некоторых питательных сред для культуры клеток растений in vitro
Компоненты |
Питательные среды (содержание компонентов, мг/л) |
|||
MS* |
ER* |
B-5* |
Nitcsh* |
|
Макроэлементы |
||||
NH4 NO3 |
1650 |
1200 |
- |
720 |
KNO3 |
1900 |
1900 |
2500 |
950 |
CaCl2 • 2H2O |
440 |
440 |
150 |
- |
CaCl2 |
- |
- |
- |
166 |
MgSO4 • 7H2O |
370 |
370 |
250 |
185 |
kH2PO4 |
170 |
340 |
- |
68 |
(NH4)2SO4 |
- |
- |
134 |
- |
NaH2PO4 • H2O |
- |
- |
150 |
- |
Микроэлементы |
||||
KI |
0,83 |
- |
0,75 |
- |
H3BO3 |
6,20 |
0,63 |
3,00 |
10 |
MnSO4 • 4H2O |
22,30 |
2,23 |
- |
25 |
MnSO4 • H2O |
- |
- |
10,00 |
- |
ZnSO4 • 4H2O |
6,80 |
- |
- |
- |
ZnSO4 • 7H2O |
- |
- |
2,00 |
10 |
ZnNa2 EDTA |
- |
15,0 |
- |
- |
Na2MoO4 • 2H2O |
0,25 |
0,025 |
0,25 |
0,25 |
CuSO4•5H2O |
0,025 |
0,0025 |
0,025 |
0,025 |
CoCl2 • 6H2O |
0,025 |
0,0025 |
0,025 |
- |
Na2 EDTA • 2H2O |
37,30 |
37,30 |
37,30 |
37,30 |
FeSO4 • 7H2O |
27,80 |
27,80 |
27,80 |
27,80 |
Витаминные и гормональные добавки** |
||||
Миоинозит |
100 |
- |
100 |
100 |
Никотиновая кислота |
0,5 |
0,5 |
1,0 |
5,0 |
Пиридоксин НСl |
0,5 |
0,5 |
1,0 |
0,5 |
Тиамин НСl |
0,1 |
0,5 |
10,0 |
0,5 |
Фолиевая кислота |
0,5 |
|||
Биотин |
0,05 |
|||
Глицин |
2,0 |
2,0 |
- |
2,0 |
β-Индолил уксусная кислота (ИУК) |
1,0-30,0 |
- |
- |
0,1 |
α-Нафтил уксусная кислота (НУК) |
- |
1,0 |
- |
- |
2,4-дихлорфеноксиуксусная кислота (2,4D) |
- |
- |
0,1-1,0 |
- |
Кинетин |
0,04-10,0 |
0,02 |
0,1 |
- |
Сахароза |
30 000 |
40 000 |
20 000 |
20 000 |
рН Среды |
5,7 |
5,8 |
5,5 |
5,5 |
Агар-Агар |
7000*** |
7000*** |
7000*** |
8000*** |
* MS: T. Murashige, F. Skoog. A revised medium for rapid growth and bioassays with tobacco tissue cultures // Physiol.Plant. 1962. Vol. 15. P. 473-497.
ER: T. Eriksson. Studies on the growth requirements and growth measurements of cell culture of Haplopappus gracilis. Physiol. Plant. 1965. Vol. 18. P. 976-983.
B-5: O. L. Gamborg, R. A. Miller, K. Ojima. Nutrient requirements of suspension cultures of soybean root cells // Exp. Cell Res. 1968. Vol. 50. P. 151-158.
Nitsch: J. P. Nitsch, C. Nitsch. Haploid plants from pollen grains // Science. 1969. Vol. 163. P.85-87.
** Состав и количество витаминных и гормональных добавок могут варьировать в зависимости от целей эксперимента, эксплантата, вида растений и др. (данный состав представлен в соответствии с оригинальными прописями авторов).
*** Для получения среды нормальной консистенции достаточно 6000 мг/л агар-агара.
Минеральные элементы. Для обеспечения полноценного метаболизма клеток в культуре in vitro в питательных средах должен присутствовать ряд макро- и микроэлементов неорганического происхождения. В соответствии с рекомендациями Международной ассоциации физиологов растений те элементы минерального питания растений, которые требуются в концентрациях, превышающих 0,5 mМ, относят к макроэлементам, а те, что необходимы в более низких концентрациях, - к микроэлементам. Основные макроэлементы питательных сред для культуры клеток растений: азот, калий, фосфор, кальций, магний и сера. Они представлены в питательных средах в виде соответствующих солей, которые хорошо усваиваются растительными клетками. Важно отметить, что азот присутствует в питательных средах в нитратной и аммонийной форме. Их соотношение во многих случаях имеет большое значение. В качестве дополнительного источника азота в состав сред в некоторых случаях добавляют аминокислоты (аланин, глутаминовую кислоту, глицин, аргинин, аспарагиновую кислоту, пролин и др.). Иногда смесь аминокислот заменяют гидролизатом казеина.
Основные микроэлементы питательных сред: железо (двухвалентное), марганец, бор, медь, цинк, йод, молибден, кобальт. Наиболее важными микроэлементами являются железо и медь, потому что они участвуют в регуляторных процессах и окислительно-восстановительных превращениях, входят в состав коферментов. Железо используется в виде хелатов [FeSO4 + ЭДТА (этилендиаминтетрауксусная кислота или ее динатриевая соль Na2 ЭДТА, трилон Б)].
Углеводы являются необходимым компонентом питательных сред для культуры клеток растений, так как в большинстве случаев последние не способны к автотрофному питанию. При изолировании эксплантатов из хлорофиллоносных тканей и помещении их на питательную среду они, как правило, теряют хлорофилл. При культивировании на свету одни культуры остаются лишенными хлорофилла, другие - зеленеют, но не способны обеспечивать себя полностью углеводами за счет фотосинтеза. Кроме того, углеводы в питательной среде выполняют осмотические функции, особенно в случае культуры протопластов.
Чаще всего углеводным компонентом в составе питательных сред для культуры клеток растений является сахароза в концентрации 2-3 %. Для культуры пыльников применяют более высокие концентрации - 6-10 %. Помимо сахарозы в качестве источника углеродного питания берут глюкозу, фруктозу, галактозу, мальтозу и др. Основной осмотик для культуры протопластов - маннитол (13 %). Также применяют для этих целей сорбитол, глюкозу, сахарозу, сочетание различных сахаров.
Витамины относятся к веществам, играющим существенную роль в культуре клеток растений. Большая часть витаминов входит в состав ферментов, катализирующих метаболически важные реакции. В состав питательных сред чаще всего включают водорастворимые витамины: тиамин, пиридоксин, никотиновую кислоту, а также рибофлавин, биотин, пантотеновую кислоту, аскорбиновую кислоту. Во многих питательных средах для культуры клеток растений присутствует миоинозит (мезоинозит), который в растениях участвует в обмене ауксина. В культуре клеток мезоинозит играет важную роль в биосинтезе пектина и гемицеллюлозы, участвует в утилизации ионов.
Действие витаминов на рост культуры клеток зависит от способности клеток синтезировать их в оптимальном или субоптимальном количестве и от состава других компонентов питательной смеси, с которыми витамины могут взаимодействовать синергически (например, с цитокининами) или антагонистически. При внесении полной смеси витаминов стимулирующее действие может определяться синергизмом между отдельными витаминами.
Фитогормоны и регуляторы роста и развития растений. Фитогормоны - синтезируемые растениями органические соединения, которые оказывают влияние на их рост и развитие. Кроме натуральных фитогормонов, выделенных из растений, имеется достаточно большое количество искусственных соединений, которые обладают аналогичным действием. Их называют регуляторами роста и развития растений (далее - регуляторы роста). В питательные среды в основном добавляют регуляторы роста, поскольку они более дешевые, более стойкие и во многих случаях их активность выше, чем у фитогормонов.
Чаще всего в питательных средах присутствуют различные ауксины и цитокинины. Для определенных целей также используют гиббереляины, абсцизины, этилен, ретарданты.
Природный ауксин в растениях встречается в основном в виде р-индолил- 3-уксусной кислоты (гетероауксина) (ИУК). Второй представитель этого класса фитогормонов - фенилуксусная кислота (ФУК), однако ее активность значительно ниже ИУК. Ауксины - это производные аминокислот: ИУК - триптофана, ФУК - фенилаланина. Ауксины в растениях играют важную роль в процессах удлинения стебля, междоузлий, тропизма, апикального доминирования, образования придаточных и боковых корней, луковиц, заложения вегетативных почек и др. В культуре клеток ауксины - обязательные компоненты, необходимые для инициации процессов морфогенеза. Они оказывают влияние на деление, растяжение и дифференциацию клеток.
Избыток ауксина в растениях разрушается ИУК-оксидазой. Для практических целей в сельском хозяйстве, а также для культуры клеток растений часто применяют не ИУК, а синтетические ауксины, так как они не разрушаются ИУК-оксидазой. Молекулы синтетических ауксинов имеют разную структуру, но содержат ароматическое или гетероциклическое кольцо, боковая часть которого представлена остатком алифатической кислоты. Чаще всего в питательных средах в качестве ауксина используют 2,4-дихлорфеноксиуксусную кислоту (2,4-Д). Также применяют индолил-3-масляную кислоту (ИМК), α-нафил-1-уксусную кислоту (НУК), фенилуксусную кислоту (ФУК),
2,4,5-трихлорфеноксиуксусную кислоту (2,4,5-Т), n -хлорфеноксиуксусную кислоту (ПХФК), пиклорам (4-амино-3,5,6-трихлорпиколиновая кислота) и т. п. По действию на культуру стебля табака активность 2,4-Д в 8-12 раз, а 2,4,5-Т, ПХФК и пиклорама в 2-4 раза выше, чем у ИУК.
Цитокинины в растениях выполняют функции, связанные с индукцией клеточных делений, модификацией апикального доминирования и дифференциацией стеблей. Они способствуют ветвлению, формированию почек, ускоряют прорастание семян, вызывают прерывание периода покоя спящих почек, семян и клубней. Они являются важнейшим фактором индукции митотической активности клеток в культуре клеток растений, а также в процессах инициации клеточной дифференциации и морфогенеза при взаимодействии с другими фитогормонами.
Цитокинины представляют собой N-замещенные производные аденина и синтезируются в растении из двух главных предшественников - мевалоновой кислоты и 5'-АМФ. Возможен синтез цитокининов из продуктов распада некоторых тРНК, содержащих модифицированный аденозин. Показана высокая кининовая активность и у дифенилмочевины и ряда ее производных. Первый цитокинин, который был использован в питательных средах для культуры клеток растений, - кинетин (N6-фурфуриламинопурин), выделенный из ДНК спермы сельди К. Миллером и Ф. Скугом в 1955 г. Как отмечалось в гл. 1, открытие кинетина имело революционное значение, поскольку дало возможность управлять процессом регенерации растений из каллюсных и суспензионных культур. Позднее были выделены натуральные фитогормоны с кинино- вой активностью - зеатин (6-4гидрокси-3метилтранс-2-бутаниламинопурин) и 6-изопентиламинопурин 2iР, ИПА). В настоящее время основным цитокинином, который используют в питательных средах для культуры клеток, является синтетический регулятор роста 6-бензиламинопурин (6-бензиладенин, 6-БАП). Однако в некоторых случаях незаменимыми являются значительно более дорогостоящие зеатин (или зеатин рибозид) и 2iР.
Гибберелины с точки зрения химического строения - тетрациклические карбоновые кислоты. В растениях они образуются из мевалоновой кислоты, синтезированной из ацетил-КоА. В тканях растений одновременно встречаются несколько гиббереллинов, в процессе онтогенеза их набор и соотношение изменяются. Подобно ауксинам, гиббереллины оказывают множественные действия: стимулируют рост в фазе растяжения и деления клеток (например, камбия), вызывают рост плодов. Рост в фазе растяжения стимулируется одновременно действием гиббереллинов и ауксина. В других случаях гиббереллины могут выступать как антагонисты ауксина, например, задерживать рост придаточных корней. Их используют для прерывания периода покоя семян, луковиц и клубней, усиления роста растений. Подобно ауксинам они способны вызывать партенокарпию (так, их рекомендуют использовать для обработки виноградников в целях увеличения размеров кистей). Известно около 70 гиббереллинов, однако на практике наиболее часто применяют гибберелловую кислоту GA3 (ГК 3), которую получают путем микробиологического синтеза. В питательных средах для культуры клеток растений гиббереллины используют для усиления роста апикальных меристем или недоразвитых зиготических зародышей при получении из них растений-регенерантов, усиления роста суспензионных культур при пониженной их плотности и других целей.
Абсцизовая кислота (АБК) обладает множественным физиологическим действием. Хорошо известно действие АБК как ингибитора роста растений, способствующего переходу растений в состояние покоя. Во многих случаях АБК выступает антагонистом ауксинов, цитокининов и гиббереллинов. В питательных средах для культуры клеток растений АБК иногда применяют в сочетании с другими фитогормонами для обеспечения нормального роста и развития соматических эмбриоидов.
Этилен. Все части растений образуют этилен. Особенно этот процесс усиливается при воздействии стрессовых факторов. В культуре клеток растений этилен может оказывать стимулирующий или ингибирующий эффект (в различных системах) на процессы морфогенеза. Для образования этилена в целях воздействия на растения или культуру клеток растений обычно используют химические вещества, выделяющие этот газ при разрушении, например, 2-хлороэтилфосфоновую кислоту (препараты известны под названиями Этрел, Этафон, Кампозан).
Ретарданты - регуляторы роста различной химической природы, подавляющие рост растений. Их применяют в растениеводстве для уменьшения высоты сельскохозяйственных растений, увеличения толщины стебля, что в результате позволяет уменьшить полегание. В биотехнологии использование ретардантов (хлохолинхлорида, алара и др.) может быть полезным для уменьшения длины междоузлий пробирочных растений. Это позволяет удлинить срок между пересадками растений на свежую питательную среду, а также обеспечивает лучшую приживаемость растений при высадке их в грунт.
Органические добавки неопределенного состава. Клетки растений более чувствительны, чем микроорганизмы, к присутствию посторонних ингредиентов, поэтому требуют химически чистых компонентов среды. Вместе с тем некоторые питательные среды содержат натуральные биологические добавки: жидкий эндосперм кокосового ореха (кокосовое молоко), экстракт эндосперма каштана, гидролизат казеина, солодовый экстракт, томатный сок, дрожжевой экстракт, картофельный отвар и др. Практика использования подобных добавок широко применялась в 30-60-е гг. XX в., когда технологии культивирования клеток и получения растений-регенерантов для большинства видов растений были разработаны недостаточно. Особенно популярным было использование кокосового молока, чей эффект, как выяснилось позднее, был обусловлен присутствием в нем фитогормона зеатина. Однако в последнее время исследователи предпочитают применять компоненты питательных сред определенного состава и высокой степени очистки, что обеспечивает воспроизводимость результатов. Тем не менее иногда удается достичь более высокой результативности морфогенеза в культуре клеток благодаря натуральным биологическим добавкам, например, при использовании картофельного отвара для повышения выхода зеленых гаплоидных растений-регенерантов в культуре пыльников пшеницы.
Адсорбенты. Некоторые эксплантаты выделяют в питательную среду вещества, которые могут ингибировать каллюсообразование и привести к остановке роста и гибели культуры. Для их адсорбции в питательные среды добавляют активированный уголь или другие адсорбенты, например, поливинилпирролидон.
Гелирующие агенты. Каллюсные культуры и пробирочные растения в культуре in vitro выращивают на полутвердых (гелеобразных) питательных средах, которые обеспечивают хороший доступ компонетов питательной среды для клеток или растений и не требуют постоянного перемешивания культур для их аэрации, что является обязательным при использовании жидких питательных сред. Для получения гелеобразных питательных сред в них добавляют гелирующие вещества, которые должны отвечать следующим требованиям: они не должны оказывать неблагоприятного влияния на культивируемые клетки растений; свойства питательной среды, в которую добавлен гелирующий агент, не должны существенно меняться при ее автоклавировании и в процессе культивирования клеток. В горячем состоянии питательная среда должна быть жидкой, а при комнатной температуре (температуре культивирования) - иметь полутвердую (гелеобразную) консистенцию.
Чаще всего в качестве гелирующего агента используют агар-агар (агар), который выделяют из красных водорослей, например, Gelidium amansii. Агар представляет собой смесь полисахаридов, производных галактозы: нейтральной полимерной фракции - агарозы, обеспечивающей силу геля, и заряженных анионных полисахаридов - агаропектинов, влияющих на его вязкость. Качество агара зависит от степени его очистки и может варьировать у разных производителей. Поэтому желательно использовать высокоочищенный агар. Концентрация агара в питательной среде - 0,6-1,0 %. Помимо агара, используют также агарозу (в культуре одиночных клеток, протопластов), гельрит (полисахарид, который получают путем микробного синтеза из Pseudomonas elodea), фитагель и др., состав которых легче поддается контролю.
Большое значение имеет pH питательной среды. Оптимальное значение pH во многом зависит от вида растений, точнее от того, на каких почвах определенные виды растений предпочитают расти в естественных условиях: на кислых, нейтральных или щелочных. Для большинства видов растений pH питательной среды для культуры клеток in vitro 5,5-5,8. Однако эти значения могут быть ниже для растений, произрастающих в естественных условиях на кислых почвах, и выше - для растений, растущих на щелочных почвах.
2.3. Приготовление питательных сред
Питательные среды для культуры клеток растений готовят по прописям из необходимых химических компонентов. Рекомендуется использовать реактивы марки ХЧ (химически чистые) или ОСЧ (особо чистые). Желательно приобретать реактивы марки «Plant Cell Culture Tested» (апробированы для культуры клеток растений). При приготовлении растворов используется дистиллированная или бидистиллированная вода.
Ряд ведущих производителей химических реактивов, например, SIGMA, MERC, SERVA, FLUKA и др., наладили производство готовых питательных сред для культуры клеток растений и отдельных их компонентов (макро-, микроэлементов, витаминов и т. д.). Использование готовых смесей позволяет значительно упростить процесс приготовления питательных сред, повысить их качество.
В прописях питательных сред концентрации минеральных и органических компонентов обычно выражают в единицах массы на объем (мг/л), для чего в англоязычной литературе иногда используют сокращение «ppm» (англ.: 1 part per million). Международной ассоциацией физиологии растений рекомендовано для этих целей использовать молярную концентрацию: молекулярную массу вещества, выраженную в граммах (1 моль - 1М), в миллиграммах (1mM), в микрограммах (1pM), на литр раствора. При этом концентрации макроэлементов и органических добавок предлагается выражать в mМ, а микроэлементов, витаминов, регуляторов роста - в μМ. Таким образом, если в прописи питательной среды написано, что она содержит 1 μМ 2,4-Д, то это означает, что в среде содержится 221 μг/л этого регулятора роста. Для перевода концентрации компонента среды, выраженного в мг/л, в концентрацию, выраженную в mМ, используют следующую формулу: количество mМ = количество мг вещества/молекулярная масса вещества.
При приготовлении питательных сред, особенно из отдельных компонентов, а не из готовых смесей, удобно пользоваться маточными (запасными) концентрированными растворами. Это не только упрощает работу, но и повышает точность дозировки компонентов среды. Обычно готовят следующие запасные растворы: микроэлементы (отдельно раствор йодистого калия), хлористый кальций, витамины, хелат железа, регуляторы роста.
Приготовление отдельных запасных растворов имеет свои особенности. Так, для приготовления 100 мл запасного раствора микроэлементов в мерную колбу наливают 50-60 мл дистиллированной воды, в которую последовательно добавляют предварительно растворенные в небольшом количестве воды соли (в отдельной емкости) в количестве (мг), как они приведены в прописи. Важно соблюдать приведенный в прописи порядок добавления микроэлементов, хорошо их перемешивать. После добавления последнего микроэлемента объем раствора доводят дистиллированной водой.
Для приготовления 100 мл запасного раствора хелата железа берут навески сульфата железа (II) семиводного - 557 мг и Na2ЭДТА - 745 мг. Каждую из навесок растворяют в горячей дистиллированной воде (на водяной бане) объемом 25-30 мл. После полного растворения компонентов растворы смешивают в мерной колбе и доводят объем раствора дистиллированной водой. Раствор должен иметь довольно яркую желтую окраску, слегка опалесцировать. На 1 л питательной среды обычно добавляют 5 мл такого запасного раствора.
При приготовлении запасных растворов регуляторов роста следует учитывать, что фитогормоны, относящиеся к группе ауксинов (2,4-Д, ИУК, НУК, ИМК и др.), а также гиббереллин, являются слабыми органическими кислотами, поэтому их растворение проводят в щелочах. Для их растворения подходит 96 % этиловый спирт. Фитогормоны группы цитокининов (6-БАП, зеатин, кинетин и др.), напротив, растворяют в кислотах. Для этой цели подходит 1 н соляная кислота. Запасные растворы 6-БАП, зеатина и гиббереллина целесообразно делать из расчета 1 мг/1мл. Поскольку при хранении в холодильнике концентрированных растворов некоторых ауксинов происходит их кристаллизация, рекомендуется делать их запасные растворы более разбавленными, а именно 0,1 мг/1 мл (в питательную среду добавляется в десять раз больше запасного раствора соответственно).
Все запасные растворы хранят в холодильнике при 4-5 °С в химической посуде (флаконах или плоскодонных колбах) с плотно закрывающимися крышками. Для хранения раствора йодистого калия используют флакон из темного стекла. Все флаконы должны быть подписаны в соответствии с содержимым, концентрацией (например, 1 мг/1 мл) и указанием даты приготовления раствора. Растворы могут храниться в холодильнике без потери качества до 6 месяцев. При более длительном хранении или появлении инфекции целесообразно приготовить свежий раствор. Растворы зеатина и гиббереллина используются достаточно редко и их следует хранить при -20 °С. Поэтому эти растворы целесообразно аликвотировать в новые стерилизованные автоклавированием пробирки Эппендорф объемом 1,5-2 мл и, упаковав в специально выделенный для них контейнер, хранить в морозильной камере. В таких условиях растворы зеатина и гибереллина могут сохраняться без потери активности более двух лет.
Питательную среду удобно готовить в большом стакане или колбе подходящего объема. Вначале в стакан (колбу) наливают дистиллированную (бидистиллированную) воду на 1/2 требуемого объема, в воду добавляют согласно прописи порошкообразные минеральные компоненты среды (или готовые к применению смеси макро- и микроэлементов), затем компоненты в виде запасных растворов (при использовании готовых смесей макро- и микроэлементов в среду добавляют недостающие элементы согласно прописи). Необходимо добиваться полного растворения каждого вводимого порошкообразного компонента перед введением следующего, для чего можно воспользоваться магнитной мешалкой.
Углеводный компонент вносится последним. Объем раствора доводится до конечного с помощью дистиллированной воды (в мерной колбе). После этого раствор выливают в стакан, в котором доводят рН питательной среды до требуемого значения с помощью 1н NаОН. Растворы щелочи добавляют по каплям в питательную среду, в которую опущены электроды включенного рН-метра. Для перемешивания раствора можно использовать магнитную мешалку. В случае перетитрования раствора среду подкисляют аналогичным образом с помощью 1н соляной кислоты.
Если предполагается использовать полутвердую среду, к ней добавляют навеску агара (или другого гелеобразующего вещества) и тщательно его перемешивают. Растворение агара проводят путем нагревания раствора на водяной бане или при стерилизации среды в автоклаве. Для растворения агара в небольших объемах среды можно использовать микроволновую печь.
Как видно из приведенного выше описания питательных сред, они имеют весьма сложный состав. Использование готовых смесей компонентов среды и запасных растворов позволяет упростить процесс приготовления сред. Тем не менее он требует высокой концентрации внимания работников. Следует также иметь в виду, что в прописях обычно приводятся концентрации отдельных компонентов в расчете на 1 литр конечного объема питательной среды. В реальности нередко приходится готовить и другие объемы. В связи с этим рекомендуется при приготовлении питательной среды использовать так называемый чек-лист, в котором приведены компоненты питательной среды и запасные растворы в порядке их добавления в готовящийся раствор и их количество, которое добавляется в раствор. В процессе приготовления среды после добавки каждого очередного компонента (маточного раствора) в чек-листе делается отметка о добавлении его в раствор. Для каждого конкретного случая (в зависимости от того, какую среду необходимо приготовить и в каком объеме) желательно заранее готовить отдельный чек-лист.
Разлив по культуральным сосудам и стерилизация питательных сред может различаться в зависимости от типа культуры и целей эксперимента. В большинстве случаев для культуры клеток используют стеклянные пробирки, укупоренные изготовленными из ваты пробками, обернутыми марлей. Среды разливают по пробиркам, контейнерам после растворения агара, укупоривают их пробками, затем автоклавируют при 0,8-0,9 атм в течение 20-30 мин.
В последнее время получили распространение для культуры клеток растений пластиковые пробирки с крышками-колпачками или контейнеры разового использования. Соответственно питательную среду в них разливают в асептических условиях (в ламинар-боксе) после автоклавирования. Во многих случаях для культуры клеток используют чашки Петри (стеклянные или разовые пластиковые), в которые также питательную среду разливают после автоклавирования. Наконец, некоторые питательные среды содержат термолабильные компоненты (зеатин, гиббереллин, аскорбиновая кислота и др.), которые разрушаются или теряют активность при автоклавировании. Такие компоненты берут в нужном количестве (из расчета на полный объем приготавливаемой питательной среды). Растворяют их в небольшом количестве дистиллированной воды или взятой из приготовленного объема готовой среды до добавления в нее гелирующего компонента и стерилизуют в асептических условиях путем фильтрации через бактерицидные фильтры (нейлоновые мембраны с микропорами). Добавляют их в проавтоклавированную и охлажденную до 50-60 °С питательную среду. Запасные растворы регуляторов роста, концентрация которых в питательной среде небольшая, можно фильтровать заранее в виде концентрированного раствора и добавлять их в проавтоклавированную питательную среду в соответствии с прописью с помощью автоматических пипеток, снабженных стерильными наконечниками.
2.4. Обеспечение асептики при работе с культурой клеток растений
Как отмечалось выше, культура клеток растений может быть получена и успешно поддерживаться только при условии соблюдения асептики. Это достигается благодаря использованию различных методов стерилизации помещений, лабораторной посуды, инструмента, питательных сред. Особо тщательно стерилизуют поверхность эксплантатов, предназначенных для получения культуры клеток. Все работы, при которых открывают культуральные сосуды (разлив стерильной питательной среды по пробиркам, чашкам Петри, колбам, вычленение эксплантатов и их перенос на питательную среду, перенос части культуры на свежую питательную среду и др.), проводят в стерильных условиях в рабочем пространстве ламинар-бокса с соблюдением правил асептики.
Вся посуда (за исключением пластиковой одноразовой) перед употреблением должна быть стерилизована автоклавированием с последующим подсушиванием в сушильном шкафу или с использованием вакуумной сушки при наличии ее в автоклаве. Перед автоклавированием посуду заворачивают в крафт-бумагу или помещают в биксы, чтобы исключить их повторное заражение при транспортировке. Режим автоклавирования: давление 1,5 атм, время стерилизации 40-60 мин. Подсушивание в сушильном шкафу проводят при температуре около 100 °С в течение 30-40 мин.
Инструменты автоклавировать нельзя, так как они от этого портятся. Их помещают в плотно закрывающийся металлический пенал, в котором они переносятся из одного помещения в другое, и стерилизуют путем прогревания в сушильном шкафу при температуре 160 °С в течение 2-4 ч. При работе в ла- минар-боксе, чтобы избежать контакта инструментов с рабочими поверхностями, инструменты размещают на специальном, термостойком и огнеупорном (металлическом) штативе (рис. 2.1, б). Инструменты в процессе работы (после каждого акта использования) стерилизуют погружением в 96 % этанол и последующим обжиганием в пламени спиртовки (или газовой горелки, если ламинар-бокс ею оборудован). Поскольку горячие инструменты могут повредить растительные ткани, необходимо иметь, как минимум, двойной набор инструментов для проведения одной операции (один набор в работе, второй остывает). В некоторых лабораториях для стерилизации инструмента в ходе работы используют специальные нагреватели, например, инфракрасные.
Перед работой проводится стерилизация ламинар-бокса с помощью встроенных бактерицидных ламп в течение 40-60 мин. За 10-15 мин до окончания обработки ламинар-бокса ультрафиолетом дополнительно включают активную продувку стерильным воздухом. Для этого устанавливают режим продувки ламинар-бокса 80-100 % мощности. После окончания стерилизации выключают бактерицидные лампы, снижают поток воздуха до 40-60 % мощности. Непосредственно перед исследованием рабочие поверхности ламинар-бокса протирают 96 % этанолом. Сотрудник, проводящий работы в ламинар-боксе, должен протирать руки этиловым спиртом в начале работы и периодически в ее процессе.
Стерилизация поверхности растительных тканей перед вычленением эксплантатов и помещением их на питательную среду является одним из наиболее важных этапов получения культуры клеток растений, так как во многих случаях добиться полной их стерильности очень сложно. Успех стерилизации зависит от целого ряда факторов. Как правило, эксплантаты от растений, выращенных в условиях закрытого грунта, намного чище по сравнению с эксплантатами от растений, выращиваемых в поле. Сильно загрязнен растительный материал подземных органов растений (клубней, луковиц и т. п.). Их перед стерилизацией необходимо тщательно вымыть в мыльном растворе и прополоскать дистиллированной водой. Сложно стерилизовать растительный материал густо опушенных тканей (покрытых волосками), что затрудняет контакт стерилизующих агентов с поверхностью из-за образующихся пузырьков воздуха. Для их стерилизации применяют специальные приемы, описанные ниже. Наконец, решающим может быть выбор стерилизующих агентов. Для поверхностной стерилизации растительного материала используют растворы гипохлорита кальция или натрия (5-10 %), раствор перекиси водорода (10-12 %), бромную воду (1-2 %), растворы нитрата серебра (1 %), сулемы (хлорида ртути 0,1 %) и другие агенты, которые можно найти в каталогах фирм, производящих реактивы для культуры клеток растений. В особо трудных случаях в питательную среду добавляют антибиотики.
Высокая эффективность стерилизации эксплантатов была достигнута нами при использовании 70 % этанола и диацида. Диацид представляет собой 0,1 % водный раствор этанолмеркурихлорида С2H5СlHg и цетилпиридинил- хлорида С21Н38Сl • Н2O. Его можно использовать многократно: при правильном хранении он сохраняет эффективность в течение одного года и более. Стерилизуемый растительный материал погружают сначала в спирт (30-40 с), затем в раствор диацида (7-10 мин). После этого его тщательно промывают в 4-5 порциях проавтоклавированной дистиллированной воды.
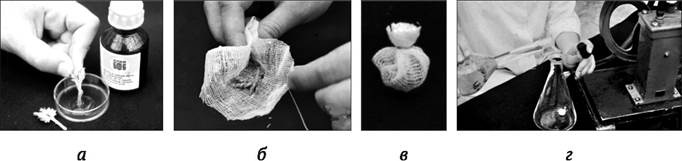
Для того чтобы улучшить смачивание стерилизуемых опушенных поверхностей эксплантатов, применяют так называемую вакуумную стерилизацию. Для ее проведения растительный материал помещают в колбу Бунзена, в которую заливают стерилизующий раствор. Колбу плотно укупоривают с помощью плотно прилегающей к горлышку пробки, подсоединяют через отводок к вакуумному насосу, и с его помощью откачивают из нее воздух (рис. 2.4).
Рис. 2.4. Стерилизация растительного материала с использованием вакуумного насоса Камовского: а - обработка среза побега (генеративный побег картофеля с бутонами, из которых предполагается вычленять пыльники) клеем БФ-6 для предотвращения попадания стерилизующего агента в срез побега в условиях вакуума; б - упаковка побегов в марлевый мешочек, позволяющий стерилизующему агенту свободно проникать к стерилизуемому материалу, а также быстро извлекать растительный материал из колбы после стерилизации; в - мешочек с упакованным растительным материалом; г - мешочек с растительным материалом, помещенный в колбу Бунзена, подсоединенную к вакуумному насосу через боковой отводок (экспериментатор заливает одной рукой в колбу стерилизующий агент, в другой руке держит пробку для укупоривания колбы)
(фото Т. В. Никонович)
Вычленение эксплантатов и перенос их в культуральные сосуды на питательную среду производят непосредственно после стерилизации растительного материала. Эту процедуру выполняют в ламинар-боксе, тщательно соблюдая правила асептики. В простейшем случае стерилизованный растительный материал помещают в открытые проавтоклавированные чашки Петри и стерильным инструментом (скальпелем или ножницами) вырезают фрагменты растительного материала нужного размера. Пробирки открывают в пламени спиртовки и с помощью стерильного длинного пинцета или уретральных щипцов эксплантат переносят на поверхность питательной среды. Для каждой очередной такой операции используют новые автоклавированные чашки Петри и простерилизованный (погружением в 96 % этанол с последующим прожиганием в пламени спиртовки) и охлажденный инструмент.
В некоторых случаях эксплантаты весьма мелкие, их необходимо освободить от покровных тканей (например, пыльники, которые извлекают из простерилизованных цветочных бутонов, колосков). Для такого случая удобно использовать проавтоклавированную подложку из двойных листов целлофана, переложенных крафт-бумагой. Растительный материал, например, цветочные бутоны, помещают ближе к краю, между двух листов целлофана и, придерживая их сверху пальцем (через целлофан), извлекают стерильным инструментом пыльники, не опасаясь их контаминации. Одной пары целлофановых листов размером 15x15 см хватает для извлечения пыльников из 8-12 бутонов (по 2-3 с каждой стороны целлофанового листа).
2.5. Условия культивирования. Перенос культур на свежую питательную среду
В зависимости от типа эксплантата и целей эксперимента для культуры клеток используют различные культуральные сосуды (стеклянные или пластиковые пробирки, чашки Петри разного размера, колбы и контейнеры) и условия культивирования. Культивирование производят в культуральных комнатах, оборудованных кондиционером. Многие культуры выращивают в темноте в термостатах. Оптимальная температура 24-26 °С. Однако в зависимости от вида растений, она может быть немного выше или ниже.
Если требуется освещение культур (для поддержания культур пробирочных растений, клонального размножения растений in vitro и др.), в простейшем случае в культуральной комнате размещают стеллажи с подсветкой лампами дневного света. Лампы включаются и выключаются автоматически в определенное время. Обычно длина светового периода составляет 14-18 ч, темнового - 6-10 ч. Температура в световой период может быть 22-26 °С, в темновой - несколько ниже, 18-20 °С. Освещенность культур варьирует в достаточно широких пределах (от 1 до 10 тыс. люкс). Для освещения культур чаще всего используют лампы дневного света. Однако могут применяться и другие лампы, в том числе со специфическими спектральными характеристиками.
Температурный и световой режим культивирования, спектральные характеристики света могут оказывать существенное влияние на индукцию процессов морфогенеза в культуре клеток растений. Поэтому для установки различных режимов культивирования целесообразно использовать климатические камеры.
Для культивирования клеточных суспензий в культуральной комнате устанавливают качалки, ротационные установки или более сложные приспособления для перемешивания и аэрации культур (биореакторы).
В процессе культивирования каллюсные клетки стареют (дифференциация каллюсных клеток), теряют способность делиться и постепенно отмирают. Также происходит истощение питательной среды, в нее могут выделяться клеточные метаболиты, которые оказывают неблагоприятное влияние на рост культур. Сама культура может существенно увеличиться в объеме, в результате чего размеры культурального сосуда становятся недостаточными. В связи с этим через определенные промежутки времени небольшой фрагмент каллюса, или объем суспензии (инокулят), переносят в стерильных условиях в приготовленные сосуды со свежей питательной средой (пассирование, субкультивирование). При регулярном пассировании способность к делению каллюсных клеток или клеток в суспензии может поддерживаться в течение десятков лет. Пробирочные растения при субкультивировании черенкуют на свежую питательную среду переносят небольшой фрагмент растения, например, кусочек стебля с 1-2 пазушными почками, из которого восстанавливается пробирочное растение.
Перенос культур с одной среды на другую применяют также для индукции у них процессов морфогенеза, прежде всего в целях получения растений-регенерантов. Это обусловлено тем, что питательные среды для пролиферации и морфогенеза клеточных культур, как правило, существенно различаются. Одновременно с пассированием нередко изменяют и условия культивирования (световой и температурный режимы).
Заключение
Работы по получению и поддержанию культуры клеток растений требуют специальных помещений, оборудования, инструментов, предполагают использование сложных питательных сред.
Существует большое количество питательных сред для разных задач культивирования, видов растений и типов эксплантатов. Наиболее часто используется среда Мурасиге и Скуга. Она хорошо сбалансирована по входящим в нее компонентам и дает хорошие результаты при культивировании клеток многих видов растений. Питательные среды для культуры клеток растений должны включать в себя все необходимые минеральные и органические элементы в концентрациях, максимально приближенных к тем, которые получают интактные растения для нормального роста и развития в условиях in vivo: макро- и микроэлементы, витамины, углеводы. Добавка в питательную среду регуляторов роста растений позволяет стимулировать пролиферацию культур клеток или индуцировать процессы морфогенеза.
Культура клеток растений может быть получена и успешно поддерживаться только при условии соблюдения асептики. Это достигается благодаря использованию различных методов стерилизации помещений, лабораторной посуды, инструмента, питательных сред. Особо тщательно стерилизуют поверхность эксплантатов, предназначенных для получения культуры клеток. Все работы, при которых открывают культуральные сосуды (разлив стерильной питательной среды по пробиркам, чашкам Петри, колбам, вычленение эксплантатов и их перенос на питательную среду, перенос части культуры на свежую питательную среду и др.) проводят в стерильных условиях в рабочем пространстве ламинар-бокса с соблюдением правил асептики.
В зависимости от типа эксплантата и целей эксперимента для культуры клеток используют различные культуральные сосуды и условия культивирования. Культивирование производят в культуральных комнатах, оборудованных кондиционером, в темноте (в термостатах) или при освещении (на специальных стеллажах, оборудованных подсветкой, либо в климатических камерах). Температурный и световой режим культивирования, спектральные характеристики света могут оказывать существенное влияние на пролиферацию клеток, индукцию процессов морфогенеза в культуре клеток растений.
Через определенные промежутки времени производят перенос культур на свежую питательную среду (пассирование, субкультивирование) для того,
чтобы избежать истощения питательных сред, неблагоприятного эффекта метаболитов, выделяемых в среду в процессе культивирования, недостаточного объема культурального сосуда для разросшихся культур.
Контрольные вопросы
1. Назовите основные элементы синтетических питательных сред для культуры клеток растений.
2. Для каких целей используют запасные растворы компонентов питательной среды?
3. Каким образом обеспечивают условия асептики при получении культуры клеток растений?
4. Для чего необходимо проводить субкультивирование клеточных культур?