БІОТЕХНОЛОГІЯ - В. Г. Герасименко - 2006
Частина ІІ. Спеціальні біотехнології
Розділ 16. ДНК-ВАКЦИНИ
16.4. МОДУЛЯЦІЯ ІМУННОЇ ВІДПОВІДІ
В сироватках крові інтактних тварин присутні в невеликих титрах аутоантитіла проти ДНК, але вони мало специфічні. Молекули ДНК є слабкими імуногенами внаслідок своєї рухливої конформації в розчині, тому введення в тканини організму рекомбінантних плазмід не впливає на титри антитіл проти ДНК.
Для багатьох антигенів інокуляція 50-100 мкг очищеної плазмідної ДНК з/або без бустерного введення призводить до сильної імунної відповіді на відповідний білок, ген якого входить до складу ДНК-вакцини. В численних дослідах на лабораторних тваринах було встановлено, що кількість рекомбінантної плазміди, необхідної для ДНК-вакцинації, може коливатись у межах 0,001-10 мкг на 1 г маси тіла тварини, що значною мірою визначається вибраним методом та місцем введення плазмідної ДНК. Так, у деяких випадках внутрішньошкірне введення ДНК-вакцини дозволяє отримати імунну відповідь, рівну або більшу, ніж при внутрішньом’язовому введенні, при використанні плазмідної ДНК в концентраціях, в сотні разів нижчих. Це може пояснюватися тим, що шкіра та мембрани слизових оболонок є анатомічними сайтами, в які потрапляють більшість екзогенних антигенів. Лімфоїдні тканини, поєднані зі шкірою, утримують спеціалізовані клітини, які підвищують імунну відповідь. Кератиноцити продукують інтерлейкін-1 (ІЛ-1) та α-фактор некрозу пухлин, які можуть активувати лімфоцити, макрофаги та дендритні клітини. Клітини Лангерганса шкіри переносять антиген від шкіри до лімфатичних вузлів (рис. 16.2). Вони є потенційними активаторами нативних Т-лімфоцитів. Спеціальний підклас Т-лімфоцитів, які циркулюють (епідермотропні лімфоцити) прямують у шкіру і відіграють критичну роль у шкірному імунітеті. Дендритні клітини і макрофаги дерми можуть також захоплювати антиген і ініціювати імунну відповідь. Таким чином, трансфекція за допомогою генної рушниці епідермальних або дермальних клітин in vivo за допомогою ДНК може вважатись ефективним шляхом генної імунізації, що нагадує фізіологічну відповідь на патоген при інфекційному процесі або при використанні живих вакцин. Водночас існують дані (Deruabin O. et al., 2003), що без докладання механічних зусиль для введення ДНК безпосередньо в клітини досить ефективною є внутрішньом’язова імунізація, при якій спостерігається найвищий рівень експресії антигену. Особливістю такого введення є формування клітинного імунітету з утворенням переважно специфічних цитотоксичних лімфоцитів (ЦТЛ), а механізм індукції гуморальної імунної відповіді не визначений до кінця, тому що кількість антигенпрезентуючих клітин у м’язах незначна.
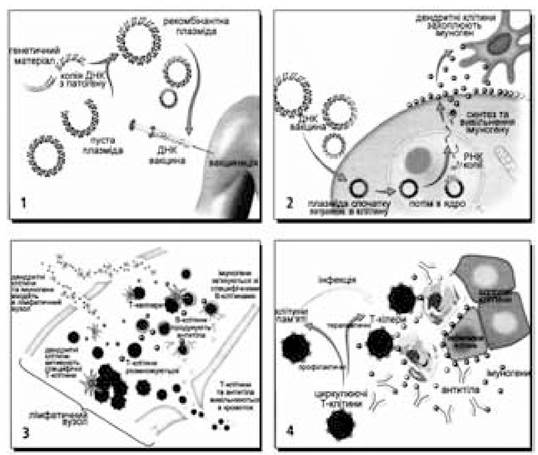
Рис. 16.2. Схема модуляції імунної відповіді при внутрішньошкірному введенні ДНК-вакцини
Формування імунної відповіді при введенні ДНК-вакцини має певні особливості. На прикладі вірусу кліщового енцефаліту було показано, що попри на низький рівень експресії вірусних генів при генній імунізації, який становив 10-12 г, відбувалась індукція імунної відповіді і ефективний захист тварин, тоді як імунізація розчиненими інактивованими білковими вакцинами з концентрацією вірусних білків приблизно 10-9 г не викликала утворення кількості антитіл, які б навіть виявлялися в імуноферментному аналізі (Морозова О.В. та ін., 2000). Таким чином, введення ДНК-вакцини призводить до індукції специфічної клітинної та гуморальної відповіді.