Молекулярная биотехнология. Принципы и применение - Глик Б., Пастернак Дж. 2002
Основы молекулярной биотехнологии
Химический синтез, определение нуклеотидной последовательности и амплификация ДНК
Химический синтез ДНК
Технологический прогресс в любой области науки всегда стимулирует ее дальнейшее развитие. С появлением новых технологий появляется возможность ставить новые эксперименты и облегчается проведение старых. Становление молекулярной биотехнологии как науки обязано целому ряду технологических разработок; многие из них ныне широко применяются как в крупных исследовательских центрах, так и небольших научных коллективах. Теперь не составляет особого труда химически синтезировать одну молекулу ДНК, определить нуклеотидную последовательность другой и амплифицировать с помощью полимеразной цепной реакции третью. Все это стало возможным благодаря той информации, которая была получена в ходе основополагающих исследований как самой ДНК, так и механизма ее репликации. Эти экспериментальные подходы стали неотъемлемой частью молекулярного клонирования - процедуры, позволяющей выделять из ДНК нужные фрагменты, охарактеризовывать их и производить с ними разнообразные манипуляции.
С разработкой быстрых и недорогих методов химического синтеза одноцепочечных ДНК-фрагментов с заданной нуклеотидной последовательностью методология молекулярного клонирования и характеризации ДНК существенно изменилась. Химически синтезированные олигонуклеотиды можно использовать для конструирования целых генов или их фрагментов, для амплификации специфических фрагментов ДНК, для направленных мутаций изолированных ДНК, а также в качестве зондов при гибридизации и в качестве линкеров, облегчающих клонирование.
С появлением приборов для автоматического химического синтеза ДНК (ДНК-синтезаторов) получение одноцепочечных олигонуклеотидов длиной <50 звеньев стало более или менее рутинной процедурой. Основным компонентом любого ДНК-синтезатора является система клапанов и насосов, с помощью которых в реакционную смесь по строго заданной программе вводятся нуклеотиды и реагенты, обеспечивающие присоединение нужных мономерных единиц к растущей цепи. В отличие от биологического, в ходе химического синтеза ДНК каждый новый нуклеотид можно присоединять к 5'-гидроксильному концу цепи. Все реакции осуществляются последовательно в одной реакционной колонке, а продолжительность каждой из них и время отмывания контролируются с помощью компьютера.
Фосфорамидитный метод В настоящее время это наиболее распространенный метод химического синтеза ДНК. Исходными строительными блоками в нем являются модифицированные дезоксирибонуклеозиды. Модификация состоит в присоединении к аминогруппам дезоксиаденозина и дезоксицитидина бензольной группы, а к аминогруппе дезоксигуанозина — изобутирильной. Тимидин, у которого отсутствует аминогруппа, не модифицируют. Такая модификация необходима для защиты нуклеозидов от нежелательных побочных реакций при росте цепи. Синтез осуществляют в твердой фазе (растущая цепь ДНК фиксируется на твердом носителе), что позволяет проводить все реакции в одной емкости, легко отмывать после каждого этапа ненужные реагенты и добавлять новые в количестве, обеспечивающем возможно полное протекание реакции.
Этапы многоступенчатого синтеза представлены на рис. 5.1. Первый нуклеозид (азотистое основание + сахар) фиксируют на инертном твердом носителе, обычно это пористые стеклянные шарики с порами одинакового размера. 3'-гидроксильная группа первого нуклеозида, который будет 3'-концевым нуклеотидом синтезируемой цепи, прикрепляется к спейсерной молекуле, ковалентно связанной с носителем. Чтобы предотвратить неспецифическое взаимодействие 5'-гидроксильной группы первого нуклеотида до добавления в реакционную смесь второго нуклеотида, ее защищают с помощью диметокситритильной (ДМТ) группы (рис. 5.2). Такую группу содержит каждый присоединяемый к растущей цепи нуклеотид, а кроме того, он несет диизопропиламинную группу, присоединенную к 3'-фосфитной группе, которая в свою очередь защищена метальным остатком (рис. 5.3). Такая молекулярная конфигурация и называется фосфорамидитом.
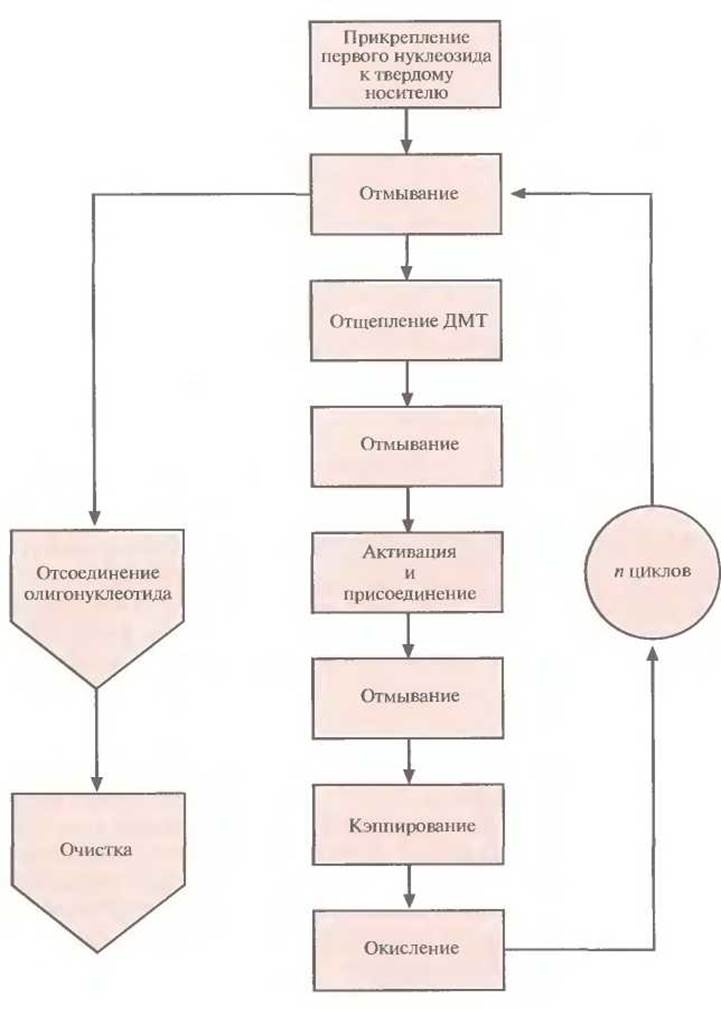
Рис. 5.1. Химический синтез олигонуклеотида. После n циклов образуется одноцепочечный фрагмент ДНК из n + 1 нуклеотида.
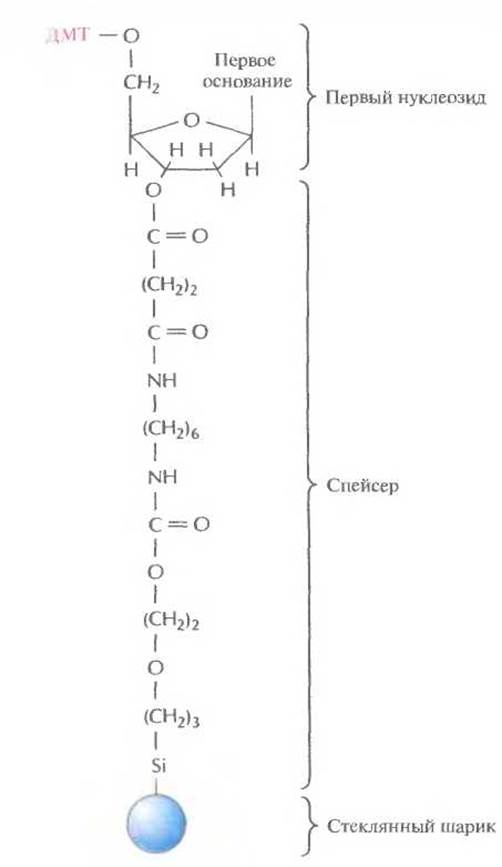
Рис. 5.2. Комплекс, с которого начинается химический синтез цепи ДНК. К 5'-гидроксильной группе дезоксирибозы первого нуклеозида присоединена диметокситритильная (ДМТ) группа, а к 3' -гидроксильной группе — спейсерная молекула. Последняя в свою очередь связана с твердым носителем (пористым стеклянным шариком).
Цикл начинается после присоединения первого нуклеозида к стекляному шарику. Далее колонку обильно промывают каким-либо безводным реагентом (например, ацетонитрилом), чтобы удалить воду и другие нуклеофильные вещества, и продувают через нее аргон для вытеснения ацетонитрила. Затем с помощью трихлор-уксусной кислоты (ТХУ) отщепляют 5'-ДМТ (детритилирование) от присоединенного нуклеотида, с тем чтобы высвободить (экспонировать) реакционноспособную 5'-гидроксильную группу (рис. 5.4). Колонку вновь промывают ацетонитрилом для удаления ТХУ и продувают через нее аргон для удаления ацетонитрила. Процесс запрограммирован таким образом, чтобы на втором этапе в колонку одновременно вводились следующий нуклеозид (в виде фосфорамидита) и тетразол (активация и присоединение). Тетразол активирует фосфорамидит, так что 3'-фосфитная группа образует ковалентную связь с 5'-гидроксильной группой первого нуклеозида (рис. 5.5). Невключившийся фосфорамидит и тетразол удаляют продуванием аргона.
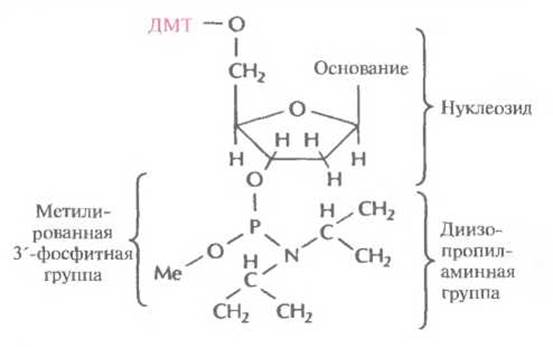
Рис. 5.3. Структурная формула фосфорамидита. Такие производные всех четырех оснований — А, Т, G и С — используются для химическою синтеза ДНК. ДМТ — диметокситритил, Me — метальная группа.
Поскольку по окончании первого этапа не все фиксированные на носителе нуклеозиды оказываются связанными с фосфорамидитом, необходимо предотвратить их взаимодействие с нуклеозидом, добавленным на втором этапе. Для этого непрореагировавшую 5'-гидроксильную группу ацетилируют с помощью уксусного ангидрида и диметиламинопиридина (кэппирование) (рис. 5.6). Если этого не сделать, то уже после нескольких циклов синтезируемые олигонуклеотиды будут различаться как по длине, так и по нуклеотидной последовательности. Фосфиттриэфирная связь, образовавшаяся на втором этапе между нуклеотидами, нестабильна и может разорваться в присутствии кислоты или щелочи. Поэтому фосфиттриэфир окисляют с помощью йодной смеси до более стабильного пятивалентного фосфаттриэфира (рис. 5.7). Затем промывают колонку и повторяют весь цикл (детритилирование, активация и присоединение, кэппирование, окисление; рис. 5.1). Все описанные операции проводят до тех пор, пока к растущей цепи в соответствии с программой не присоединится последний нуклеозид. Синтезированные олигонуклеотиды связаны со стеклянными шариками; каждый фосфаттриэфир несет метальную группу; каждый гуанин, цитозин и аденин содержит защищенную аминогруппу, а на 5'-конце последнего нуклеотида находится ДМТ-группа.

Рис. 5.4. Детритилирование — отщепление 5'-диметокситритильной (ДМТ) группы с помощью трихлоруксусной кислоты (ТХУ).
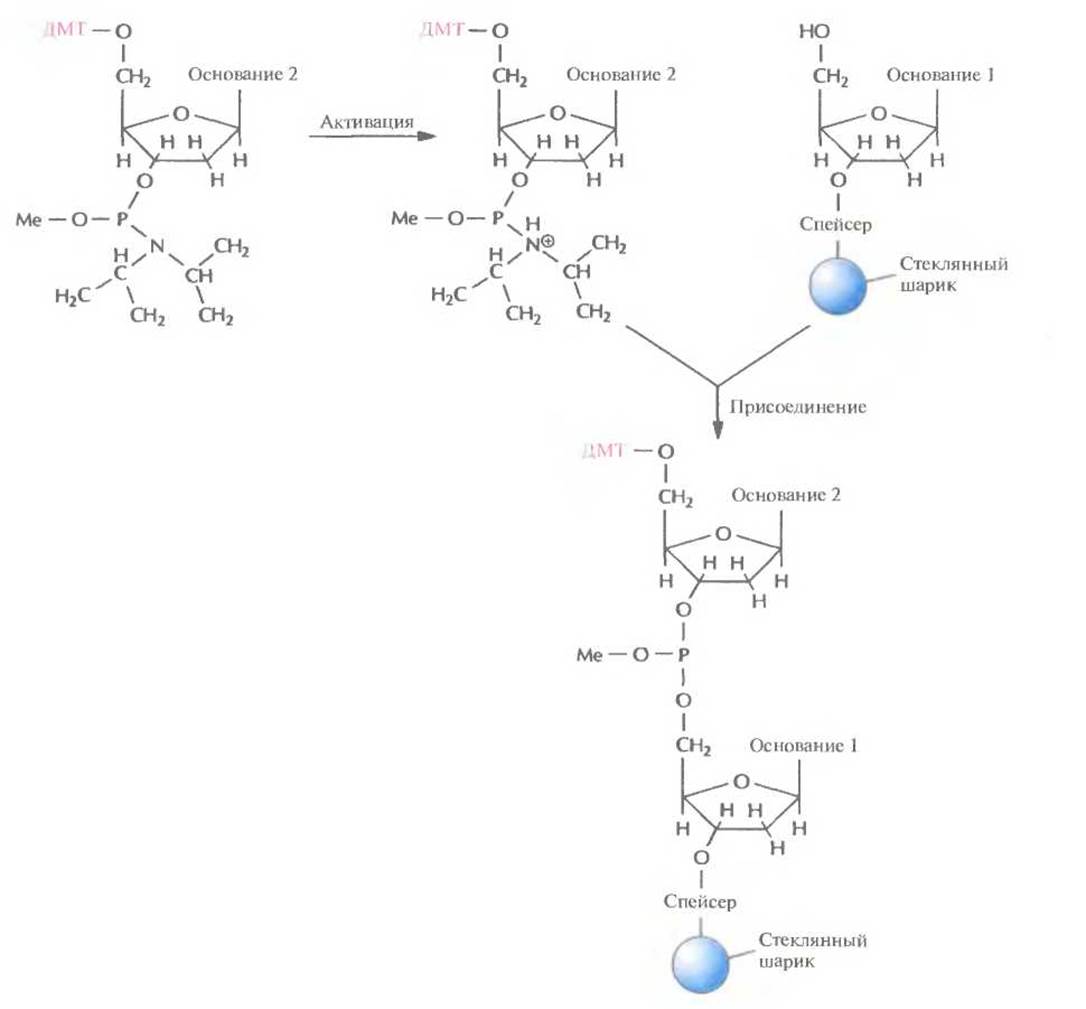
Рис. 5.5. Активация и присоединение. 3'-фосфитная группа активированного фосфорамидита образует ковалентную связь с 5'-гидроксильной группой фиксированного на стеклянном шарике детритилированного нуклеозида. ДМТ — диметокситритильная группа, Me — метильная группа.

Рис. 5.6. Кэппирование. Свободные 5'- гидроксильные группы непрореагировавших в первом цикле детритилированных нуклеозидов ацетилируют, чтобы предотвратить их участие в следующем цикле.
Метальные группы удаляют с помощью химической обработки непосредственно в реакционной колонке. Затем отсоединяют олигонуклеотиды от спейсерной молекулы вместе с 3'-гидроксильным концом и элюируют их из колонки; далее последовательно удаляют бензоильные, изобутирильные и ДМТ-группы. 5’-конец цепи фосфорилируют ферментативным (полинуклеотидкиназа Т4+АТР) или химическим методом. Эту реакцию можно проводить и тогда, когда олигонуклеотид еще связан с носителем, но после детритилирования.
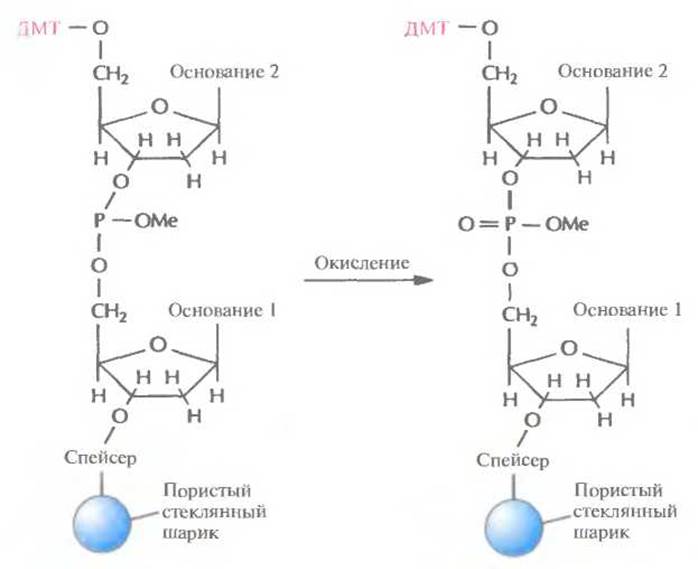
Рис. 5.7. Окисление. Фосфиттриэфир окисляется до пятивалентного фосфаттриэфира, что приводит к стабилизации фосфодиэфирной связи и делает ее более устойчивой к действию кислот и шелочей. ДМТ — диметокситритильная группа. Me — метальная группа.
Чтобы выход продукта был достаточно высок, эффективность присоединения нуклеотидов на каждом этапе должна быть не ниже 98%. Эффективность контролируют спектрофотометрическими методами, определяя количество удаляемых тритильных групп. Если, например, при синтезе 20-членного олигонуклеотида эффективность каждого цикла равна 99%, то 82% (т. е. 0,9920∙ 100) олигонуклеотидов будут иметь именно такую длину. Если же синтезируется 60членный олигонуклеотид, то при той же эффективности только 55% олигонуклеотидов будут содержать по 60 нуклеотидов. А если средняя эффективность цикла не превышает 98%, то доля олигонуклеотидов заданной длины будет гораздо ниже (табл. 5.1). Фирмы — изготовители коммерческих ДHК-синтезаторов обычно гарантируют среднее значение эффективности присоединения 98%. Но для этого необходимо использовать реагенты и химикаты очень высокой степени чистоты, что не всегда удается выполнить. Как правило, реальная эффективность присоединения составляет 95%, хотя иногда удается достичь и 99%-ной эффективности. Чтобы получить олигонуклеотиды заданной длины, первичные продукты большинства химических синтезов необходимо очистить с помощью либо высокоэффетивной жидкостной хроматографии под высоким давлением с обращенной фазой, либо электрофореза в полиакриламидном геле. Поскольку все «неудачные» последовательности короче, чем тот олигонуклеотид, который хотят получить, сделать это нетрудно.
Таблица. 5.1. Средний выход олигонуклеотидов заданной длины (и) при разных значениях средней эффективности цикла
|
Эффективность, % |
Средний выход, % |
||||
|
n = 20 |
n = 40 |
n = 60 |
n = 80 |
n = 100 |
|
|
90 |
12 |
1,5 |
0,18 |
0,02 |
0,003 |
|
95 |
36 |
13 |
4,6 |
1,7 |
0,6 |
|
98 |
67 |
45 |
30 |
20 |
13 |
|
99 |
82 |
67 |
55 |
45 |
37 |
|
99,5 |
90 |
82 |
74 |
67 |
61 |
Применение синтезированных олигонуклеотидов
Олигонуклеотиды, синтезированные химическими методами, находят широкое применение в молекулярной биотехнологии. Их используют в качестве зондов при ДHК-гибридизации, линкеров, соединяющих разные молекулы ДНК в экспериментах по клонированию, праймеров при секвенировании ДНК или осуществлении сайт-специфического мутагенеза клонированных генов-мишеней.
1. Нуклеотидную последовательность специфических олигонуклеотидных зондов (длиной 20—40 звеньев) находят из данных об аминокислотной последовательности соответствующих белков.
2. Для получения линкеров синтезируют олигомеры, которые представляют собой палиндромные одноцепочечные нуклеотидные последовательности, спаривающиеся (гибридизующиеся) между собой. Линкеры содержат сайты узнавания для рестрицирующих эндонуклеаз, что позволяет осуществлять с их помощью клонирование фрагментов ДНК (рис. 5.8, А и Б). Короткий дуплекс длиной 6—12 пар нуклеотидов лигируют по тупым концам с ДНК-мишеныо (обычно кДНК). Разрезают новую молекулу нужной рестрицирую- щей эндонуклеазой и получают фрагменты с выступающими одноцепочечными концами (липкими концами), с помощью которых встраивают ДНК-мишень в соответствующий вектор. Прежде чем проводить встраивание, рестрицированную смесь фракционируют для отделения ДНК с липкими концами от лишних линкерных молекул. Вектор тоже обрабатывают рестриктазой, отжигают его с фрагментами ДНК с липкими концами и сшивают с помощью ДНК-лигазы фага Т4. ДНК-мишень не должна содержать сайтов рестрикции, присутствующих в линкерной последовательности, в противном случае она также будет расщепляться ферментом.
3. Один из вариантов линкерных последовательностей, так называемые «адаптеры», часто содержат сайты для двух и более рестрицирующих эндонуклеаз (рис. 5.8, В). С их помощью можно встраивать кДНК в вектор лигированием по тупым концам, а затем вырезать, используя другую рестриктазу. Адаптор, изображенный на рис. 5.8, В, встраивают в BamHI-сайт вектора перед включением ДНК-мишени в SmaI-cайт по тупым концам. После клонирования кДНК вырезают из вектора с помощью рестриктазы ВаmHI. В этом случае вектор не должен содержать SmаI-сайтов, и ни вектор, ни кДНК не должны нести BamHI -сайтов.

Рис. 5.8. Типичные линкеры и адаптор. А. EcoRI-линкер. состоящий из 6 пар нуклеотидов. Б. EcoRI-линкер из 8 пар нуклеотидов. В. BamHI-SmaI-адаптор с BamНI-липкими концами и сайтом узнавания для Smal.
4. Одноцепочечные олигонуклеотиды из -17—24 звеньев используют в качестве праймеров при секвенировании ДНК и проведении ПЦР.
5. Одноцепочечные олигонуклеотиды используют в качестве праймеров для сайт-специфического мутагенеза in vitro.
6. Необходимость в химическом синтезе нуклеотидной последовательности, кодирующей какой-то конкретный белок, может возникнуть тогда, когда клонирование соответствующего гена затруднено. При этом нуклеотидную последовательность гена находят из данных об аминокислотной последовательности белка. К химическому синтезу прибегают и тогда, когда кодоны, из которых состоит данный ген, плохо считываются организмом-хозяином, и уровень трансляции оказывается очень низким. В таком случае можно синтезировать ген с таким набором кодонов (оптимизация кодонов), при котором аминокислотная последовательность кодируемого белка остается прежней, а кодоны считываются хозяйским организмом более эффективно.
Синтез генов
Если химически синтезированную двухцепочечную ДНК предполагается использовать в качестве гена или его фрагмента, то каждую из ее цепей синтезируют отдельно. Получить короткие гены (60—80 п. н.) технически несложно: для этого синтезируют комплементарные цепи и затем отжигают их. В случае крупных генов (>300 п. н.) приходится применять специальные стратегии, поскольку эффективность каждого цикла химического синтеза никогда не достигает 100%. Например, если ген состоит из 999 пар нуклеотидов, а эффективность каждого цикла равна 99%, то доля полноразмерных одноцепочечных ДНК по окончании процесса составит не более 0,004%. Чтобы решить эту проблему, синтетические (двухцепочечные) гены собирают из модулей — (одноцепочечных) фрагментов длиной от 20 до 100 нуклеотидов.
Один из способов конструирования синтетического гена заключается в получении набора олигонуклеотидов длиной 20—60 нуклеотидов каждый с перекрывающимися концами. Нуклеотидные последовательности цепей задают так, чтобы после отжига концевые сегменты гена имели тупые концы. Каждый внутренний сегмент имеет выступающие 3'- и 5'-концы, комплементарные таковым соседнего сегмента (рис. 5.9). После сборки гена остается сшить одноцепочечные разрывы с помощью ДНК-лигазы Т4. Синтетические гены могут быть сконструированы так, чтобы помимо белок-кодирующих последовательностей они содержали концевые участки, обеспечивающие их встраивание в клонирующий вектор (сайты для рестрицирующих эндонуклеаз), а также, если это необходимо, сигнальные последовательности для правильной инициации и терминации транскрипции и трансляции.
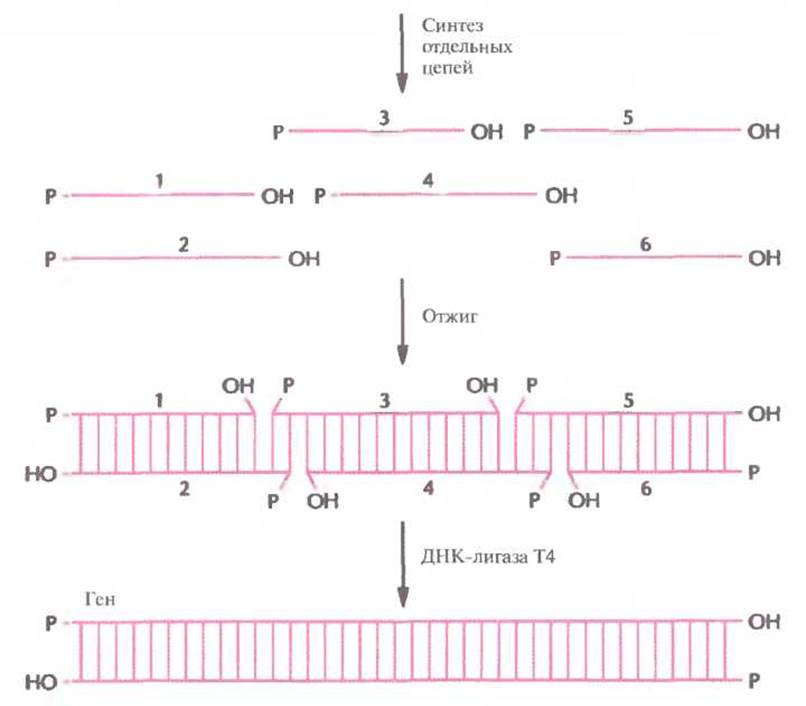
Рис. 5.9. Сборка синтетического гена из коротких олигонуклеотидов. Синтезируют отдельные олигонуклеотиды длиной от 20 до 60 звеньев каждый с такими нуклеотидными последовательностями, чтобы при отжиге из них образовалась двухцепочечная молекула. Оставшиеся одноцепочечные разрывы сшивают с помощью ДНК-лигазы Т4.
ноцепочечные разрывы с помощью ДНК-лигазы Т4. Синтетические гены могут быть сконструированы так, чтобы помимо белок-кодирующих последовательностей они содержали концевые участки, обеспечивающие их встраивание в клонирующий вектор (сайты для рестрицирующих эндонуклеаз), а также, если это необходимо, сигнальные последовательности для правильной инициации и терминации транскрипции и трансляции.
Для получения полноразмерных генов другим способом тоже вначале синтезируют специфический набор перекрывающихся олигонуклеотидов длиной от 40 до 100 звеньев. При их отжиге происходит спаривание 6—10 3'- и 5'-концевых взаимно комплементарных нуклеотидов, а между ними остаются большие бреши. Протяженность спаренных участков достаточно велика, чтобы стабилизировать всю структуру. Бреши заполняют ферментативным путем с помощью ДНК-полимеразы I Escherichia coli, использующей 3'-гидроксильные группы для инициации репликации и одноцепочечные участки в качестве матрицы. Оставшиеся одноцепочечные разрывы сшивают с помощью ДНК-лигазы Т4 (рис. 5.10).
Более протяженные гены (>1000 п. н.) обычно собирают из двухцепочечных фрагментов, каждый из которых в свою очередь состоит из 4—6 перекрывающихся олигонуклеотидов (от 20 до 60 п. н. каждый). Если после синтеза и отжига образуется достаточное количество фрагментов, то их просто соединяют друг с другом. В противном случае каждый фрагмент клонируют и амплифицируют. Двухцепочечные фрагменты последовательно соединяют друг с другом до образования полноразмерного гена. Чтобы гарантировать правильность нуклеотидной последовательности химически синтезированного гена, секвенируют каждый двухцепочечный фрагмент, а затем и весь ген.
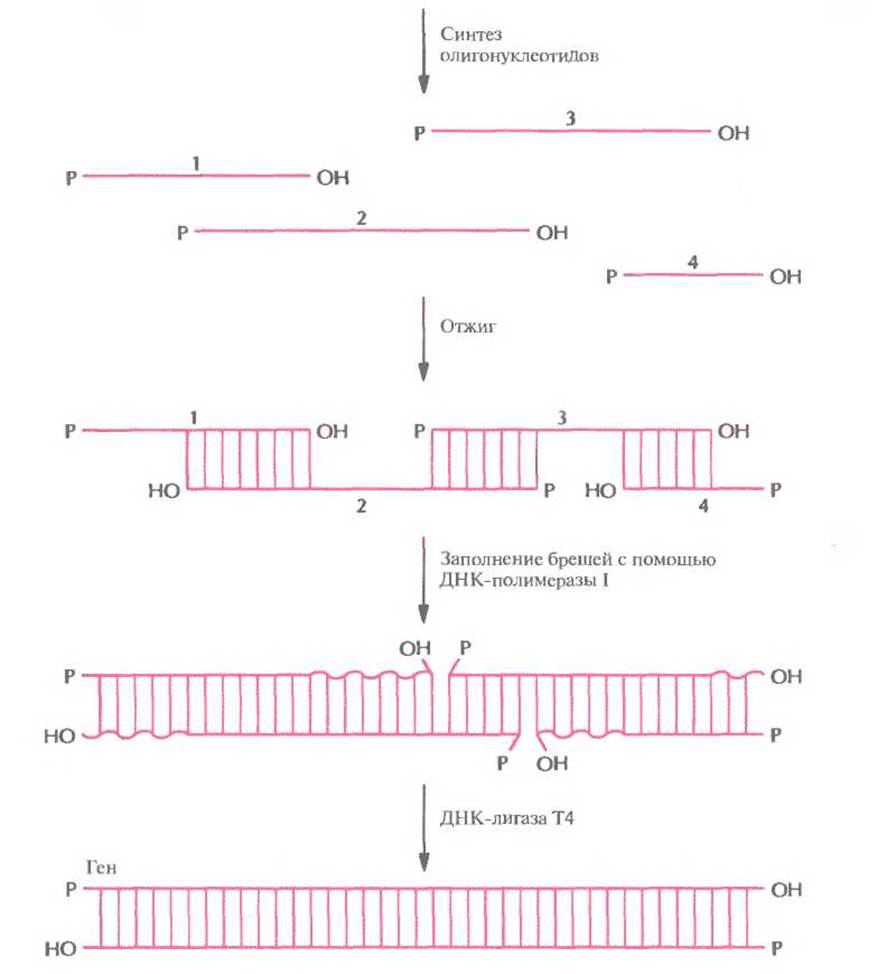
Рис. 5.10. Сборка протяженного гена in vitro с участием ферментов. Вначале химическими методами синтезируют отдельные олигонуклеотиды с такими нуклеотидными последовательностями, чтобы при отжиге между ними образовывались спаренные участки длиной 6—10 пар нуклеотидов. Оставшиеся между ними бреши заполняют с помощью ДНК-полимеразы 1 Е.coli, а одноцепочечные разрывы сшивают ДНК-лигазой Т4.