Основы молекулярной биологии. Часть 1: Молекулярная биология клетки - А.Н. Огурцов 2011
Компоненты биомолекулярных комплексов
Атомный состав живых организмов
В живых организмах обнаруживаются только 40 наиболее легких элементов из 92 природных химических элементов, присутствующих в природе. Причем из этих 40, только 27 существенны для жизнедеятельности организмов, остальные элементы (например, висмут, свинец, олово, кадмий, сурьма, таллий и др.) являются загрязняющими примесями.
Атомный состав даже очень разных по уровню сложности организмов различается значительно меньше, чем состав любого организма отличается от состава литосферы.
На долю четырех химических элементов - С, О, Н и N - приходится около 98% веса организма. Из этих элементов состоят все органические соединения, поэтому их называют органогенами.
Остальные элементы, составляющие организм, подразделяются на макроэлементы (К, S, Р, Cl, Mg, Na, Ca и Fe), которые содержатся в количестве 0,01-0,1 весовых %, и микроэлементы (Zn, Cu, I, F, Mn, В, Br, Со, Mo, Si, Ba, Se, V, Cr, Ni), содержание которых меньше 0,01%.
Несмотря на малые количества, микроэлементы выполняют некоторые незаменимые функции (например, входят в состав ферментов), поэтому недостаток любого из них приводит к серьезным нарушениям обмена веществ. Избыток микроэлементов столь же опасен из-за возможности их вступления в неспецифические химические реакции.
Из неорганических веществ клетки большая часть находится в виде солей. Концентрации катионов и анионов в клетке и в среде её обитания, как правило, сильно отличаются.
Например, внутри животной клетки концентрация ионов К+ равна 140 мМ, a Na+- от 5 до 15 мМ, тогда как в межклеточной или внешней среде мало калия (5 мМ) и довольно высокая концентрация натрия (145 мМ). Это различие в концентрации ионов между клеткой и средой выполняет специальную функцию создания разности потенциалов на плазматической мембране и, пока клетка жива, активно поддерживается. После смерти клетки содержание ионов в клетке и среде быстро выравнивается.
От солей в значительной мере зависят поступление воды в клетку и буферные свойства клеток и тканей. Клеточные мембраны проницаемы для молекул воды и непроницаемы для крупных молекул и ионов.
Если в среде содержание воды более высокое, чем в клетке, то выравнивание концентрации воды между клеткой и средой происходит путем проникновения воды из среды в клетку (явление осмоса). На этом свойстве, например, основано всасывание воды корнями растений.
Неорганические ионы (Са2+ и Mg2+) участвуют в регуляции каталитической способности многих белков-ферментов, связываясь с ними и тем самым активируя их.
Другие ионы (Cu2+, Fe2+, Zn2+) сами входят в состав реакционного центра некоторых ферментов.
Ион Са2+ играет важную роль в распространении нервного импульса и мышечном сокращении, а неорганический фосфат является необходимым компонентом внутриклеточной АТФ-зависимой системы переноса энергии.
Неорганические соли содержатся в клетке не только в растворенном, но и в твердом состоянии, выполняя структурную функцию. В частности, прочность и твердость костной ткани и раковинам моллюсков придает нерастворимый гидроксиапатит, состав которого можно приблизительно описать формулой Са5(РO4)3OН.
В водных растворах биологически важные ионы, такие как К+, Na+, Са2+, Mg2+, Сl-, не существуют в виде изолированных ионов, а всегда гидратированы - окружены электростатически взаимодействующими с ионом полярными молекулами воды (рисунок 40).
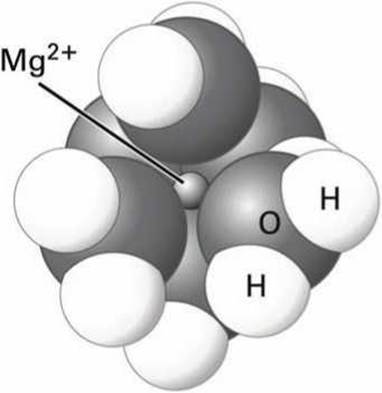
Рисунок 40 - Гидратированный катион магния