МІКРОБІОЛОГІЯ - М.Г. Сергійчук - 2008
Розділ 5. МЕТАБОЛІЗМ МІКРООРГАНІЗМІВ
ДЕЯКІ ПРОЦЕСИ АНАБОЛІЗМУ В МІКРООРГАНІЗМІВ
Оскільки більшість процесів анаболізму в мікро- та макроорганізмів ідентичні, розглянемо лише деякі з них, типові саме для мікроорганізмів.
Реакції анаболізму у клітині можна розділити на три рівні: рівень 1 - синтез мономерів та дрібних молекул; рівень 2 - синтез полімерів та макромолекул; рівень 3 - синтез структурних компонентів клітини. Утворення структурних компонентів клітини здійснюється з чотирьох класів макромолекул: нуклеїнових кислот, білків, полісахаридів і складних ліпідів. Для синтезу макромолекул клітині необхідно понад 100 дрібних молекул: рибонуклеотидів (4 типи), дезоксирибонуклеотидів (4 типи), амінокислот (близько 20), моноцукрів (близько 15), понад 20 речовин для синтезу складних ліпідів, 20 коферментів і переносників тощо. Вони утворюються з попередників біосинтезу, які також називають ключовими метаболітами, проміжними метаболітами або центраболітами. Ключовими метаболітами є глюкозо-1-фосфат, глюкозо-6-фосфат, рибозо-5-фосфат, еритрозо-4-фосфат, фосфоенолпіруват, піруват, 3-фосфогліцеринова кислота, α-кетоглутарова кислота, сукциніл-КоА, щавлево-оцтова кислота, діоксіацетонфосфат, ацетил-КоА.
У гетеротрофних мікроорганізмів ключові метаболіти вилучаються з катаболічних, а точніше, амфіболічних шляхів, а в автотрофних - синтезуються з неорганічного вуглецю. У зв'язку з цим у метаболізмі автотрофів розрізняють один потік вуглецю, направлений на біосинтез (СО2 → ключові метаболіти → складні органічні сполуки). У гетеротрофів спостерігається два потоки вуглецю: один (катаболічний), направлений на розщеплення органічного субстрату через ключові продукти до СО2 та Н2О; другий (анаболічний) - від ключових продуктів на біосинтез (рис. 5.27).
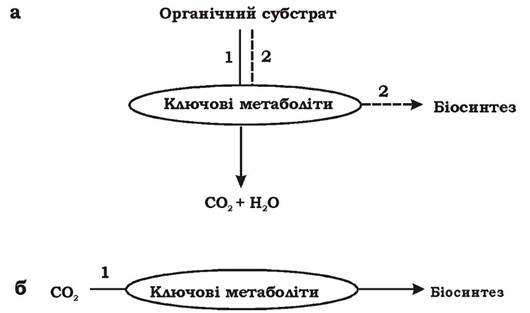
Рис. 5.27. Два потоки вуглецю в метаболізмі гетеротрофних мікроорганізмів (а) та один потік вуглецю в метаболізмі автотрофних мікроорганізмів (б)
Таким чином, у хемоорганотрофних мікроорганізмів початковий субстрат частково розщеплюється до кінцевих продуктів з утворенням АТФ та відновлених еквівалентів, а частково служить будівельним матеріалом для біосинтезу.
Відтік ключових метаболітів з циклічних шляхів може порушити їхнє функціонування. Уявімо, наприклад, що клітина росте на глюкозі як єдиному джерелі енергії, електронів і вуглецю. Для отримання енергії вона має розщепити молекулу глюкози через гліколітичний шлях та ЦТК. Але для біосинтезу амінокислот клітині необхідно також вилучити з ЦТК деяку кількість α-кетоглутарату та ЩОК. Якщо клітина почала процес метаболізму зі 100 молекул глюкози, то з них утвориться 200 піруватів, а отже і 200 ацетил-КоА, які спрямуються в ЦТК. Уявімо, що на першому оберті циклу для біосинтезу глутамінової кислоти з ЦТК буде вилучено 50 молекул α-кетоглутарової кислоти, а для синтезу аспарагінової кислоти - 50 молекул ЩОК. Залишається лише 100 молекул ЩОК для приєднання наступної порції ацетил-КоА. На другому оберті циклу на ЦТК подаються наступні 200 молекул ацетил-КоА, але включитися в цикл уже можуть лише 100 молекул, оскільки в циклі є лише 100 молекул ЩОК. Знову 50 молекул α-кетоглутарової кислоти та 50 молекул ЩОК видаляться з циклу на біосинтез. На третьому оберті циклу 200 молекул ацетил-КоА надходять у ЦТК, але акцептора для них (ЩОК) уже немає. Отже, без додаткового поповнення пулу ключових метаболітів, що відходять на біосинтез, циклічні шляхи, функціонувати не можуть. Таке поповнення здійснюється за рахунок спеціальних анаплеротичних реакцій (реакцій поповнення).
Відомо кілька типів реакцій, що класифікують як анаплеротичні:
1. Утворення оксалоацетату (ЩОК) з пірувату чи фосфоенолпірувату (реакція Вуда - Веркмана).
2. Поповнення пулу ЩОК за рахунок гліоксилатного шунта.
3. Перетворення аспарагінової кислоти в оксалоацетат (див. реакції трансамінування амінокислот).
4. Перетворення глутамінової кислоти в α-кетоглутарову внаслідок дезамінування.
Найбільш важливою у природі анаплеротичною реакцією є реакція карбоксилювання пірувату до ЩОК за допомогою піруваткарбоксилази:
![]()
Вона відбувається в мітохондріях клітин тварин, але не рослин. Ця реакція здійснює безпосередній зв'язок між гліколізом та ЦТК. Піру- ваткарбоксилаза активується ацетил-КоА, тому коли кількість ацетил- КоА перевищує запаси ЩОК, рівень ЩОК швидко збільшується за допомогою піруваткарбоксилази. Реакція енерговитратна.
Реакція Вуда - Веркмана (рис. 5.28): Фосфоенолпіруват (ФЕП) карбоксилюється за допомогою фосфоенолпіруваткарбоксилази:
![]()
Ця реакція має місце у дріжджів, бактерій і вищих рослин, але ніколи у тварин. Вона відбувається з використанням багатої на енергію сполуки - фосфоенолпірувату, але без безпосереднього гідролізу АТФ.
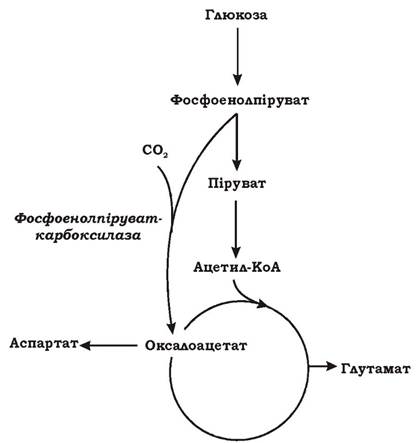
Рис. 5.28. Анаплеротична реакція Вуда - Веркмана
Гліоксилатний шунт - це одна з модифікацій ЦТК, функцією якої є синтез додаткової молекули ЩОК (рис. 5.29). Від звичайного ЦТК він відрізняється наявністю двох ферментів: ізоцитратліази та малатсинтетази. Ізоцитратліаза каталізує реакцію розщеплення ізоцитрату до сукцинату та гліоксилату. Малатсинтетаза бере участь у реакції конденсації додаткової молекули ацетил-КоА та гліоксилату з утворенням малату.
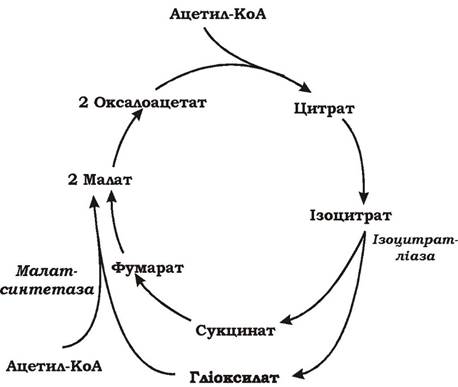
Рис. 5.29. Гліоксилатний шунт
Отже, у гліоксилатному шунті у процес включаються дві молекули ацетил-КоА і синтезується додаткова молекула ЩОК. Гліоксилатний шунт є у мікроорганізмів та рослин, але відсутній у тварин.