МІКРОБІОЛОГІЯ - М.Г. Сергійчук - 2008
Розділ 9. РОЛЬ МІКРООРГАНІЗМІВ У КРУГООБІГУ РЕЧОВИН У ПРИРОДІ
Кругообіг азоту
Запаси азоту у природі досить значні. Над площею 1 км2 земної поверхні міститься понад 8 млн т цього важливого елемента. Але в ситуації, коли рослини купаються в азоті, вони постійно відчувають його нестачу, подібно до того, як це буває з людиною, яка потрапила в океан і страждає від спраги.
У природі відбувається постійний кругообіг азоту, в якому беруть участь як мікроорганізми, так і тварини та виші рослини. Головна роль мікроорганізмів полягає в тому, що вони забезпечують мінералізацію відмерлих решток, переводячи азот органічних сполук у мінеральні форми: амонійні солі, солі азотної та азотистої кислот, аміак, молекулярний азот.
Мінеральні форми азоту входять в органічні речовини мікробної клітини та клітин рослинних організмів.
Кругообіг азоту (рис. 9.1) відбувається в декілька етапів (фаз), а оскільки це цикл, то не принципово, з якої фази розпочинати, тому для зручності розпочнемо його розгляд із процесу амоніфікації.
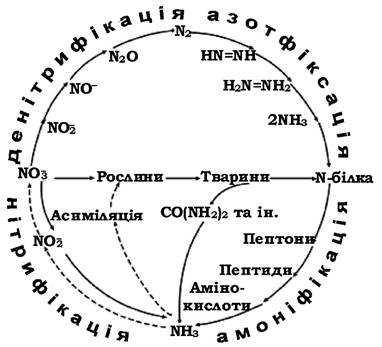
Рис. 9.1. Схема кругообігу азоту
Амоніфікація - це процес розкладу азотовмісних органічних сполук з утворенням аміаку (NH3). Цей процес називають також гниттям, а мікроорганізмів, що його викликають, - амоніфікаторами або гнильними.
Амоніфікації піддягають різні азотовмісні органічні сполуки: білки та їхні похідні (пептони, пептиди, амінокислоти); нуклеїнові кислоти та їхні похідні (пуринові та піримідинові основи); сечовина; сечова та гіпурова кислоти; гумусові сполуки; хітин.
Амоніфікуючу здатність проявляє більшість мікроорганізмів, які синтезують протеолітичні ферменти: Proteus vulgaris, Pseudomonas aeruginosa, P. fluorescens, Bacillus subtilis, B. mycoides, B. cereus, Clostridium tetani, C. perfringens, C. putrificum, C. sporogenes та інші бактерії, а також гриби.
Механізм процесу амоніфікації білків полягає у ферментативному їх гідролізі до пептонів, пептидів, апотім до амінокислот:
![]()
Амінокислоти, що утворилися у процесі розкладу білків, мінералізуються з різною швидкістю. Деякі з них (треонін, метионін) досить стійкі, інші (аргінін, триптофан) швидко розкладаються під впливом мікроорганізмів. Шляхи внутрішньоклітинної чи позаклітинної трансформації амінокислот різні. Можливі такі процеси:
а - окиснювальне дезамінування, яке каталізується специфічними оксидазами. При цьому утворюється NH3 і відповідна кетокислота, яка в подальшому трансформується в оксикислоту або альдегід, тобто не накопичується:
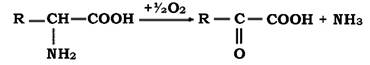
б - відновлювальне дезамінування проходить з утворенням відповідної органічної кислоти. Такі трансформації проходять за участю анаеробних мікроорганізмів:
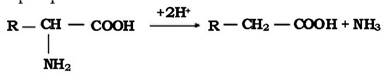
в - дезамінування, з утворенням NH3 і ненасичених кислот:
![]()
г - мікроорганізми можуть здійснювати також процес декарбоксилювання:
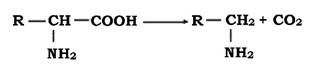
При анаеробному декарбоксилюванні амінокислот можуть утворюватися токсичні продукти, до яких належать диаміни, наприклад кадаверин і путресцин. Кадаверин утворюється при розкладі лізину, а путресцин - орнітину:
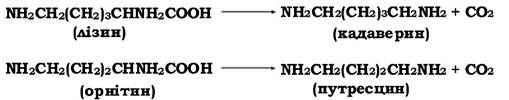
Сечовина теж належить до азотовмісних органічних сполук. Людина протягом доби виділяє приблизно 30 г цієї сполуки. Сечовина синтезується деякими грибами (наприклад, шампіньйони містять до 13 % за сухою масою сечовини). Ця сполука утворюється також при гідролітичному розщепленні аргініну під впливом аргінази:
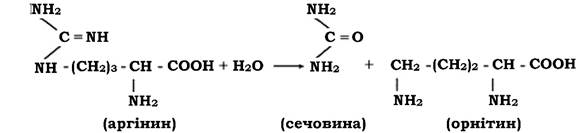
Протягом року на планеті живими організмами синтезується близько 35 млн т сечовини, яка у ґрунтах чи водоймах швидко розкладається під впливом мікроорганізмів, що синтезують уреазу, до вуглеаміачної солі, а оскільки це нестійка сполука, то вона швидко розкладається на складові частини:
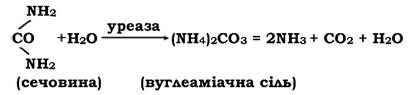
Мікроорганізми, здатні до деструкції сечовини, називаються уролітичними. Уперше в 1862 р. їх описав Л. Пастер. Вони виявляються у ґрунті, стічних водах, рубці жуйних тварин. Серед них є представники родів Micrococcus (M. urea), Bacillus (B. pasteurii), Sporosarcina (S. ureae). Ці бактерії здатні розвиватися в лужному середовищі при pH 9,0-10,0, що дає їм можливість гідролізувати значні кількості сечовини до аміаку.
Сечова кислота в невеликих кількостях (< 0,04 %) міститься в сечі. Вона може розкладатися багатьма групами мікроорганізмів. На перших етапах гідролізу утворюється тартронова кислота й сечовина:
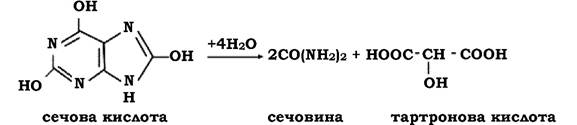
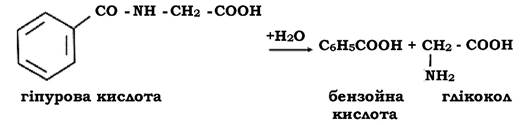
При гідролітичному розщепленні гіпурової кислоти утворюється бензойна кислота і глікокол, які можуть використовуватися мікроорганізмами як джерело вуглецевого та азотного живлення:
Хітин - азотовмісна сполука, полімер ацетилглюкозаміну. Ця сполука розкладається багатьма мікроорганізмами, оскільки хітин постійно виявляється у ґрунті. Він міститься в зовнішньому скелеті безхребетних тварин, у панцирних покривах комах, у клітинній стінці багатьох грибів.
Здатність до розщеплення хітину проявляють мікроорганізми, які синтезують фермент хітиназу. Цей фермент на початкових етапах розкладає хітин до хітобіози і хітотриози, які потім розщеплюються хітобіазою до оцтової кислоти, глюкози й аміаку.
Аміак, який утворюється у ґрунті чи воді, досить швидко окиснюється до солей азотистої, а потім азотної кислот. Цей процес отримав назву нітрифікації.
До робіт Л. Пастера накопичення нітратів у ґрунті пояснювалося як суто хімічний процес - окиснення аміаку атмосферним киснем. Ґрунту при цьому відводилася роль хімічного каталізатора. Пастер передбачив, що утворення нітритів - це мікробіологічний процес. Перші експериментальні підтвердження такого передбачення одержали Т. Шлезінг і А. Мюнц у 1879 р., але виділити мікроорганізми- нітрифікатори вдалося лише в 1890-1892 рр. С. Виноградському. З цією метою він запропонував принципово новий підхід - використання елективних середовищ. Цей підхід дав можливість відкрити в мікроорганізмів новий тип обміну речовин - хемосинтез. Характерною особливістю хемосинтетиків є їхня здатність отримувати енергію для синтезу органічної речовини із СО2 атмосфери при окисненні неорганічних речовин - амонійних солей.
С. Виноградський показав також, що процес нітрифікації проходить у два етапи, які викликаються різними групами мікроорганізмів. Одна група здійснює окиснення аміаку до азотистої кислоти - перша фаза процесу нітрифікації NО2-), інша група - до азотної кислоти (NO3-) - друга фаза.
До нітрифікаторів першої фази відносять представників п'яти родів: Nitrosomonas, Nitrosococcus, Nitrosospira, Nitrosolobus і Nitrosovibno. Єдиний представник, вивчений більш-менш достатньо, - Nitrosomonas europea. Сумарно перша фаза може бути представлена таким рівнянням:
![]()
Друга фаза - це окиснення азотистої кислоти до азотної:
![]()
До нітрифікаторів другої фази належать представники родів Nitrobacter, Nitrospira і Nitrococcus. Найкраще досліджено Nitrobacter winogradskii.
Нітрифікуючі бактерії розвиваються при pH 6,0-8,6, оптимум - 7,5-8,0. При pH менше 6,0 і більше 9,2 ці бактерії не розвиваються. Оптимальна температура розвитку нітрифікаторів - 25-30 оС. Але для деяких штамів оптимальною є температура в межах 26 оС або близько 40 оС, інші нормально розвиваються при температурі 4 оС.
Вважається, що умови для розвитку нітрифікуючих бактерій є сприятливими також для росту рослин. Це дає право вважати, що наявність активного режиму нітрифікації може бути одним із показників родючості ґрунту.
Здатність окиснювати аміак до нітритів і нітратів установлено і для деяких хемоорганогетеротрофних бактерій, наприклад представників родів Arthrobacter, Xanthomonas, Pseudomonas. Але інтенсивність гетеротрофної нітрифікації значно менша від автотрофної.
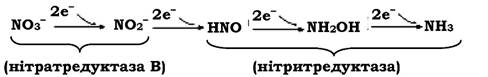
Нітрати, які утворилися у ґрунті в процесі нітрифікації, піддаються подальшим змінам: вони можуть бути використані рослинами; вимиватися у водойми; закріплюватися у клітинах мікроорганізмів, які використовують його як джерело азоту; відновлюватися мікроорганізмами до молекулярного азоту або аміаку. Останній процес отримав назву денітрифікації. Якщо відновлення нітратів супроводжується утворенням аміаку, то такий процес називають асиміляторною (асиміляційною) денітрифікацією (нітратредукцією). Цей тип денітрифікації виявляється як у рослин, так і у багатьох мікроорганізмів, він проходить поетапно, з утворенням проміжних продуктів (нітриту - NO2-; азотноватистої кислоти - HNO; гідроксиламіну - NH2OH). Перший етап реакції каталізується нітратредуктазою В. Синтез ферменту розпочинається, коли нітрат є єдиним джерелом азоту в середовищі. Нітрит, що утворився, трансформується за участю нітритредуктази до аміаку, тобто відновлення нітрату при асиміляторній денітрифікації відбувається поетапно:
При дисиміляторній денітрифікації нітрати виступають у ролі окиснювача органічної речовини, що забезпечує мікроорганізми необхідною енергією. Нітрати віддають свій кисень не відразу, а поетапно, тобто відновлення нітрату також є багатоступеневим процесом:
![]()
Здатність до дисиміляційної нітратредукції проявляють лише специфічні факультативно анаеробні бактерії. У ґрунтах переважають денітрифікатори родів Pseudomonas (P. aeruginosa, Р. fluorescens, P. stutzeri) і Paracoccus (P denitnficans), а також термофільні представники роду Bacillus. Ці та інші мікроорганізми використовують нітрати як акцептори водню у відсутності О2 для окиснення органічних речовин до кінцевих продуктів - СО2 і Н2О, а в аеробних умовах - це звичайні окиснювачі органічного субстрату. Існування денітрифікаторів в анаеробних умовах можуть забезпечувати також нітрити. Такі енергетичні процеси називають нітратним диханням. Наприклад, якщо в середовищі є моноцукри, то їх окиснення може бути подано таким чином:
![]()
Більшість денітрифікаторів - хемоорганотрофи. Вони потребують наявності в середовищі органічних сполук. Але відновлювати нітрати здатні також і деякі хемолітоавтотрофи. Наприклад, факультативно анаеробний сіркоокиснювач Thiobacillus denitnficans здатний розвиватися в анаеробних умовах, використовуючи нітрати як кінцевий акцептор водню. Як джерело енергії цей мікроорганізм використовує сірку або тіосульфат, трансформуючи їх до сульфату. Нітрат відновлюється до молекулярного азоту:
![]()
Схематично процес асиміляційної і дисиміляційної денітрифікації можна подати таким чином:
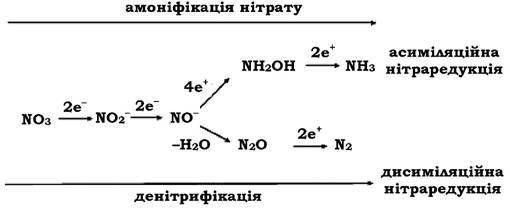
Як видно з наведених рівнянь, мікробіологічна денітрифікація супроводжується збідненням ґрунту мінеральними формами азоту. Щорічно в атмосферу повітря надходить із ґрунту близько 300 млн т N2. Але не варто розглядати цей процес лише як негативний, оскільки з глобального погляду він має вирішальне значення для збереження життя на планеті. У нормально аерованих ґрунтах нітрати є кінцевими продуктами. Вони добре розчиняються у воді, слабко поглинаються ґрунтовими частинками, а отже, добре вимиваються у водойми. Усе це могло б призвести до зниження вмісту молекулярного азоту в атмосфері повітря. Але N2, який надходить в атмосферу у процесі денітрифікації, зв'язується знову мікроорганізмами і йде на побудову органічної речовини, що становить наступний етап циклу азоту - азотофіксацію.
Азотофіксація здійснюється у природі двома шляхами: біологічним і небіологічним. Небіологічний шлях (наприклад, грозові розряди) дає приблизно 0,5 % у баланс, а загальна продуктивність азотофіксації становить ~ 300 млн т за рік.
У зв'язку з помітним збагаченням ґрунту зв'язаними формами азоту його фіксація привернула увагу багатьох учених. Ж. Бусенго в 1838 р. першим помітив, що конюшина й інші бобові рослини збагачують ґрунт азотом. Подібну закономірність у 1885 р. спостерігав і М. Бертело, який визначив, що після стерилізації ґрунту підвищення вмісту зв'язаних форм азоту припиняється. Згодом, у 1886-1888 рр., Г. Гельригель і Г. Вільфарт виявили зв'язок між фіксацією азоту і бульбочками на кореневій системі бобових. Бобові можуть рости у відсутності зв'язаних форм азоту лише в тому випадку, коли їхня коренева система має бульбочки (рис. 9.2).
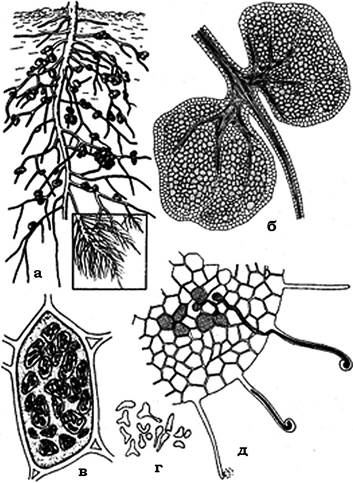
Рис. 9.2. Симбіотична фіксація азоту в кореневих бульбочках бобових:
а - корінь гороху з бульбочками; б - бульбочки в розрізі; в - рослинна клітина, заповнена бактеріями (Rhizobium); г - бактерії, які містяться у клітинах рослини, набувають незвичної форми (бактероїди, інволюційні форми); д - проникнення клітин бактерій через кореневі волоски і ріст інфекційної нитки
У 1888 р. М. Бейєринк зробив важливе відкриття: виділив у чистій культурі симбіотичний фіксатор N2, який був віднесений до роду Rhizobium. У 1893 р. С. Виноградський зробив нове відкриття: виділив із ґрунту анаеробний вільноживучий фіксатор N2 - Clostridium pasteurianum, а згодом, 1901 р., М. Бейєринк описав аеробний вільноживучий фіксатор N2 - Azotobacter chroococcum.
До 1949 р. здатність до фіксації молекулярного азоту приписувалась лише представникам родів Clostridium і Azotobacter. У 1949 р. у всіх діазотрофів було відкрито нітрогеназну систему, яка забезпечує відновлення ацетилену до етилену, тобто було встановлено зв'язок між фіксацією N2і відновленням ацетилену:
![]()
Крім молекулярного азоту та ацетилену, нітрогеназна система відновлює також азид, закис азоту, ціанід, нітрил і ізонітрил.
Застосування тесту на відновлення ацетилену дозволило встановити, що здатність до фіксації N2 проявляють також представники інших родів бактерій: Azomonas, Aerobacter, Achromobacter, Klebsiella, метаногенні бактерії, деякі синьозелені водорості та ін.
Представники роду Azotobacter належать до родини Azotobactenaceae. Клітини овальної форми діаметром 1,5-2,0 мкм, плеоморфні - від паличкоподібних до кулястих (рис. 9.3). Розташовуються поодиноко, парами або утворюють нехарактерні угруповання. Рухаються за допомогою перитрихальних джгутиків або нерухомі. Синтезують капсулу, яка оточує, як правило, дві клітини. У несприятливих умовах утворюють цисти (форма спокою). До роду Azotobacter належать A. chroococcum, A. a,gile, A. vinela,ndii. Оптимальне значення pH для їхнього розвитку 7,0-7,2, максимальне - 9,0. У ґрунтах із pH 5,6 майже не виявляються. Поширення і деякі характеристики представників роду Azotobacter наведено в табл. 9.1.
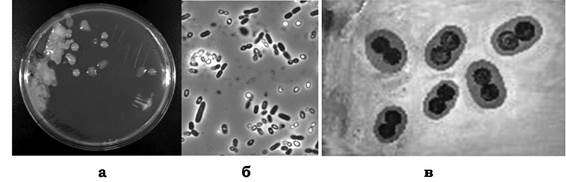
Рис. 9.3. Azotobacter chroococcum:
а - колонії A. chroococcum; б - трансформація паличкоподібних клітин у кокові форми; в - диплококи оточені капсулою
До родини Azotobactenaceae належить також рід Azomonas (A. agilis, A. insignus, A. macrocytogenes). Морфологічно представники цього роду подібні до Azotobacter. У процесі росту культура може виділяти багато слизу, але цист не утворює. Колонії на агаризованому середовищі безбарвні, деякі штами продукують флюорокуючі пігменти. Оптимальне значення pH для азотофіксації наближається до нейтрального, але деякі штами можуть фіксувати азот за pH 4,6-4,8. Виявляються у ґрунтах та водоймах.
Таблиця 9.1. Види роду Azotobacter та їх поширення
Вид |
Розмір, форма клітини та їх розташування |
Характеристика колоній |
Поширення |
A.chroococcum |
2,0 х 3,1 мкм; переважно шароподібна; парами |
Слизові; темнозабарвлені; містять цисти |
Ґрунти |
A. agile |
2,8 х 3,3 мкм; шароподібна, овальна; поодиноко і парами |
Виділяють жовтий пігмент з білою флуоресценцією |
Водойми каналів і канав |
A. vinelandii |
1,5 х 3,4 мкм; шароподібна, овальна; переважно парами |
Великі, слизові; виділяють жовтий пігмент із зеленою флуоресценцією; інколи містять цисти |
Ґрунти |
До аеробних грамнегативних паличок і коків належать також представники роду Beijerinckia (B. derxii, B. indica, B. mobilis). Клітини паличкоподібної форми, дещо зігнуті або грушоподібні, деякі мають тенденцію до галуження. Зустрічаються як рухомі, так і нерухомі клітини. Рухомі форми мають перитрихальний тип джгутикування. Утворюють капсули (оточують декілька клітин), деякі види утворюють цисти (оточують одну клітину). Ростуть у діапазоні pH від 3,0 до 9,510,0. При старінні культури колонії можуть набувати жовто- коричневого, бурштиново-коричневого, рижуватого або рожевого кольору. Виявляються у ґрунтах, особливо часто в тропічних широтах.
Бактерії, виділені з бульбочок бобових рослин, віднесено до роду Rhizobium (грец. rhizo - корінь) родини Rhizobiaceae. Вони виявляються частіше у ґрунтах, де ростуть бобові. Але можуть зустрічатися й у вільному стані як сапрофіти.
Морфологічно - це палички розміром 0,5-0,9х1,2-3,0 мкм, плеоморфні. Рухаються за допомогою єдиного полярного (субполярного) або перитри- хальних джгутиків (2-6 штук). Оптимальне pH 6,0-7,0. На агаризованих середовищах утворюють округлі, опуклі, напівпрозорі, слизові колонії. Характерною особливістю представників цього роду є їх здатність проникати в кореневі волоски бобових рослин і стимулювати утворення бульбочок, усередині яких бактерії містяться як внутрішньоклітинні симбіонти. У бульбочках бактерії мають вигляд плеоморфних форм - бактероїдів, які здійснюють фіксацію N2, трансформуючи його у зв'язану форму (аміак), доступну для використання рослиною-хазяїном. До роду Rhizobium належать: R. leguminosarum (R. leguminosarum biov. viceae, R. leguminosarum biov. tdfolii, R. leguminosarum biov. phaseoli), R. loti та R. meliloti.
У 1989 р. було описано рід бульбочкових бактерій Photorhizobium, представники якого проявляють здатність до симбіотичної азотофіксації й фотосинтезу. У 1990 р. описано ще один вид, віднесений до роду Rhizobium, - R. galegae, який функціонує в симбіозі з козлятником.
Усі симбіотичні азотофіксатори характеризуються такими ознаками, як специфічність, вірулентність і активність.
Специфічність - це властивість утворювати бульбочки на кореневій системі лише певних видів бобових рослин. Специфічність не має абсолютного характеру, але при неспецифічному інфікуванні утворюються, як правило, неактивні або малоактивні бульбочки.
Вірулентність - це здатність бульбочкових бактерій проникати через кореневі волоски в корінь рослини й утворювати бульбочки. Інколи бульбочкові бактерії можуть бути маловірулентними, тобто не заражають або погано заражають бобову рослину.
Активність бульбочкових бактерій визначається інтенсивністю азотофіксації, яка залежить від вмісту червоного пігменту - гемоглобіну, який називається в даному випадку леггемоглобіном, тобто - це гемоглобін бобових рослин, який міститься у вакуолях рослинних клітин. Він сприяє процесу засвоєння азоту, підтримуючи окисно-відновний стан на певному рівні. Леггемоглобін зумовлює рожеве забарвлення бульбочок. Такі забарвлені бульбочки і є активними. Бувають випадки, коли штам проявляє специфічність, є вірулентним, але не активний. У такому випадку бульбочки утворюються, але вони не здатні фіксувати N2. Ізоелектрична точка тканини бульбочки, утвореної активними культурами, лежить значно нижче (pH 3,0-4,0), ніж тканини бульбочки, яка утворилася під впливом неактивного штаму (pH 6,0-6,5).
Реально лише прокаріоти здатні зв’язувати азот атмосфери і будувати з нього всі азотовмісні органічні сполуки своїх клітин. Причина полягає в тому, що азот - це інертний елемент. Два атоми в його молекулі мають потрійний зв’язок. Для розриву одного з трьох зв’язків у його молекулі необхідно витратити близько 125 ккал на одну грам-молекулу азоту. Два інші зв’язки розриваються легше, витрати енергії при цьому становлять 63 і 37 ккал відповідно. Схема розриву зв’язків у молекулі азоту можна подати таким чином:
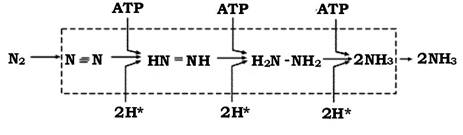
Потреби в АТФ в азотофіксувальних бактерій досить велика: для відновлення однієї молекули азоту витрачається 12 молекул АТФ. Функціонування нітрогеназної системи забезпечується не лише надходженням енергії, а й постійним потоком електронів для відновлення N2 до аміаку. Схему взаємозв'язків між процесами, які лежать в основі відновлення молекулярного азоту до аміаку, наведено на рис. 9.4.
Аміак, який утворився при фіксації N2, зв'язується кетокислотами, що супроводжується синтезом відповідних амінокислот (рис. 9.5).
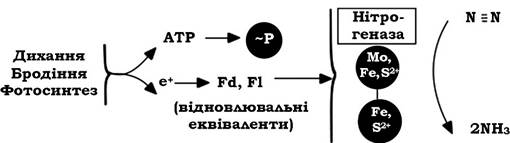
Рис. 9.4. Взаємозв'язок процесів, які лежать в основі фіксації молекулярного азоту:
Fd - ферредоксин; Fl - флаводоксин
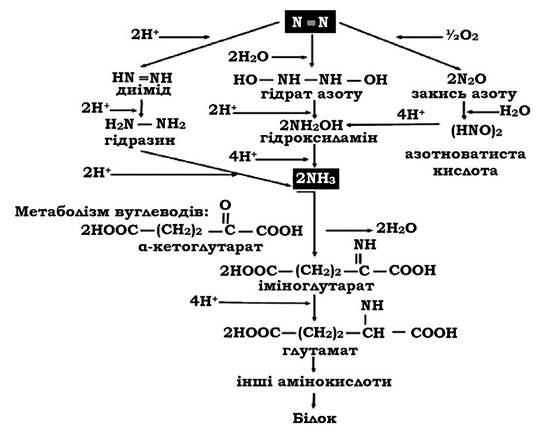
Рис. 9.5. Шляхи зв'язування молекулярного азоту