БИОХИМИЯ И МОЛЕКУЛЯРНАЯ БИОЛОГИЯ - В. ЭЛЛИОТ - 2002
ГЛАВА 14. ФОТОСИНТЕЗ - СПОСОБ ПЕРЕДАЧИ ЭНЕРГИИ ЭЛЕКТРОНАМ ВОДЫ
Образование ATP в аэробных клетках зависит от переноса электронов с веществ, обладающих высоким энергетическим потенциалом, вниз по энергетической шкале на кислород. Поскольку количество пищи на Земле ограничено, для продолжения жизни должен существовать какой-то способ «подъема» электронов на самый верх энергетической шкалы. Небольшая оговорка может быть сделана в отношении недавно открытых глубоководных морских организмов. Они обитают в районе разломов земной коры, где бьют горячие источники, богатые сероводородом (H2S). Сероводород - мощный восстановитель, поэтому его электроны могут транспортироваться по энергетическому градиенту с выделением энергии, которая может быть использована для генерации АТР в клетках при условии, что они снабжены соответствующим биохимическим аппаратом. Однако эти формы жизни могут существовать лишь до тех пор, пока сероводород и другие подобные ему вещества образуются в разломах земной коры. Для существования же громадного большинства других организмов необходим круговорот электронов. Это утверждение верно и в отношении любых ранних форм жизни в первичном океане. Какие бы виды готовых к употреблению пищевых веществ в нем ни содержались, экспоненциально размножающиеся организмы давно бы их использовали. По этой причине резервуары для «стока» электронов могли бы истощиться еще в анаэробной атмосфере, которая, как полагают, существовала до появления фотосинтеза.
Общие сведения
Фотосинтез - биологический процесс, осуществляющий кругооборот электронов. Он имеет несколько явных преимуществ:
✵ неисчерпаемость источника энергии - солнца;
✵ неисчерпаемость донора электронов - воды;
✵ выделяющийся кислород является неисчерпаемым резервуаром для стока электронов, позволяющим осуществлять высвобождение энергии из высокоэнергетических электронов пищевых молекул.
Весь этот перечень свидетельствует о том, что появление фотосинтеза было самым важным событием с момента возникновения жизни. Суть поддерживаемого фотосинтезом глобального энергетического цикла иллюстрирует рис. 14.1.
Рис. 14.1. Цикл переноса электронов, связывающего процессы фотосинтеза и окислительного фосфорилирования в живой природе (изображено схематично)
Ассимиляция СО2 представляет собой вторичный процесс по отношению к подъему электронов воды на высокий энергетический уровень
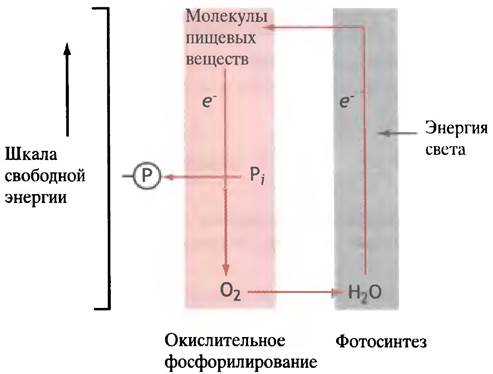
Вероятно, вы знаете, что при фотосинтезе СО2 и Н2О преобразуются в углеводы (обычно в моносахариды или крахмал). Общее уравнение, описывающее этот процесс, можно представить в виде:
6СО2 + 6Н2О —> С6Н12О6 + 6О2
∆G°′ = 2872 кДж • моль-1.
Чтобы синтезировать глюкозу из СО2 и Н2О, необходимо выполнение двух условий. Во-первых, нужно иметь восстанавливающий агент с достаточно низким редокс-потенциалом (с высокой энергией). При фотосинтезе таким восстановителем служит NADPH; при глюконеогенезе у животных восстановителем служит не NADPH, a NADH (см. главу 11). Во-вторых, должен быть доступен АТР как движущая сила синтеза. Именно на выполнение этих двух условий - переноса электронов с воды на NADP+ и синтеза АТР - расходуется поглощенная при фотосинтезе энергия света.
Место фотосинтеза - хлоропласт
Реакции фотосинтеза протекают в хлоропластах клеток зеленых растений. Подобно митохондриям, хлоропласта являются внутриклеточными органеллами, внешняя
мембрана которых проницаема для протонов, а внутренняя - нет. Как и митохондрии, хлоропласты имеют собственную ДНК. Она кодирует часть их белков, и собственный аппарат биосинтеза белков, который по своим свойствам подобен прокариотическому (см. с. 296). Считается, что хлоропласты - далекие потомки прокариотических фотосинтезирующих одноклеточных организмов, некогда вступивших в симбиоз с эукариотическими клетками.
В отличие от митохондрий, внутренние мембранные структуры хлоропластов - тилакоиды представлены замкнутыми уплощенными мембранными мешочками, уложенными в стопки - граны - и соединенными между собой мембранными выростами (ламеллами). Пространство внутри хлоропласта (без гран) называют стромой (рис. 14.2).
Рис. 14.2. Строение хлоропласта. Граны образованы стопками тилакоидов
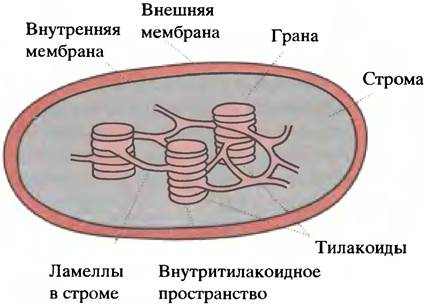
Хлорофилл (пигмент, улавливающий свет) и все переносчики электронов находятся в мембране тилакоидов, тогда как синтез углеводов из СО2 и Н2О происходит в строме. Синтетические процессы в хлоропласте называют темновыми, имея в виду, что они не приводятся в действие светом, хотя и происходят на свету, а являются следствием генерации NADPH и АТР в мембране тилакоидов. Распределение ролей между тилакоидами и стромой иллюстрирует рис. 14.3.
Рис. 14.3. Фотосинтетический процесс (изображено схематично)
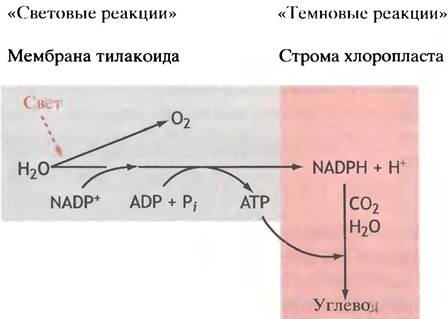
Фотосинтетический аппарат и его организация в тилакоидной мембране
Стоит вспомнить, как устроена цепь переноса электронов в митохондриях, потому что у нее много общего с фотосинтетическим аппаратом. Во внутренней мембране митохондрий находятся белковые комплексы четырех типов, между которыми перемещаются электроны, используя для этого подвижные переносчики: убихинон -низкомолекулярное жирорастворимое вещество - и цитохром с - небольшой водорастворимый белок.
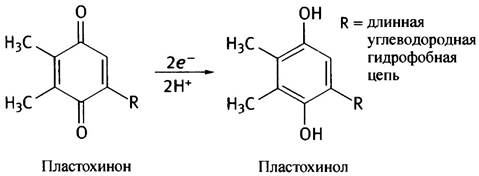
В тилакоидной мембране есть три типа комплексов (рис. 14.4). Первые два связываются диффундирующим переносчиком электронов - пластохиноном, похожим по структуре на убихинон, а второй и третий - небольшим водорастворимым белком пластоцианином, также участвующим в переносе электронов. Он содержит атом меди, который служит то донором, то акцептором электронов, и поэтому находится поочередно в состоянии Сu+ или Сu2+.
Рис. 14.4. Световая фаза фотосинтеза (схематично). Главная задача системы - передать электроны из воды на NADP+ и создать на тилакоидной мембране протонный градиент, достаточный для хемиосмотического синтеза АТР. Этот градиент создается благодаря расщеплению воды фотосистемой II и активному транспорту протонов комплексом цитохромов bf. Электроны доставляются от фотосистемы II к цитохромам bf с помощью пластохинона (Q). Все это похоже на цепь передачи электронов в митохондриях (где Q - убихинон). Пластоцианин (Рс), подобно цитохрому с в митохондриях, служит белковым переносчиком электронов, а ферредоксин расположен на противоположной стороне мембраны
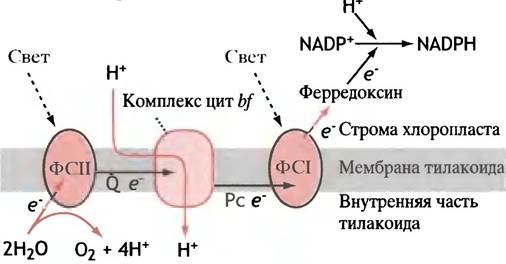
Эти три комплекса называются соответственно фотосистемой II (ФСII), комплексом цитохромов bf и фотосистемой I (ФСI). Пусть вас не смущает, что фотосистема II стоит в цепи раньше фотосистемы I - нумерация отражает всего лишь очередность их открытия. Функция всего этого аппарата заключается в осуществлении реакции:
2NADP+ + 2Н2O —> 2NADPH + 2Н+ + O2.
Реакция сопровождается очень большим увеличением свободной энергии. До сих пор мы рассматривали только такие эндоэргонические реакции, которые реализовывались за счет энергии, накопленной в виде химических связей. При фотосинтезе используется энергия света: на образование каждой молекулы NADPH расходуется энергия двух поглощенных фотонов. Этой энергии хватает на то, чтобы восстановить молекулы NADP+ водой, а излишек использовать на синтез АТР. Такой расклад позволяет полностью удовлетворить сформулированные выше два основных условия синтеза углеводов из СO2 и Н2O: наличие восстанавливающего агента и АТР. Теперь перейдем к рассмотрению механизмов улавливания энергии света фотосистемами II и I.
Что такое хлорофилл?
В зеленых растениях рецептором, воспринимающим свет, служит хлорофилл. В бактериях и водорослях есть другие светоулавливающие пигменты, но здесь мы ограничимся рассмотрением высших растений.
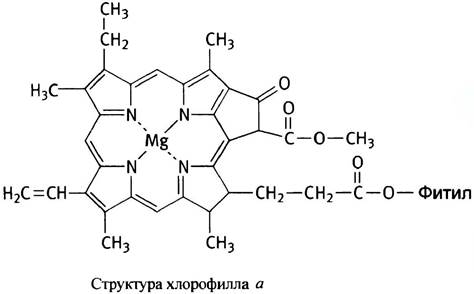
Хлорофилл представляет собой тетрапиррол, напоминающий по строению гем (см. главу 27). От гема его отличает природа центрального атома (магний вместо железа), а также строение боковых групп. Одна из этих групп в хлорофилле содержит длинную гидрофобную углеводородную цепь, которая служит якорем, удерживающим хлорофилл в липидном бислое. Как и гем, хлорофилл обладает системой сопряженных двойных связей, что определяет его интенсивную окраску. В растениях присутствуют два хлорофилла (a и b), различающиеся боковыми группами: в хлорофилле b вместо одной из боковых метальных групп присутствует альдегидная. Оба хлорофилла поглощают свет в голубой и красной областях видимого спектра (хотя максимумы поглощения слегка различаются) и отражают зеленый свет, что и придает этому пигменту и листьям растений соответствующую окраску.
Молекула хлорофилла, поглотив фотон, переходит в возбужденное состояние, сопровождающееся перемещением одного из электронов на более высокий энергетический уровень (он перепрыгивает на новую атомную орбиту). Однако возбужденная молекула нестабильна и стремится вернуться к исходному состоянию. В случае, когда фотон поглощается отдельной молекулой хлорофилла, эта энергия затем рассеется в виде тепла и света (флуоресценция), и ничего не произойдет. Если же молекулы хлорофилла упакованы плотно и упорядоченно, как в тилакоидной мембране, возбуждение передается соседним молекулам при помощи так называемого резонансного переноса энергии. В зеленых растениях молекулы хлорофилла упакованы в функциональные комплексы, называемые фотосистемами, поэтому область распространения энергии ограничена размерами этих комплексов (рис. 14.5).
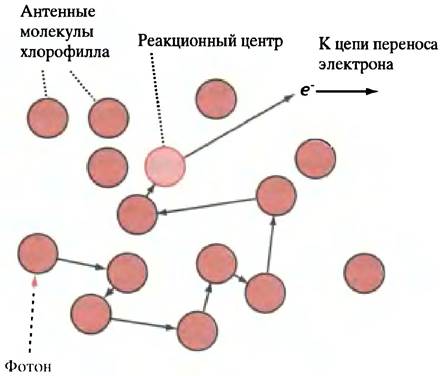
Рис. 14.5. Активация молекулы хлорофилла в реакционном центре. Реакционный центр представлен светлым кружком. Молекула хлорофилла в этом центре возбуждается благодаря резонансному переходу энергии от улавливающих квант света антенных молекул хлорофилла (темные кружки)
В каждой фотосистеме наряду с большим числом молекул «обычного» хлорофилла есть так называемые реакционные центры, которые содержат предположительно
две молекулы хлорофилла в комплексе с белками. В этих центрах у хлорофилла энергия возбужденного состояния невелика, так что ее резонансного переноса на свободные молекулы хлорофилла не происходит. Таким образом, реакционный центр представляет собой нечто вроде ловушки, в которую рано или поздно попадает энергия любого фотона, поглощенного любой «обычной» молекулой хлорофилла в пределах данной фотосистемы. Как только это происходит, электрон, находящийся на верхнем энергетическом уровне, передается акцептору, обладающему соответствующим редокс-потенциалом. Этот акцептор стоит в начале фотосинтетической цепи переноса электронов.
Итак, фотосистемы представляют собой сложные комплексы, состоящие из молекул хлорофилла, улавливающих свет, реакционного центра и цепи переноса электронов. Хлорофилл в составе реакционного центра фотосистемы II обозначают как Р680, а в составе фотосистемы I - Р700 (от англ. Pigment - пигмент; числа соответствуют длине волны максимума поглощения света в нм). Молекулы хлорофилла, закачивающие уловленную энергию в такие центры, называют антенными.
Механизм светозависимого восстановления NADP+
На рис. 14.6 изображена так называемая Z-схема двух фотосистем, демонстрирующая не только организацию цепи переноса электронов, но также редокс-потенциалы отдельных компонентов. Почему фотосистем две? Ответить на этот вопрос поможет следующая аналогия: чтобы питать трехвольтовую лампочку, нужны две последовательно включенные полуторавольтовые батарейки. При фотосинтезе восстановление NADP+ играет роль «нагрузки», а «батарейками» служат фотосистемы II и I.
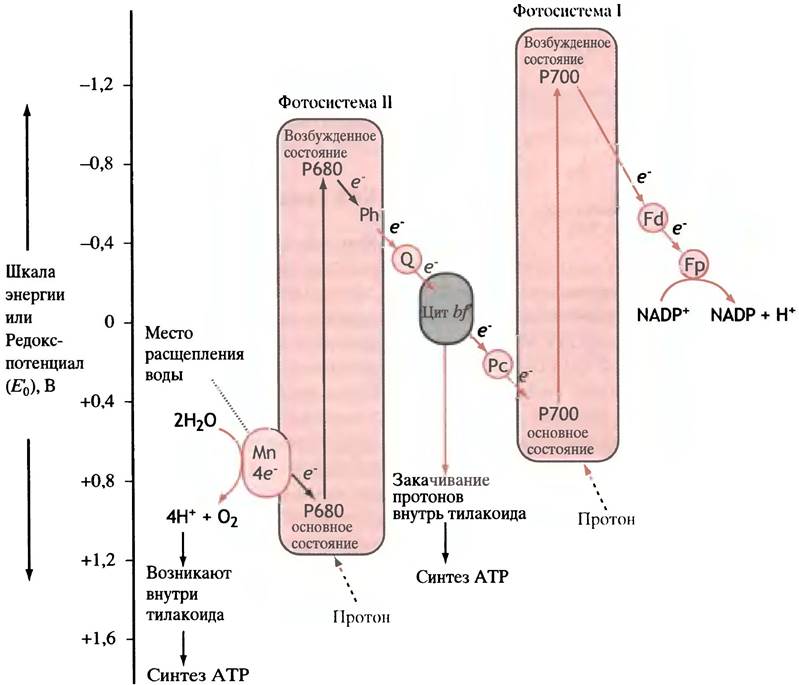
Рис. 14.6. Фотосинтез: перенос электронов от воды к НАОР+ (Z-схема). Анализ этого рисунка следует начать с переноса электрона от возбужденной молекулы Р680 к Р700. Р680 затем приобретает утраченный электрон от воды и ожидает нового акта возбуждения. Электрон, поступивший на Р700, после возбуждения молекулы передается на NАDР+. Рh - феофитин; Q - пластохинон; Рс - пластоцианин; Fd - ферредоксин; Fр - ферредоксин-NАDР-редуктаза
В действительности эти «батарейки» создают большую разность редокс-потенциалов, чем нужно для восстановления NADP+, и излишек расходуется на синтез АТР.
Начнем с хлорофилла Р680 в реакционных центрах фотосистемы II. В темноте он находится в основном (невозбужденном) состоянии, не проявляя никаких восстановительных свойств. Когда Р680 получает энергию фотона от антенного хлорофилла, он переходит в возбужденное состояние и стремится отдать возбужденный электрон, оказавшийся на верхнем энергетическом уровне. В результате этот электрон приобретает переносчик электронов фотосистемы II - феофитин. Это - пигмент; по своему строению он похож на хлорофилл, но не содержит Mg2+.
Две восстановленные молекулы феофитина последовательно отдают полученные электроны на восстановление пластохинона - растворимого в липидах переносчика электронов от фотосистемы II к комплексу цитохромов bf.
Последний состоит из двух цитохромов и железосерного центра. Он осуществляет перенос электронов от восстановленного пластохинона к пластоцианину.
Что же происходит с фотосистемой I? На хлорофилл Р700 в реакционном центре этой фотосистемы также стекает энергия фотона, уловленного антенным хлорофиллом, так что он становится мощным восстанавливающим агентом. Электрон с возбужденного хлорофилла Р700 передается по короткой цепочке переносчиков (на рис. 14.6 она для простоты не показана) на ферредоксин - водорастворимый белок стромы, содержащий электроноакцепторный кластер атомов железа. Именно ферредоксин с помощью FАD-зависимого фермента ферредоксин-NАDР+-редуктазы восстанавливает NАDР+ в NАDРН.
2Ферредоксинвосст + NАDР+ + 2Н+ —> 2Ферредоксинокисл + NАDРН + Н+.
Ясно, что обе фотосистемы, отдав по электрону, должны получить их обратно, чтобы вернуться в исходное состояние.
Иными словами, из восстановителей они переходят в ранг окислителей. Р700+ приобретает электрон у восстановленного пластоцианина:
Р700+ + РсСu+ —> Р700 + РсСu2+.
Что же касается фотосистемы II, то Р680+ возвращается в исходное состояние необычным образом: электрон он получает от воды!
Расщепление воды фотосистемой II
Р680+ очень сильный окислитель; его сродство к электрону даже выше, чем у кислорода, так что он вполне может извлечь электрон из воды. Чтобы превратить 2 молекулы воды в 4 протона (Н+) и O2, требуется отнять у них 4 электрона. При этом, как и при восстановлении O2 в митохондриях, необходимо избежать образования реакционноспособных промежуточных продуктов вроде перекиси водорода, крайне опасных для биологических систем. Эту задачу в фотосистеме II выполняет Мn2+-содержащий белковый комплекс (рис. 14.8, а), известный как водорасщепляющий центр, который отбирает электроны у воды, расщепляя ее на кислород и протоны, и передает их на Р680+, после чего последний готов к дальнейшим реакциям.
Как генерируется АТР?
Комплекс цитохромов bf, который использует пластогидрохинон для восстановления пластоцианина, похож на митохондриальный комплекс III (см. рис. 8.19) тем, что перенос им электронов сопряжен с трансмембранным транспортом протонов с внешней стороны тилакоидной мембраны вовнутрь. По аналогии с митохондриальным Q-циклом можно ожидать, что при этом внутрь тилакоида попадут четыре протона на каждую окисленную молекулу пластогидрохинона (см. с. 127). Однако такая стехиометрия не подтверждается экспериментальными данными. При расщеплении воды образуются также протоны внутри тилакоидов. Оба эти процесса (перенос протонов через мембрану и их образование внутри тилакоида) способствуют уменьшению pH внутри тилакоида до 4,5; на мембране тилакоида создается протонный градиент. Захват протона при восстановлении NADP+ ферредоксином в строме способствует поддержанию трансмембранного градиента.
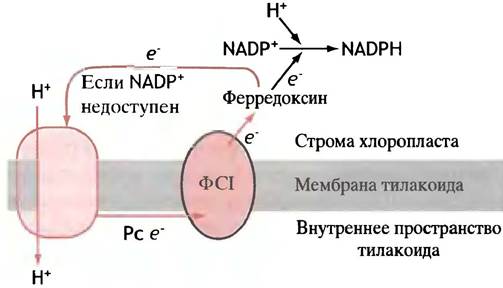
Таким образом, фотосинтетический аппарат включает в себя протонный насос. Этот насос создает на тилакоидальной мембране Н+-градиент, достаточный для хемиосмотического синтеза АТР из ADP и Рi. Работа протонного насоса не связана жестко с восстановлением NADP+. Если весь NADP+ восстановился в NADPH, ферредоксин отдает электроны цитохромному комплексу bf, а тот переносит их на пластоцианин. Такой перенос сопряжен с закачиванием протонов. Электроны при этом движутся по кругу: фотосистема I —> ферредоксин —> комплекс цитохромов bf —> пластоцианин —> фотосистема I (рис. 14.7). Поэтому такой вариант синтеза АТР называют циклическим фотофосфорилированием, управляемым циклическим током электронов.
Рис. 14.7. Циклический перенос электронов. Когда все молекулы NADP4 восстановлены, ферредоксин переносит электроны на комплекс цитохромов bf. Это приводит к интенсификации транспорта протонов и, следовательно, способствует синтезу АТР
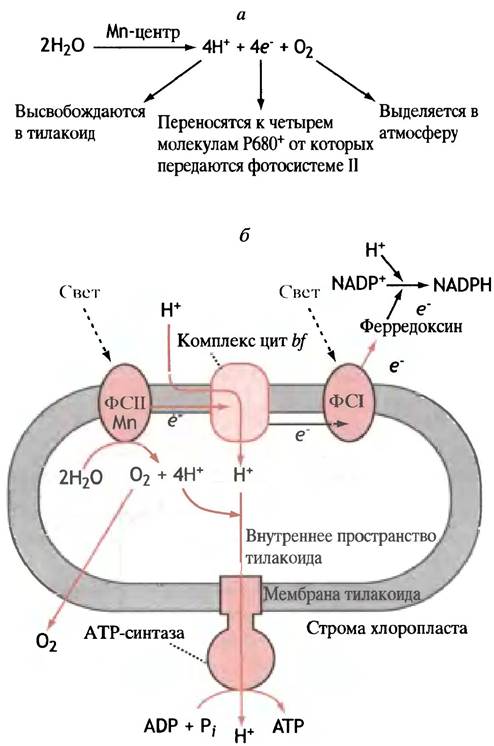
Полностью схема электронных и протонных потоков при фотосинтезе в хлоропластах представлена на рис. 14.8.
Рис. 14.8. Электронные и протонные потоки, происходящие внутри тилакоида (схематично) а - Суммарная реакция в Мn2+-содержащем центре; б - движение протонов и электронов
Почему протонный насос в митохондриях выкачивает протоны из матрикса в окружающую среду, а насос в тилакоидах закачивает их внутрь? Согласно одной из гипотез, как митохондрии, так и хлоропласты являются потомками прокариотических организмов, обитавших внутри эукариотических клеток. Поэтому направление активного транспорта протонов и ориентация протонной ATP-синтазы в мембране хлоропластов и митохондрий должны совпадать. Однако мембрана тилакоидов образуется отшнуровыванием впячиваний внутренней мембраны хлоропласта; следовательно, ее полярность противоположна, что объясняет, почему протонные градиенты и ATP-синтазы митохондрий и тилакоидов имеют противоположную ориентацию.
Как СO2 превращается в углеводы?
Среди всех рассмотренных биохимических процессов фотосинтез отличается тем, что восстановление NADP+ и синтез АТР происходят за счет энергии света.
Все дальнейшие химические превращения, в ходе которых образуется глюкоза и другие углеводы, свойственны лишь растениям и ничем принципиально не отличаются от обычных ферментативных реакций.
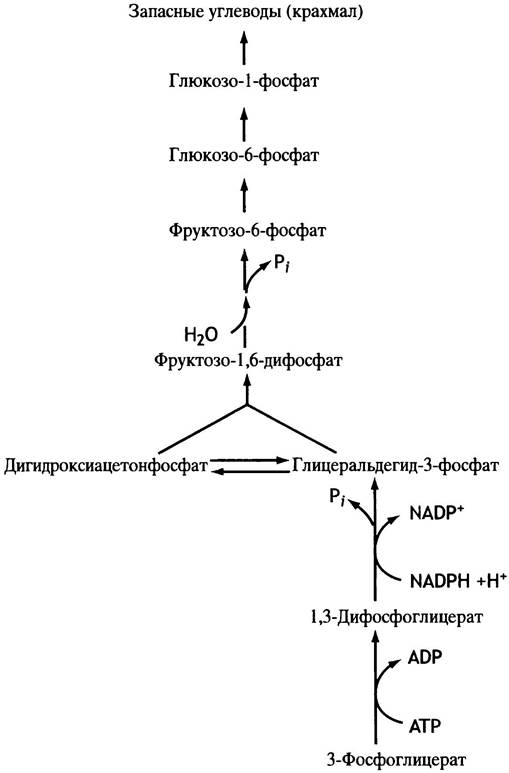
Ключевым метаболитом здесь является 3-фосфоглицерат, из которого затем углеводы синтезируются так же, как и в печени (см. рис. 11.5), с той лишь разницей, что восстановителем в этих процессах служит NАDРН, а не NАDН (рис. 14.9). Таким образом, проблема сводится к выяснению механизма образования 3-фосфоглицерата при фотосинтезе.
Рис. 14.9. Образование крахмала из 3-фосфоглицерата при фотосинтезе. Этот процесс сходен с глюконеогенезом, отличаясь лишь тем, что восстанавливающим агентом здесь служит NАDРН, а не NАDН. В отличие от синтеза гликогена, активированной формой глюкозы при получении крахмала служит АDР-глюкоза, а не UDР-глюкоза
Как образуется 3-фосфоглицерат?
Из всех ферментов самым распространенным на Земле является рибулозо-1,5-дифосфат-карбоксилаза, которую часто называют кратко «Rubisсо». Именно этот фермент использует СO2 для синтеза 3-фосфоглицерата.
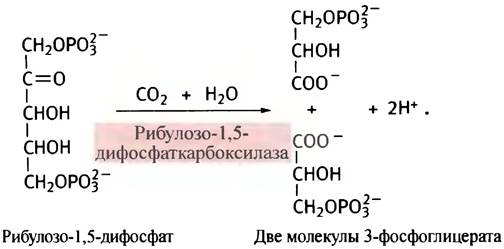
Напомним, что рибоза является альдопентозой, а рибулоза (ее оптический изомер) - кетопентозой. Карбоксилаза расщепляет рибулозо-1,5-дифосфат на 2 молекулы 3-фосфоглицерата, фиксируя при этом 1 молекулу СO2. Затем 3-фосфоглицерат превращается в разнообразные моносахариды.
Из чего синтезируется рибулозо-1,5-дифосфат?
Ответ, в принципе, очень прост. Из 6 молекул рибулозодифосфата (всего 30 С-атомов) и 6 молекул СO2 (6 С-атомов) образуются 12 молекул 3-фосфоглицерата (36 С-атомов). Две из них (2С3) направляются на синтез углеводов (С6), который протекает согласно схеме, показанной на рис. 14.9.
Оставшиеся 10 молекул фосфоглицерата (всего 30 С-атомов) преобразуются в 6 молекул рибулозодифос- фата (всего 30 С-атомов). Этот процесс достаточно сложен и сводится к различным превращениям С3-, С4-, С5-, С6- и С7-сахаров с помощью альдолазы и транс- кетолазы (см. с. 181; напомним, что транскетолаза переносит С2-блоки). В упрощенном виде происходящее можно описать следующей схемой:
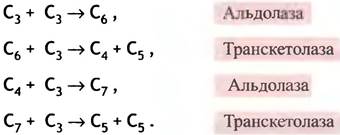
Суммарный результат: 5 С3 —> 3 С5.
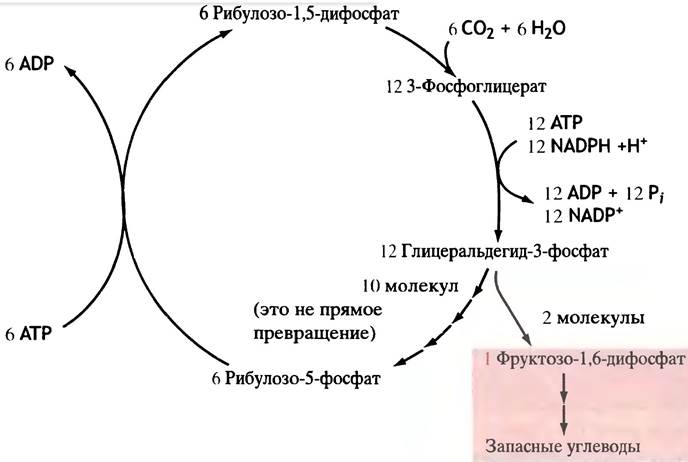
Итак, 6 молекул рибулозодифосфата, 6 молекул СO2 и 6 молекул Н2O преобразуются в 12 молекул фосфоглицерата; они превращаются в 6 молекул рибулозодифосфата и 1 молекулу фруктозо-6-фосфата, из которой затем могут быть образованы запасные углеводы, например, крахмал. Весь процесс в целом известен как цикл Кальвина (рис. 14.10). Суммарную реакцию описывает довольно громоздкое уравнение:
6СO2 + 18АТР + 12NАDРН + 12Н+ + 12Н2O —> С6Н12O6 + 18АDР +18Рi + 12NАDР+ + 6Н+.
Рис. 14.10. Реакции, входящие в цикл Кальвина (упрощенная схема). Здесь показана лишь стехиометрия превращений, но не их механизм
На чем споткнулась эволюция?
Химические процессы, протекающие в организме, настолько совершенны и эффективны, что кажется невероятным, чтобы эволюция споткнулась на едва ли не самом главном из ферментов - фиксирующей СO2 рибулозо-1,5-дифосфат-карбоксилазе.
На заре фотосинтеза в первичной атмосфере совсем не было кислорода, а содержание СO2 намного превышало нынешнее. Однако, благодаря фотосинтезу, содержание кислорода постепенно увеличивалось. Карбоксилаза реагирует не только с СO2, но и с кислородом. Эти две реакции конкурентны, так что фермент правильнее было бы называть рибулозо-1,5-дифосфаткар- боксилазой/оксигеназой. Реакция карбоксилазы с кислородом совершенно бесполезна, она приводит к бессмысленному расходу АТР (этот процесс называют фотодыханием).
На ярком свету, при достаточно высокой температуре воздуха фотосинтез в зеленом листе настолько интенсивен, что в его непосредственном окружении можно зарегистрировать падение уровня СO2 и увеличение содержания кислорода. В таких условиях и протекают реакции оксигенирования, которые могут на треть уменьшить усвоение СO2. В давние времена, когда уровень СO2 в атмосфере был существенно выше, чем уровень O2, оксигенирование не могло иметь места, но в настоящее время это не так.
Странно, что в ходе эволюции не происходило усовершенствования карбоксилазы. Возможно, тому есть неведомые нам причины, ибо трудно предположить небрежность в столь важном для судеб всего живого процессе. Известно, правда, что у некоторых растений существуют специальные приспособления, позволяющие поддерживать высокий уровень СO2 вокруг тех клеток, где функционирует карбоксилаза. Вследствие этого потери от оксигенирования сведены у них до минимума. К числу таких растений, произрастающих на ярком солнце и в теплом климате, относятся кукуруза и сахарный тростник.
С4-путь
Название С3-растения означает, что первым продуктом фотосинтеза, который удается обнаружить, используя меченый 14СО2, является С3-соединение - 3-фосфо- глицерат, образующийся при участии рибулозо-1,5-дифосфаткарбоксилазы. Однако у некоторых растений первичным продуктом фиксации атмосферного СO2 является оксалоацетат (рис. 14.11). Оксалоацетат содержит четыре атома углерода; отсюда другое название - С4-растения.
Рис. 14.11. С4-Путь, обеспечивающий повышенное содержание СO2 в фотосинтезирующих клетках. Механизм образования оксалоацетата из пирувата здесь коренным образом отличается от аналогичных процессов в животных клетках, где пируват никогда не превращается в фосфоенолпируват, а последний никогда не карбоксилируется. Кроме того, здесь для восстановления оксалоацетата используется не NАDН, а NАDРН
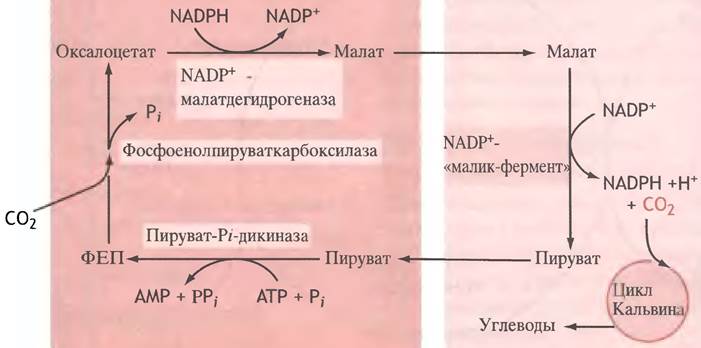
С3- и С4-растения различаются анатомическим строением своих листьев. У последних в мезофильных клетках на поверхности листа нет рибулозо-1,5-дифосфат-карбоксилазы, а фиксация СO2 у них происходит путем карбоксилирования фосфоенолпирувата. Эту реакцию катализирует фосфоенолпируват-карбоксилаза - фермент, не встречающийся у животных:
СO2 + Н2O + Фосфоенолпируват —> Оксалоацетат + Рi.
У этого фермента высокое сродство к СO2, так что никаких проблем с оксигенированием не возникает. Оксалоацетат затем восстанавливается в малат и транспортируется в клетки, где протекает фотосинтез. Там же малат декарбоксилируется так называемым малик-ферментом (см. с. 141), благодаря чему в клетках в 10-60 раз возрастает концентрация СO2:
Малат + NADP+ —> Пируват + СO2 + NADPH + Н+.
Ясно, что таким образом создаются условия для эффективной работы рибулозо-1,5-дифосфат-карбоксилазы. Образующийся пируват возвращается в мезофильные клетки, где перерабатывается пируватфосфатдикиназой снова в фосфоенолпируват. Эта реакция любопытна тем, что участвующий в ней АТР превращается не в ADP, а в АМР:
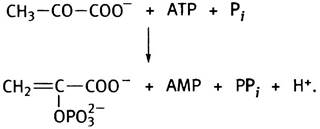
У животных превращение пирувата в фосфоенолпируват происходит совершенно иначе - через образование оксалоацетата (см. с. 148). Как только фосфоглицерат образуется в фотосинтезирующих клетках, он сразу вовлекается в цикл Кальвина.
С4-путь можно рассматривать как плату за полноценный фотосинтез, поскольку на синтез фосфоенолпирувата и транспорт кислот расходуется драгоценный АТР.
Тем не менее в жарком климате он сулит значительные преимущества. Во всяком случае, кукуруза и сахарный тростник - одни из главных поставщиков углеводов.
Отдельные биохимические реакции у С4-растений могут сильно различаться. Например, у некоторых видов первой С4-кислотой оказывается не малат, а аспартат. В таких растениях много аспартатаминотрансферазы вместо NАDР+-зависимой малатдегидрогеназы (малик-фермента; см. рис. 14.11). В фотосинтезирующих клетках С4-растений есть дополнительные декарбоксилазы С4-кислот. Две такие декарбоксилазы расположены не в цитоплазме, а в хлоропластах. Однако, какие бы механизмы ни использовались, цель одна - увеличить содержание СO2 в клетках, где работает рибулозо-1,5-дифосфат-карбоксилаза.
Вопросы к главе 14
1. Объясните, чем различаются «темновые» и «световые» реакции фотосинтеза.
2. Что означает выражение «антенный хлорофилл»?
3. Что означают термины «фотофосфорилирование» и «циклическое фотофосфорилирование»?
4. Для окисления воды требуются очень сильные окисляющие агенты. Что окисляет воду при фотосинтезе?
5. Протонный насос обусловливает транспорт электронов в фотосистеме II (ФСII) и обеспечивает движение протонов с внешней стороны тилакоидов внутрь. В митохондриях протонный насос работает в обратном направлении. Объясните почему.
6. Если растение на свету на очень короткое время поместить в атмосферу с радиоактивным 14СО2, метка сначала появляется в 3-фосфоглицерате. Почему?
7. Объясните, что такое цикл Кальвина.
8. Опишите биосинтетические реакции на пути от 3-фосфоглицерата до крахмала.
9. Фермент рибулозо-15-дифосфат-карбоксилаза (Rubisco) может реагировать и с кислородом, и с СO2. При низких концентрациях СO2 (при интенсивном солнечном свете) реакция оксигенации интенсифицируется. Как растения избегают оксигенирования под действием рибулозо-1,5-дифосфат-карбоксилазы?
10. В С4-растениях пиру ват перерабатывается в фосфоенолпируват с использованием ATR. Как это можно прокомментировать?