ОСНОВЫ БИОХИМИИ ЛЕНИНДЖЕРА - ТОМ 1. ОСНОВЫ БИОХИМИИ СТРОЕНИЕ И КАТАЛИЗ - 2011
ЧАСТЬ I. СТРОЕНИЕ И КАТАЛИЗ
7. УГЛЕВОДЫ И ГЛИКОБИОЛОГИЯ
Вопросы и задачи
1. Сахароспирты.
В сахароспиртах (производных моносахаридов) кислород карбонильной группы восстановлен до образования гидроксильной группы. Например, D-глицеральдегид можно восстановить до глицерина. Однако последний не обозначают с помощью букв D или L. Объясните, почему.
2. Распознавание эпимеров.
С помощью рис. 7-3 идентифицируйте эпимеры: а) D-аллозы, б) D)-гулозы и в) D-рибозы при С-2, С-3 и С-4.
3. Точка плавления озазонов — производных моносахаридов.
Многие углеводы реагируют с фенилгидразином (С6Н5МНNН2) с образованием ярко-желтых кристаллических производных, называемых озазонами:
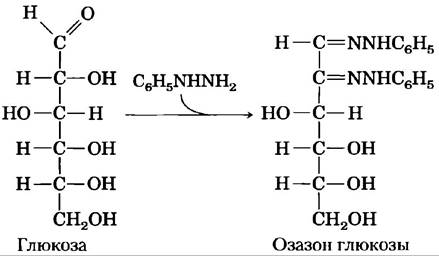
Температуру плавления этих веществ легко определяют и используют для характеристики каждого из них. Это свойство использовали при идентификации моносахаридов до появления высокоэффективной жидкостной хроматографии (ВЭЖХ) и газожидкостной хроматографии. Ниже приведены температуры плавления (ГПЛ) некоторых озазоновых производных альдоз.
Моносахарид |
ТПЛ моносахарида (°С) |
ТПЛозазона (°С) |
Глюкоза |
146 |
205 |
Манноза |
132 |
205 |
Галактоза |
165-168 |
201 |
Талоза |
128-130 |
201 |
Как видно из таблицы, определенные пары производных имеют одинаковые температуры плавления, хотя исходные моносахариды различались по этому параметру. Почему глюкоза и манноза, а также галактоза и талоза образуют озазоны с одинаковыми температурами плавления?
4. Взаимопревращения форм D-глюкозы.
Один стереоизомер моносахарида, раствор которого вращает плоскость поляризации света влево (против часовой стрелки), называется левовращающим и обозначается (-); второй стереоизомер, который вращает плоскость поляризации света вправо (по часовой стрелке), называется правовращающим и обозначается (+). Эквимолярные смеси обеих форм не вращают плоскость поляризации проходящего сквозь них света.
Оптическая активность стереоизомера количественно выражается в терминах оптического вращения, т. е. определяется числом градусов, на которое поворачивается плоскость поляризации света после прохождения через раствор с заданной концентрацией и заданной толщиной слоя. Удельное вращение ([а]25D°C) оптически активного вещества определяется по формуле:

При этом следует указывать температуру раствора и длину волны падающего света (обычно это D-линия Nа, т. е. 589 нм).
Свежеприготовленный раствор α-D-глюкозы имеет величину оптического вращения +112°. С течением времени оптическое вращение постепенно снижается и достигает равновесного значения = +52,5°. Напротив, свежеприготовленный раствор β-D-глюкозы характеризуется значением оптического вращения +19°. Оптическое вращение этого раствора со временем увеличивается и достигает того же равновесного значения.
а) Нарисуйте проекционные формулы Хеуорса для α- и β-форм D-глюкозы. В чем состоит основное различие между ними?
б) Объясните, почему при хранении раствора α-формы величина оптического вращения уменьшается? Почему растворы α- и β-форм D-глюкозы в одинаковых концентрациях постепенно приходят к одинаковому значению оптического вращения?
в) Рассчитайте процентное содержание обеих форм D-глюкозы в состоянии равновесия.
5. Конфигурация и конформация.
Какие связи в молекуле α-β-глюкозы должны быть разорваны, чтобы молекула приняла конфигурацию β-D-глюкозы? Какие связи нужно разорвать, чтобы превратить D-глюкозу в D-маннозу? Какие связи нужно разорвать, чтобы D-глюкоза из формы кресла перешла в другую конформацию?
6. Дезоксисахара.
Обладает ли D-2- дезоксигалактоза теми же химическими свойствами, что D-2-дезоксиглюкоза? Объясните свой ответ.
7. Структура сахаров.
Перечислите общие структурные черты и различия для каждой пары веществ: а) целлюлоза и гликоген; б) D-глюкоза и D-фруктоза; в) мальтоза и сахароза.
8. Восстанавливающие сахара.
Изобразите структурную формулу α-D-глюкозил-(1 —> 6)-D-маннозамина и укажите ту часть структуры, которая делает это вещество восстанавливающим сахаром.
9. Полуацетали и гликозидная связь.
Объясните различие между полуацеталем и гликозидом.
10. Вкус меда.
Фруктоза, входящая в состав меда, главным образом находится в виде β-D-пиранозы. Это один из самых сладких известных углеводов: сладость фруктозы в два раза превышает сладость глюкозы. Фруктоза в форме β-D- фуранозы гораздо менее сладкая. При нагревании меда его сладость постепенно снижается. Кроме того, кукурузный сироп с высоким содержанием фруктозы (коммерческий продукт, в котором большая часть глюкозы превращена во фруктозу) используют для придания сладости холодным, но не горячим напиткам. Какое химическое свойство фруктозы лежит в основе этих наблюдений?
11. Восстанавливающие дисахариды.
Дисахарид, являющийся либо мальтозой, либо сахарозой, обрабатывают раствором Фелинга. Образуется красная окраска. Какой дисахарид был в растворе? Объясните свой ответ.
12. Использование глюкозооксидазы для определения уровня глюкозы в крови.
Фермент глюкозооксидаза из плесневого гриба Pénicillium notatum катализирует окисление β-В-глюкозы до В-глюконо-δ-лактона. Этот фермент катализирует реакцию только p-апомера, но не влияет на α-аномер. Несмотря на эту специфичность, реакция с глюкозооксидазой обычно используется в клинической практике для определения общего содержания глюкозы в крови, представляющей собой смесь α- и β-глюкозы. Почему это возможно? Какие еще преимущества, кроме возможности определять низкие концентрации глюкозы, имеет глюкозооксидазный метод определения глюкозы по сравнению с методом Фелинга?
13. Инвертаза «инвертирует» сахарозу.
При гидролизе сахарозы (удельное оптическое вращение +66,5°) образуется эквимолярная смесь D-глюкозы (удельное вращение +52,5°) и D-фруктозы (удельное вращение -92°). (Определение оптического вращения см. в задаче 4.)
а) Предложите способ определения скорости гидролиза сахарозы с помощью фермента из клеток выстилки тонкой кишки.
б) Объясните, почему эквимолярная смесь D-глюкозы и D-фруктозы в пищевой промышленности носит название инвертированного сахара?
в) Раствор сахарозы (10%) обрабатывают ферментом инвертазой (теперь этот фермент часто называют сахаразой) до полного гидролиза. Каким будет оптическое вращение раствора в ячейке с длиной оптического пути 10 см? (Небольшим влиянием фермента можно пренебречь.)
14. Производство шоколада с жидкой начинкой.
Изготовление шоколада с жидкой начинкой можно рассматривать как интересное применение ферментов в пищевой промышленности. Ароматизированная жидкая начинка представляет собой главным образом водный раствор сахаров, обогащенный для сладости фруктозой. Существует техническая проблема: для приготовления шоколадной оболочки твердую (или почти твердую) центральную часть нужно окружить горячим расплавленным шоколадом, но в готовом продукте под твердой оболочкой должно находиться жидкое содержимое. Предложите способ решения этой задачи. (Подсказка: сахароза растворяется намного хуже, чем смесь глюкозы и фруктозы.)
15. Аномеры сахарозы.
Лактоза существует в виде двух аномеров, а вот аномерных форм сахарозы обнаружено не было. Почему?
16. Гентиобиоза.
Гентиобиоза (D-Glс (β —> 6) D-Glc) — это дисахарид, встречающийся в некоторых растительных гликозидах. Изобразите структуру этого соединения. Является ли это вещество восстанавливающим сахаром? Подвергается ли оно мутаротации?
17. Идентификация восстанавливающих сахаров.
Является ли N-ацетил-β-D-глюкозамин (рис. 7-9) восстанавливающим сахаром? А D-глюконат? Является ли восстанавливающим сахаром дисахарид GlсN (α1 ⇄ α1) GLс?
18. Расщепление целлюлозы.
Целлюлоза могла бы являться широкодоступным и дешевым источником глюкозы, но человек не способен ее переваривать. Если бы вам предложили провести определенную процедуру, которая дала бы вам эту возможность, вы бы согласились? Объясните свой ответ.
19. Физические свойства целлюлозы и гликогена.
Практически чистая целлюлоза, полученная из волокон, окружающих семена растений рода Gossypium (хлопчатник), представляет собой прочное, волокнистое и полностью нерастворимое в воде вещество. В отличие от целлюлозы гликоген, выделенный из мышц или печени, легко диспергируется в горячей воде, образуя мутный раствор. Несмотря на различие в физических свойствах, оба вещества построены из остатков D-глюкозы, соединенных 1 —> 4-связями, и имеют приблизительно одинаковые молекулярные массы. Какие особенности строения этих веществ объясняют различия в их физических свойствах? Какое биологическое значение имеют эти особенности двух полисахаридов?
20. Размеры полисахаридов.
Сравните между собой геометрические размеры молекул целлюлозы и амилозы, каждая из которых имеет молекулярную массу 200 000.
21. Скорость роста бамбука.
Стебли тропической травы бамбука в оптимальных условиях могут расти феноменально быстро — до 0,3 м/сут. Если принять, что стебли почти полностью состоят из целлюлозы, волокна которой ориентированы в направлении роста, какое число остатков сахара в секунду присоединяется к растущей целлюлозной цепи в ферментативной реакции при такой скорости роста? Длина каждого остатка D-глюкозы в молекуле целлюлозы составляет ~0,5 нм.
22. Гликоген как хранилище энергии: как долго могут лететь промысловые птицы?
Еще с древних времен было известно, что такие промысловые птицы, как куропатки, перепела и фазаны, очень быстро устают. Греческий историк Ксенофон писал: «Дрофу можно легко поймать, если ее внезапно вспугнуть, поскольку, подобно куропатке, она быстро устает и не может далеко улететь; ее мясо изумительно вкусно». Летательные мышцы промысловых птиц почти полностью обеспечиваются энергией (в форме АТР) за счет разложения глюкозо-1 -фосфата (см. гл. 14), который образуется при расщеплении накопленного в мышцах гликогена под действием фермента гликогенфосфорилазы. Скорость синтеза АТР ограничивается скоростью распада гликогена. В состоянии паники скорость распада гликогена у птиц очень высока и составляет примерно 120 мкмоль/мин глюкозо-1-фосфата в расчете на 1 г сырой ткани. Считая, что летательные мышцы содержат около 35% гликогена по весу, вычислите, как долго может лететь промысловая птица. (Среднюю молекулярную массу остатка глюкозы в гликогене считайте равной 160 г/моль.)
23. Относительная стабильность двух конформеров.
Объясните, почему две структуры, изображенные на рис. 7-19, так сильно различаются по уровню энергии (стабильности). Подсказка: см. рис. 1-21.
24. Объем, занимаемый хондроитинсульфатом в растворе.
Одной из важных функций хондроитинсульфата является смазка суставов, поскольку это вещество создает гелеобразную среду, препятствующую разрушению суставов от трения и уларов. Эта функция напрямую связана с известным свойством хондроитинсульфата: объем, занимаемый его молекулой в растворе, гораздо больше, чем в твердом состоянии. Почему так сильно увеличивается объем молекулы хондроитинсульфата в растворе?
25. Реакции гепарина.
Гепарин — гликозаминогликан с сильным отрицательным зарядом — используется в клинической практике в качестве антикоагулянта. Действие гепарина состоит в связывании некоторых белков плазмы, в том числе антитромбина III — ингибитора свертывания крови. Связывание гепарина с антитромбином III в соотношении 1:1 вызывает конформационные изменения в белке, которые значительно усиливают его ингибирующую способность. Какие аминокислотные остатки антитромбина III могут участвовать во взаимодействии с гепарином?
26. Трисахариды.
Как определить число три- сахаридов, которые можно составить из N-ацетилглюкозамин-4-сульфата (GlcNAc4S) и глюкуроновой кислоты (GlcA)? Изобразите 10 примеров.
27. Влияние сиаловой кислоты на электрофоретическую подвижность гликопротеинов.
Предположим, что у вас есть четыре формы белка с одинаковой аминокислотной последовательностью, но разным (ноль, одна, две и три) числом олигосахаридных цепей, каждая из которых заканчивается одним остатком сиаловой кислоты. Изобразите результаты разделения смеси четырех гликопротеинов в полиакриламидном геле в присутствии (см. рис. 3-18). Укажите, какому гликопротеину соответствует каждая полоса.
28. Информационное содержание олигосахаридов.
Углеводная составляющая некоторых гликопротеинов может служить для клетки участком узнавания. Для выполнения этой функции олигосахариды гликопротеинов должны иметь возможность существовать в большом разнообразии форм. Какая цепочка может существовать в большем количестве вариантов: олигопептид, состоящий из пяти различных аминокислотных остатков, или олигосахарид, построенный из пяти различных моносахаридных звеньев? Объясните свой ответ.
29. Определение степени разветвленности амилопектина.
Степень разветвленности (количество гликозидных связей α1 —> 6) в амилопектине можно определить с помощью следующей процедуры. Навеску амилопектина подвергают полному метилированию, т. с. обрабатывают метилирующим агентом (метилиодидом), замещающим все атомы водорода в гидроксильных группах сахара на метальные группы (-ОН —> -ОСН3). Затем все гликозидные связи подвергают кислотному гидролизу и определяют количество 2,3-ди- О-метилглюкозы.
а) Объясните смысл такой процедуры определения числа α1 —> 6 связей в молекуле амилопектина. Что происходит с остатками глюкозы в неразветвленных участках амилопектина при метилировании и гидролизе?
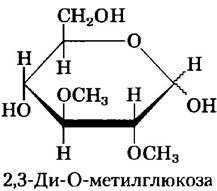
б) В результате подобной обработки из 258 г амилопектина было получено 12,4 мг 2,3-ди-О- метилглюкозы. Определите процентное содержание остатков глюкозы в амилопектине, участвующих в образовании α1 —> 6 связей. (Примите среднюю молекулярную массу остатка глюкозы в амилопектине равной 162 г/моль.)
30. Структурный анализ полисахарида.
Полисахарид с неизвестной структурой был выделен, подвергнут полному метилированию и гидролизу. Анализ продуктов выявил наличие трех метилированных сахаров, присутствующих в соотношении 20:1:1. Этими сахарами были 2,3,4-три-О- метил-D-глюкоза, 2,4-ди-О-метил-D-глюкоза и 2,3,4,6-тетра-O-метил-D-глюкоза. Определите структуру исходного полисахарида.
Анализ экспериментальных данных
31. Определение структуры антигенов групп крови ABO.
Система групп крови ABO у человека впервые была описана в 1901 г., а в 1924 г. было показано, что этот признак наследуется в виде единого генного локуса с тремя аллелями. В 1960 г. В. Т. Дж. Морган опубликовал работу, в которой суммировал все, что было известно об антигенах системы ABO. На момент публикации полная структура антигенов А, В и 0 еще не была известна; данная статья является примером, иллюстрирующим формирование научного знания.
При попытке определить структуру неизвестного биологического материала любой ученый сталкивается с двумя большими проблемами. Во-первых, если вы не знаете, что это за вещество, как вы можете быть уверены, что оно чистое? Во- вторых, если вы не знаете, что это за вещество, как вы можете быть уверены, что процесс выделения и очистки не изменит его структуры? Для ответа на первый вопрос Морган применил несколько методов. Один метод, описанный в его статье, заключается в «постоянстве аналитических значений при проверке фрактальной растворимости». В данном случае под «аналитическими значениями» понимаются измерения химического состава, точки плавления и др.
а) На основании ваших знаний о химических методах анализа предположите, что Морган понимал под «проверкой фрактальной растворимости».
б) Почему получаемые при такой проверке аналитические значения для чистого вещества являются постоянными, а для нечистого — нет?
Для ответа на второй вопрос Морган измерял иммунологическую активность веществ, присутствующих в различных образцах.
в) Почему для исследований Моргана, и особенно для ответа на второй вопрос, было важно, чтобы метод определения активности был количественным (определение уровня активности), а не качественным (определение наличия или отсутствия активности)?
Структура антигенов групп крови представлена на рис. 10-15. В своей статье Морган перечислял некоторые свойства антигенов А, В и 0, которые были известны на тот момент:
1. Антиген В содержит больше галактозы, чем антигены А и 0.
2. Антиген А содержит больше аминосахаров, чем антигены В и 0.
3. Соотношение содержания глюкозаминов/га- лактозаминов для антигена А равно 1,2, для антигена В 2,5.
г) Какие из заключений Моргана соответствуют современным данным о структуре антигенов А, В и 0?
д) Как вы объясните расхождения между предположениями Моргана и современными данными?
В более поздней работе Морган с сотрудниками использовал остроумный метод получения информации о структуре антигенов групп крови. Были обнаружены ферменты, специфическим образом разрушающие антигены. Однако они существовали только в виде грубых препаратов, возможно, содержавших примеси других ферментативных активностей. Разрушение антигенов групп крови под действием этих ферментных препаратов можно было предотвратить путем добавления в реакционную смесь определенных сахаров. Причем такое действие оказывали только те сахара, которые были найдены в структуре антигенов. Один ферментный препарат, выделенный из простейшего Trichomonas foetus, разрушал все три антигена, а его действие ингибировалось добавлением определенных сахаров. Результаты этих экспериментов сведены в представленной ниже таблице. Здесь показано, какое количество антигенов групп крови остается неизменным после обработки ферментом Т. foetus в присутствии сахаров.
Неизм |
мененный субстрат, % |
||
Добавленные сахара |
А антиген |
В антиген |
0 антиген |
Контроль(без сахара) |
3 |
1 |
1 |
L-Фукоза |
3 |
1 |
100 |
D-Фукоза |
3 |
1 |
1 |
L-Галактоза |
3 |
1 |
3 |
D-Галактоза |
6 |
100 |
1 |
N-Ацетилглюкозамин |
3 |
1 |
1 |
N-Ацетилгалактозамин |
100 |
6 |
1 |
В случае антигена 0 из сравнения контроля и эксперимента с добавлением L-фукозы видно, что L-фукоза ингибировала разрушение антигена. Это пример ингибирования конечным продуктом, когда избыток продукта реакции сдвигает равновесие реакции, предотвращая дальнейшее разрушение субстрата.
е) Хотя антиген 0 содержит галактозу, N-ацетилглюкозамин и N-ацетилгалактозамин, ни один из этих сахаров не ингибировал разрушения антигена 0. На основании этих данных установите, являлся ли ферментный препарат из Т foetus эндо- или экзогликозидазой? (Эндогликозидазы расщепляют связи между остатками в середине цепи, экзогликозидазы отщепляют по одному остатку от конца цепи.) Объясните свои рассуждения.
ж) Фукоза также присутствует в антигенах А и В. На основании структуры этих антигенов объясните, почему фукоза не предотвращала их расщепления ферментным препаратом.
з) Какие из результатов, приведенных в пунктах (е) и (ж), соответствуют структурам, представленным на рис. 10-15? Объясните свои рассуждения.