Биохимия человека Том 1 - Марри Р. 1993
Метаболизм белков и аминокислот
Биосинтез аминокислот
Биосинтез заменимых аминокислот
Из 12 заменимых аминокислот (табл. 29.1) 9 образуются из амфиболических метаболитов, а три (Cys, Туг и Нуl) — из незаменимых аминокислот.
Центральное место в биосинтезе аминокислот занимают глутаматдегидрогеназа, глутаминсинтаза и трансаминазы. Благодаря совместному действию этих ферментов катализируется включение неорганического иона аммония в а-аминогруппу аминокислот.
Глутамат
Восстановительное аминирование а-кетоглутарата катализируется глутаматдегидрогеназой (рис. 29.1). Помимо того что эта реакция приводит к образованию L-глутамата из амфиболического метаболита, а-кетоглутарата, она является ключевой стадией биосинтеза многих других аминокислот.
Глутамин
Биосинтез глутамина из глутамата катализируется глутаминсинтетазой (рис. 29.2). Данная реакция имеет как сходство с реакцией, катализируемой глутаматдегидрогеназой, так и отличия от нее. В обоих случаях «фиксируется» неорганический азот, который в одном Случае включается в аминогруппу, а в другом — в амидную группу. Обе реакции сопряжены с сильно экзергоническими реакциями: в случае глутаматдегидрогеназы с окислением NAD(P)H, а в случае глутаминсинтетазы с гидролизом АТР.
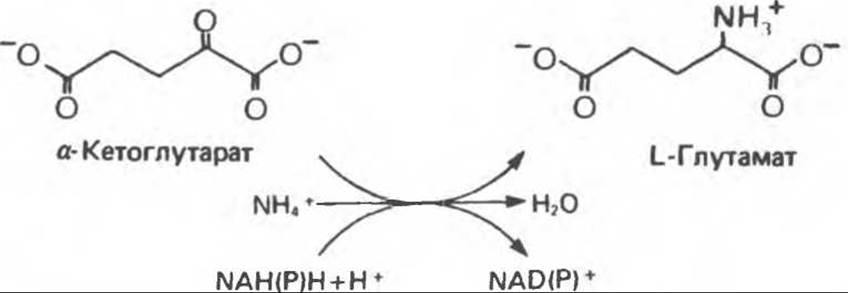
Рис. 29.1. Реакция, катализируемая глутаматдегидрогеназой. Восстановительное аминирование а-кетоглутарата ионами NH+3 происходит за счет NAD(P)H.

Рис. 29.2. Реакция, катализируемая глутаминсинтетазой.

Рис. 29.3. Образование аланина путем переаминирования пирувата. Донором аминогруппы может быть глутамат или аспартат. Другим продуктом реакции служит а- кетоглутарат или оксалоацетат.
Аланин и аспартат
L-аланин образуется из пирувата путем переаминирования с глутаматом, а L-аспартат — тем же путем из оксалоацетата (рис. 29.3). Перенос а-аминогруппы глутамата на амфиболические метаболиты иллюстрирует участие трансаминаз в процессах включения иона аммония в а-аминогруппы аминокислот.
Аспарагин
Образование аспарагина из аспартата, катализируемое аспарагинсинтетазой (рис. 29.4), сходно с синтезом глутамина (рис. 29.2). Аспарагинсинтетаза млекопитающих в качестве источника азота использует не ион аммония, а глутамин и, следовательно, не «фиксирует» неорганического азота. Бактериальные же аспарагинсинтетазы используют ион аммония, следовательно, «фиксируют» неорганический азот. Как и в случае других реакций, сопровождающихся образованием PPі, последующий гидролиз РРі, до Рі с участием пирофосфатазы обеспечивает энергетически благоприятные условия для протекания реакции.
Серин
Серин образуется из гликолитического промежуточного продукта D-3-фосфоглицерата (рис. 29.5). а-гидроксильная группа при участии NAD+ окисляется в оксогруппу; далее в результате переаминирования образуется фосфосерин, который затем дефосфорилируется, образуя серин.
Глицин
Синтез глицина в тканях млекопитающих осуществляется несколькими путями. В цитозоле печени содержится глицинтрансаминаза, катализирующая синтез глицина из глиоксилата и глутамата (или аланина). В отличие от большинства реакций переаминирования равновесие этой реакций сильно смещено в направлении синтеза глицина. Два важных дополнительных пути, функционирующие у млекопитающих, используют для образования глицина холин (рис. 29.6) и серин; в последнем случае катализ осуществляется серингидроксиметилтрансферазой (рис. 29.7).
Пролин
У млекопитающих и некоторых других организмов пролин образуется из глутамата путем обращения реакций катаболизма пролина (рис. 29.8).
Гидроксипролин
Поскольку пролин служит предшественником гидроксипролина, то обе аминокислоты рассматривают как принадлежащие к глутаматному семейству аминокислот. Хотя в тканях млекопитающих встречаются как 3-, так и 4-гидроксипролин, в последующем изложении. речь будет идти исключительно о транс-4-гидроксипролине.
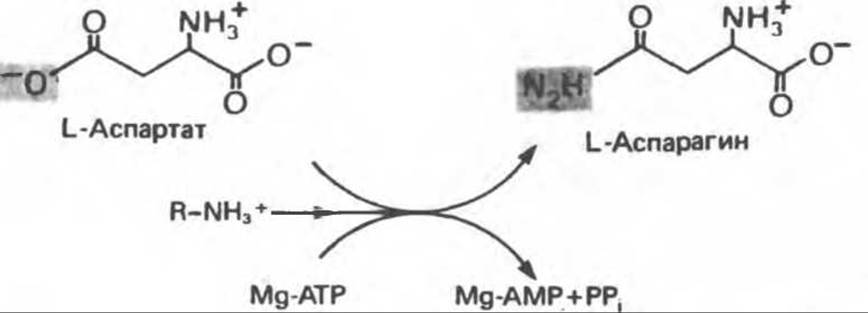
Рис. 29.4. Реакция, катализируемая аспарагинсинтетазой. Обратите внимание на сходство и различия с реакцией, катализируемой глутаминсинтетазой (рис. 29.2). Природа донора аминогруппы (R—NH+3) может различаться у разных организмов.
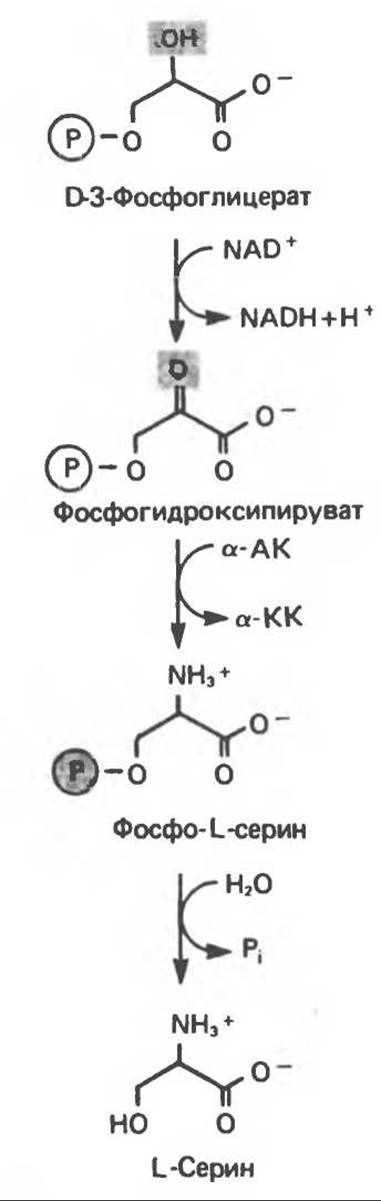
Рис. 29.5. Биосинтез серина. а-АК — а-аминокислота, аКК — а-кетокислота.
Гидроксипролин, как и гидроксилизин, содержится в тканях практически только в составе коллагена, на долю которого приходится большая часть белка в организме млекопитающих. В коллагене одна треть аминокислотных остатков приходится на глицин и еще одна треть на пролин и гидроксипролин. Гидроксипролин, представленный в коллагене весьма большим числом остатков, стабилизирует тройную спираль коллагена по отношению к действию протеаз. В отличие от гидроксилизина, гидроксильная группа которого служит местом присоединения остатков галактозы и глюкозы, гидроксильные группы гидроксипролина в коллагене остаются незамещенными.
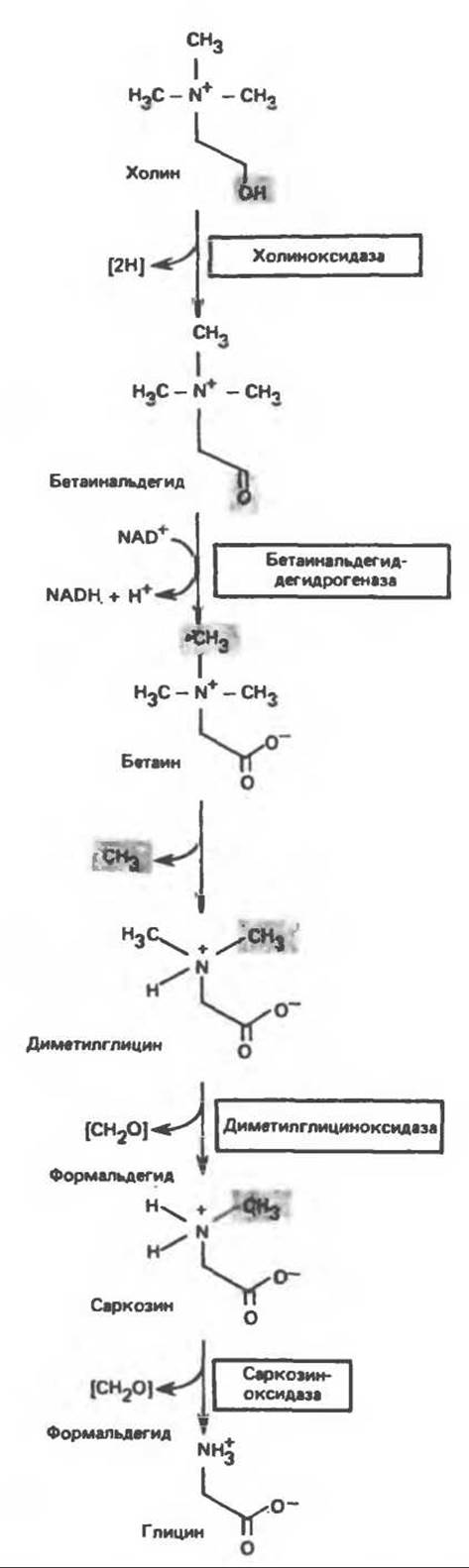
Рис. 29.6. Образование глицина из холина.
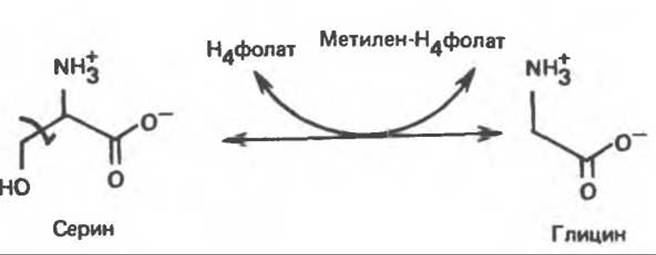
Рис. 29.7. Реакция, катализируемая серингидроксиметилтрансферазой. Реакция легко обратима. Н4 фолат — тетрагидрофолат.
Уникальной особенностью метаболизма гидроксипролина и гидроксилизина является то обстоятельство, что эти аминокислоты, входящие в состав белков пищи, не включаются в коллаген. Не существует тРНК, которая могла бы акцептировать гидроксипролин или гидроксилизин и далее включать их в растущую полипептидную цепь. В то же время пищевой пролин является предшественником гидроксипролина, а пищевой лизин — предшественником гидроксилизина в составе коллагена. Гидроксилирование пролина (или лизина) катализируется пролилгидроксилазой (или лизилгидроксилазой) — ферментами, находящимися в микросомальной фракции многих тканей (кожи, печени, легких, сердца, скелетной мышцы, гранулирующих раневых поверхностей). Эти ферменты являются пептидилгидроксилазами, поскольку гидроксилирование происходит только после включения пролина или лизина в полипептидную цепь (см. гл. 55).
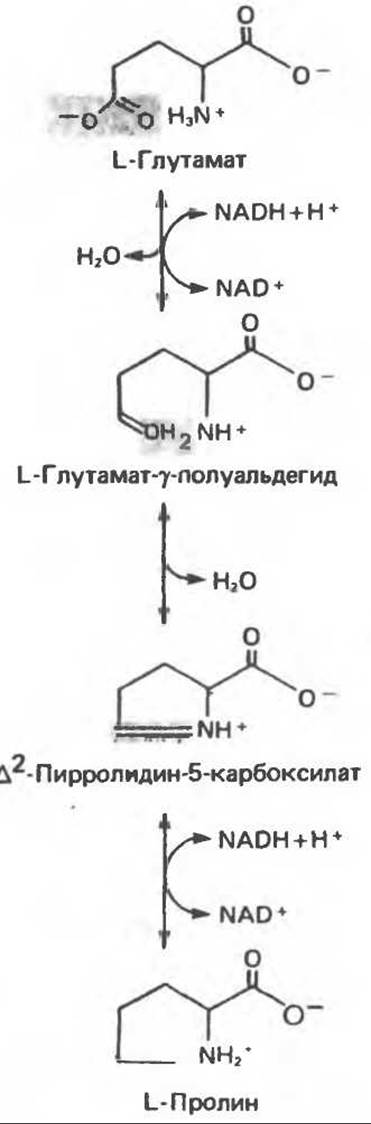
Рис. 29.8. Биосинтез пролина из глутамата путем обращения реакций катаболизма пролина.
Обе гидроксилазы являются оксигеназами со смешанной функцией и функционируют при участии молекулярного кислорода, аскорбата, ионов Fe+2 и а-кетоглутарата. Пролилгидроксилаза изучена более подробно; есть основания полагать, что лизилгидроксилаза действует аналогичным образом. На каждый моль гидроксилированного пролина декарбоксилируется I моль а-кетоглутарата с образованием сукцината. В ходе этого процесса один атом кислорода молекулы О2 включается в состав пролина, а другой — в сукцинат (рис. 29.9).
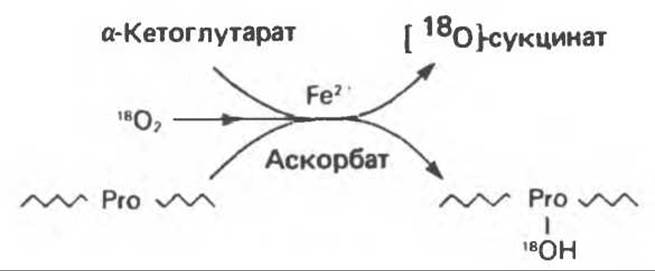
Рис. 29.9. Реакция, катализируемая пролил-гидроксилазой. Субстратом служит богатый пролином пептид. В результате реакции один атом молекулярного кислорода поступает в сукцинат, а другой — в пролин (установлено с использованием 18О2).
Цистеин
Цистеин, не относящийся к незаменимым аминокислотам, образуется из незаменимого метионина и заменимого серина. Сначала происходит превращение метионина в гомоцистеин с образованием на промежуточных стадиях S-аденозилметионина и S-аденозилгомоцистеина (см. гл. 31). Превращение гомоцистеина и серина в цистеин и гомосерин показано на рис. 29.10.
Тирозин
Тирозин образуется из фенилаланина в реакции, катализируемой фенилаланингидроксилазой (рис. 29.11), поэтому фенилаланин относится к незаменимым аминокислотам, а тирозин — нет (при условии, что диета содержит достаточное количество фенилаланина). Реакция необратима, и поэтому тирозин не может заменить пищевой фенилаланин. Фенилаланингидроксилазный комплекс является оксигеназой со смешанной функцией, она имеется в печени млекопитающих и отсутствует в других тканях. В результате реакции один атом молекулярного кислорода включается в пара-положение фенилаланина, а другой восстанавливается, образуя воду (рис. 29.11). Восстановительные эквиваленты, первоначально поставляемые NADPH, затем передаются непосредственно участвующему в реакции тетрагидробиоптерину — птеридину, подобному по структуре фрагменту фолиевой кислоты.

Рис. 29.10. Превращение гомоцистеина и серина в гомосерин и цистеин. Атом серы поступает в цистеин от метионина, углеродный скелет — от серина.
Гидроксилизин
5-Гидроксилизин (а, ε-диамино-δ-гидроксикапроат) входит в состав коллагена и отсутствует в большинстве других белков млекопитающих. Гидроксилизин в составе коллагена происходит из пищевого лизина, но не пищевого гидроксилизина. Перед гидроксилированием лизин должен включиться в пептидную цепь. Гидроксилирование остатка лизина в составе пептида катализируется лизилгидроксилазой — оксигеназой со смешанной функцией, аналогичной пролилгидроксилазе (рис. 29.9).
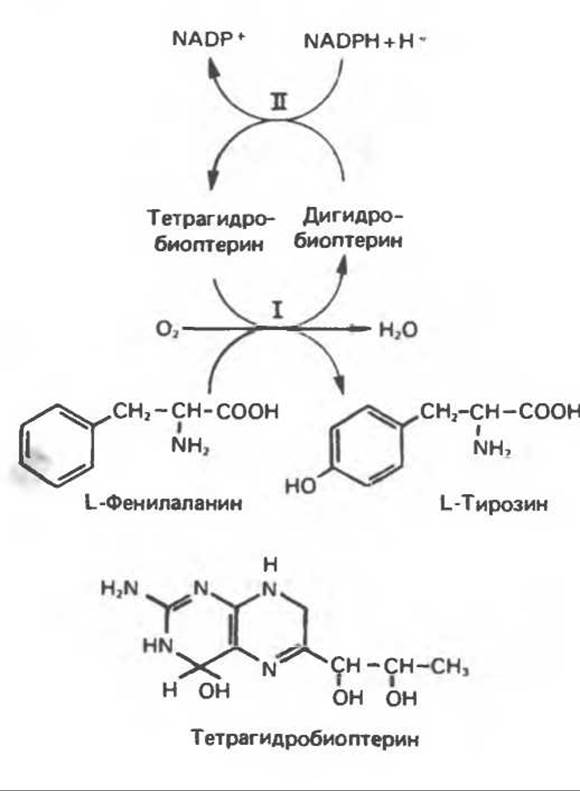
Рис. 29.11. Реакция, катализируемая фенилаланингидроксилазой. Она осуществляется с участием двух типов активности. Активность II катализирует восстановление дигидробиоптерина за счет NADPH, активность I — восстановление О2 в Н2О и превращение фенилаланина в тирозин. Нарушения хода этой реакции лежат в основе нарушений метаболизма фенилаланина, которые обсуждаются в гл. 31.