Биохимия человека Том 1 - Марри Р. 1993
Структура и функции белков и ферментов
Аминокислоты
Общие химические реакции
Карбоксильные и аминогруппы аминокислот вступают во все реакции, характерные для этих групп, т.е. в реакции образования солей, этерификации и ацилирования.
Цветные реакции
Нингидрин (рис. 3.5) осуществляет окислительное декарбоксилирование a-аминокислот с образованием СО2, NH3 и альдегида, содержащего на один атом углерода меньше, чем исходная аминокислота. Восстановленный нингидрин далее реагирует с высвободившимся аммиаком, образуя голубой комплекс с максимумом поглощения при Vmах = 570 нм. Образование этого окрашенного соединения используется в количественном тесте на а-аминокислоты, с помощью которого можно обнаружить аминокислоты, даже если их количество не превышает 1 мкг. Нингидрин реагирует не только с а-аминокислотами, но и с другими аминами; при этом тоже появляется голубая окраска, но без выделения СO2. Таким образом, выделение СO2 является индикатором участия в реакции а-аминокислоты. NH3 и пептиды тоже вступают в реакцию, но менее активно, чем а-аминокислоты. Продукт реакции между пролином (или 4-гидроксипролином) и нингидрином имеет желтую окраску.

Рис. 3.5. Нингидрин.
Таблица 3.3. L-a-аминокислоты, входящие в состав белков1)

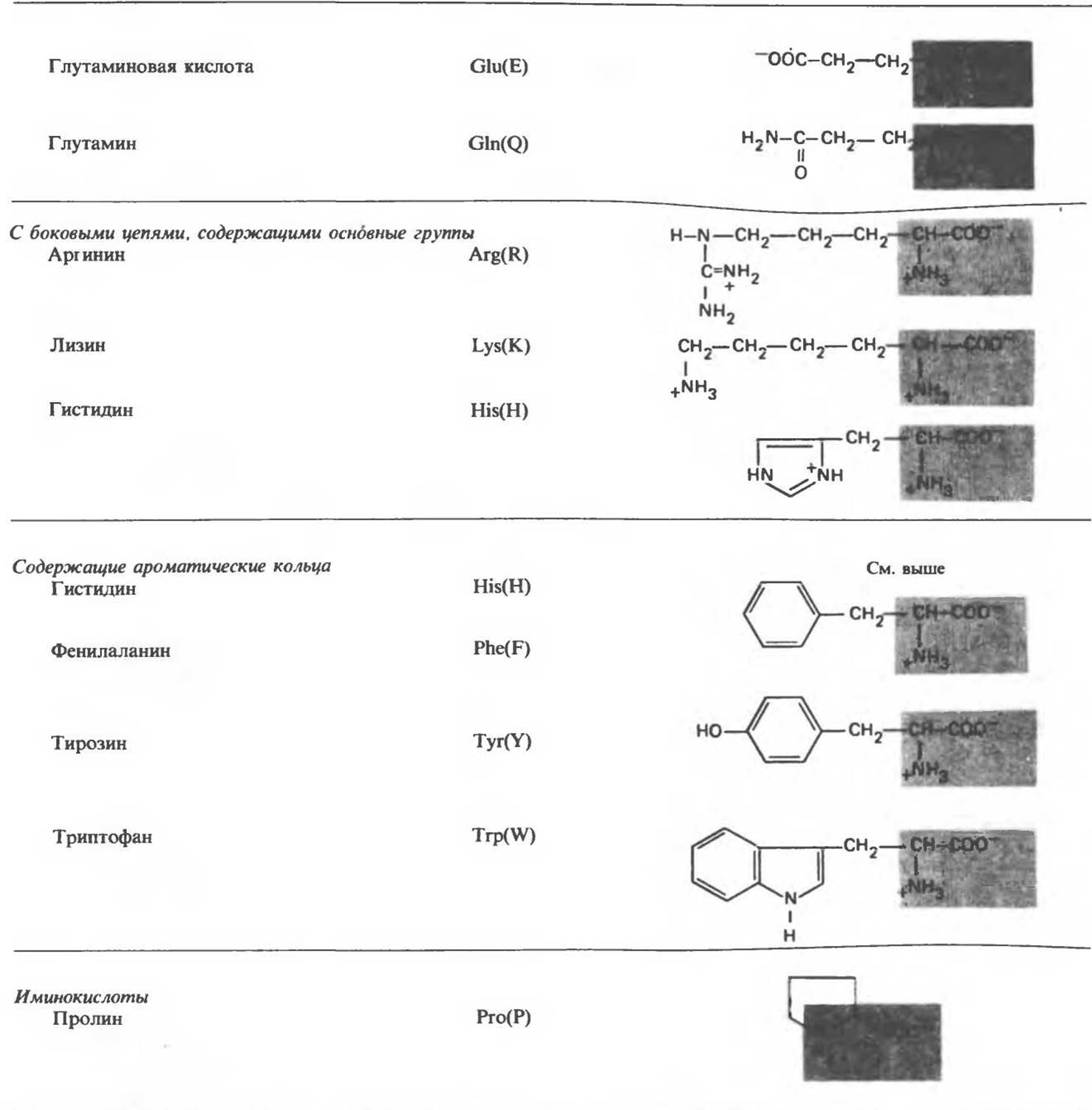
1) За исключением гидроксилизина (Hyl) и гидроксипролина (Hyp), которые включаются в полипептидную цепь в виде лизина и пролина, а затем гидроксилируются (см. гл. 29 и 54). Для всех перечисленных в таблице аминокислот имеются специфические тРНК, поэтому их включение в белок осуществляется под прямым генетическим контролем.
2) Цистин состоит из двух остатков цистеина, связанных дисульфидной связью:
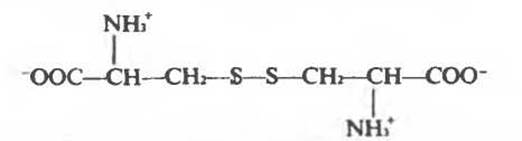
Таблица 3.4. Некоторые а-аминокислоты, не входящие в состав белков, но играющие важную роль в метаболизме
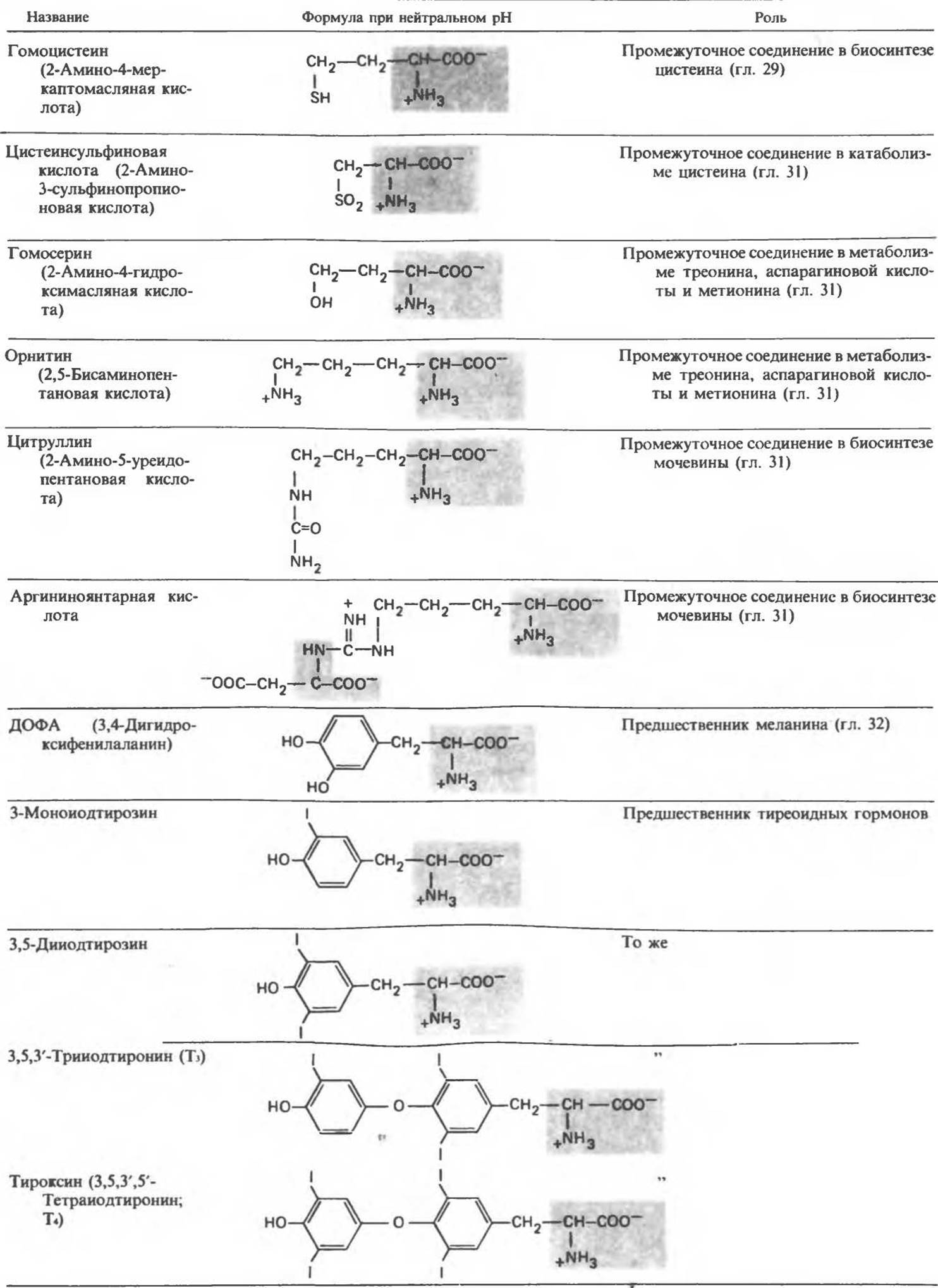
Таблица 3.5. Некоторые аминокислоты, не содержащие а-аминогрупп и играющие важную роль в метаболизме млекопитающих

Флуорескамин (рис. 3.6) является еще более чувствительным реагентом, позволяющим обнаруживать аминокислоты в количестве порядка нанограмм. Как и нингидрин, он образует комплекс не только с аминокислотами, но и с другими аминами.
Образование пептидных связей
Наиболее важной реакцией, в которой участвуют аминокислоты, является образование пептидных связей. При этом высвобождается одна молекула воды (рис. 3.7). Однако реакция осуществляется не так, как она представлена на рисунке, поскольку равновесие сильно сдвинуто в сторону гидролиза пептидной связи. Для образования пептидной связи между двумя аминокислотами карбоксильная группа должна быть предварительно активирована. Химический синтез осуществляется путем предварительного образования хлорангидрида. Биологическая активация включает взаимодействие с АТР.
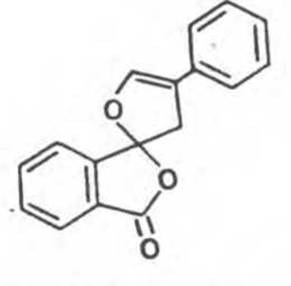
Рис. 3.6. Флуорескамин.
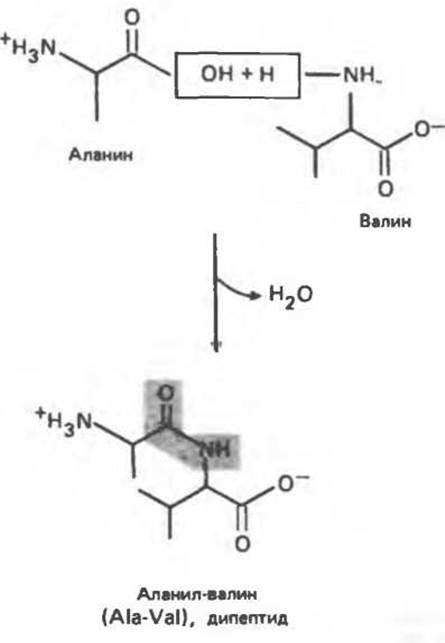
Рис. 3.7. Соединение аминокислот пептидной связью (затененная область).