Биохимия человека Том 1 - Марри Р. 1993
Структура и функции белков и ферментов
Ферменты: общие свойства
Коферменты
Многие ферменты оказывают каталитическое действие на субстраты только в присутствии специфического термостабильного низкомолекулярного органического соединения — кофермента. В таких случаях холофермент (каталитически активный комплекс) состоит из апофермента (белковая часть) и связанного с ним кофермента. Кофермент может быть связан с апоферментом ковалентными или нековалентными связями. Термин «простетическая группа» относится к ковалентно связанному коферменту. К числу реакций, требующих присутствия коферментов, относятся окислительно-восстановительные реакции, реакции переноса групп и изомеризации, а также реакции конденсации (по системе IUB это классы 1, 2, 5 и 6). Реакции расщепления, например гидролитические реакции, катализируемые пищеварительными ферментами, протекают в отсутствие кофермента (по системе IUB это классы 3 и 4).
Коферменты как вторые субстраты
Кофермент можно рассматривать как второй субстрат, или косубстрат, по двум причинам. Во-первых, в ходе реакции кофермент претерпевает химические изменения, в точности противоположные изменениям, которые происходят в субстрате. Например, в окислительно-восстановительных дегидрогеназных реакциях молекула субстрата окисляется, а молекула кофермента восстанавливается (рис. 7.1).
Подобным же образом в реакциях переаминирования пиридоксальфосфат выступает как второй субстрат в двух сочетанных реакциях и как переносчик аминогруппы между различными а-амино- и а- кетокислотами.

Рис. 7.1. Пример окислительно-восстановительной реакции, в которой NAD+ выступает в роли косубстрата.
Вторая причина, по которой кофермент можно считать равноправным участником реакции, заключается в том, что именно его участие может иметь фундаментальное физиологическое значение. Например, работа мышцы в анаэробных условиях сопровождается превращением пирувата в лактат. Но в этом случае важны совсем не лактат и не пируват: предназначением реакции является превращение NADH в NAD+. В отсутствие NAD+ гликолиз продолжаться не может и анаэробный синтез АТР (а следовательно, и работа мышцы) прекращается. Восстановление пирувата до лактата в анаэробных условиях обеспечивает окисление NADH в NAD+, необходимый для синтеза АТР. Функцию образования NAD+ могут выполнять и другие реакции. Значение этого процесса становится очевидным, если перейти от животных к другим формам жизни. У бактерий и дрожжей, растущих в анаэробных условиях, вещества, образующиеся из пирувата, служат окислителями для NADH, при этом сами они восстанавливаются (табл. 7.1).
Таблица 7.1. Системы анаэробной регенерации NAD+
|
Окислитель |
Восстановленный продукт |
Организмы, ткани |
|
Пируват |
Лактат |
Мышцы, гомоферментативные молочнокислые бактерии |
|
Ацетальдегид |
Этанол |
Дрожжи |
|
Дигидроксиацетонфосфат |
а-Глицeрофосфат |
Е. coli |
|
Фруктоза |
Маннитол |
Гетероферментативные молочнокислые бактерии |
Роль коферментов как переносчиков групп на промежуточных стадиях метаболизма
Биохимические реакции переноса можно представить в виде
D—G + А ⇄ A—G + D.
Здесь функциональная группа G переносится от молекулы донора, D—G, на молекулу акцептора А. Кофермент в этом случае может выступать либо как конечный акцептор (в реакциях отщепления водорода), либо как промежуточный переносчик (в реакциях переаминирования). Эту вторую функцию можно проиллюстрировать следующим образом:

На этой схеме показан только один комплекс (СоЕ—G), но может участвовать и несколько таких промежуточных комплексов.
Если переносимой группой является атом водорода, то обычно указывают лишь левую полуреакцию:
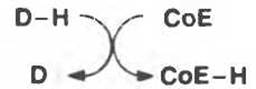
Реакции переноса водорода, протекающие в живых клетках (табл. 7.1), идут по схеме

Можно предложить следующую классификацию коферментов:
Коферменты, участвующие в переносе любых групп, кроме атомов водорода:
Сахарофосфаты
CoASH
Тиаминпирофосфат
Пиридоксальфосфат
Фолиатные коферменты
Биотин
Кобамидные (В12) коферменты
Липоевая кислота
Коферменты, участвующие в переносе атомов водорода:
NAD/NADP+
FMN, FAD
Липоевая кислота
Кофермент Q
Коферменты — производные витаминов группы В и АМР
Витамины группы В входят как составная часть во многие коферменты. Например, ферменты, участвующие в метаболизме аминокислот, нуждаются в коферментах — производных витамина В6. Витамины группы В — никотинамид, тиамин, рибофлавин и пантотеновая кислота — являются компонентами коферментов, участвующих в процессах биологического окисления и восстановления, а коферментные формы фолиевой кислоты и кобамида участвуют в переносе одноуглеродных фрагментов.
Структурным компонентом многих коферментов является адениновое кольцо, соединенное с D-рибозой и неорганическим фосфатом. Эти коферменты можно рассматривать, следовательно, как производные аденозинмонофосфата (АМР) (см. табл. 34.1). Структурные формулы NAD+ и NADP+ приведены на рис. 7.2.