Биохимия аминокислот - А. Майстер 1961
Промежуточный обмен аминокислот
Триптофан
Прочие продукты обмена триптофана
У ряда бактерий распад триптофана происходит путем триптофаназной реакции с образованием индола, пировиноградной кислоты и аммиака:
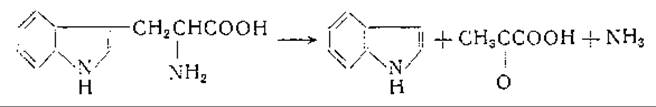
Эта реакция, впервые обнаруженная Гопкинсом и Колом [862], была детально изучена другими авторами [863, 864]. Вуд и сотрудники [865] получили из Е. coli препараты фермента, осуществляющего это превращение, и показали, что его коферментом является пиридоксальфосфат. Для реакции, по-видимому, необходимо присутствие ионов калия, аммония и, возможно, железа [866, 867]. Снелл и сотрудники [731] предположили, что механизм этой реакции заключается в отщеплении боковой цепи от комплекса, состоящего из пиридоксаля, триптофана и металла:

При распаде индола у некоторых бактерий наблюдается образование индоксила, индикана, индиго и индирубина. Эти соединения найдены в нормальной моче человека. Полагают, что они образуются бактериями кишечной флоры [881—883].


Фиг. 19. Сводная схема превращений триптофана.
Высказано предположение, что некоторые бактерии могут разлагать индол путем следующего ряда реакций [884]:
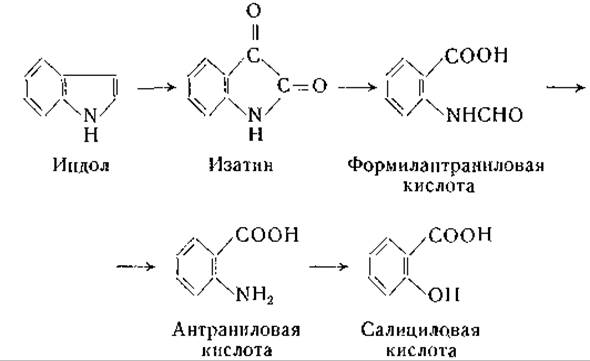
По-видимому, молекулы некоторых алкалоидов (грамин, эзерин, стрихнин, цинхонин, эметин и др.) образуются частично из триптофана; их биогенезу посвящены многочисленные исследования [885—888]. Ван-Тамелен [889] в интересной статье обсуждает взаимоотношения между 5-окситриптофаном и лизергиновой кислотой.
В опытах с никотиновой кислотой, меченной тритием в ядре, и с препаратом С14-никотиновой кислоты недавно показано, что эта кислота служит предшественником никотина в табачном растении [1131].