Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Типы реакций, катализируемых ферментами
Реакции нуклеофильного замещения (реакция типа 1)
Механизм реакций двойного замещения
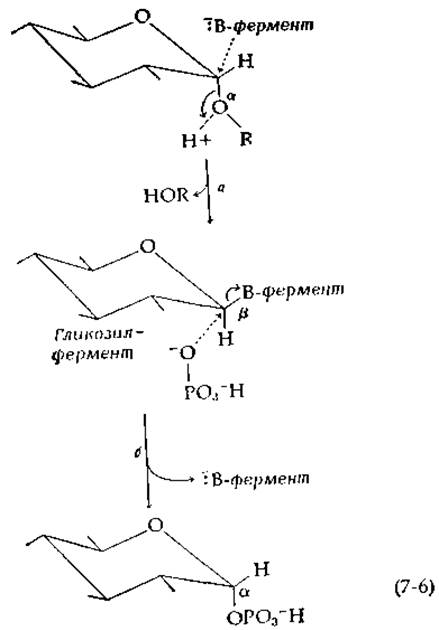
Можно допустить, что сахарозофосфорилаза катализирует два последовательных акта замещения, каждый из которых сопровождается инверсией [уравнение (7-6)].
Тогда на первой стадии реакции (7-6) происходило бы замещение нуклеофильной группы фермента (стадия а) с образованием гликозилфермента, а на второй стадии (стадия б) — атака фосфатом, сопровождающаяся регенерацией фермента и свободной нуклеофильной группой В-.
Каковы возможные предсказания и экспериментальные тесты для доказательства механизма двойного замещения? В разд. В, 3, а — в обсуждается четыре типа экспериментов, выполненных с сахарозофосфорилазой. Они могут быть использованы также для изучения и многих других ферментов.
а. Реакции обмена
Исходя из механизма двойного замещения, можно предсказать, что фермент должен катализировать парциальные реакции обмена между одним из двух субстратов и меченым продуктом. Например, сахароза, содержащая 14С в фруктозной части молекулы, должна реагировать с сахарозофосфорилазой с образованием глюкозилфермента и свободной радиоактивной фруктозы в качестве продукта замещения:
![]()
Здесь звездочками обозначены соединения, содержащие 14С. Обычно в опытах используют очень низкие молярные концентрации ферментов, и, следовательно, чтобы обнаружить реакцию (7-7), достаточно добавить с большим избытком нерадиоактивную фруктозу. В этих условиях фермент не катализирует общую химическую реакцию, а многократно переходит из состояния свободного фермента в глюкозилфермент и обратно. Каждый раз в обратной реакции фермент использует в первую очередь немеченую фруктозу. Суммарный эффект состоит в катализе ферментом обменной реакции между фруктозой и сахарозой:
![]()
Обмен между фруктозой и сахарозой наблюдали экспериментально [7], так же как и второй предсказанный обмен, а именно обмен глюкозо-1-фосфата с радиоактивным фосфатом:
![]()
Этим обменным реакциям близки реакции переноса, в которых какой-либо кетосахар, отличный от фруктозы, например D-кетоксилоза, реагирует с глюкозилферментом с образованием нового дисахарида, содержащего глюкозу и добавленную кетозу [7].
Анализ обменных реакций в качестве критерия механизма часто используется при изучении сложных ферментативных процессов во всех областях метаболизма, и поэтому его надо хорошо понять. Вместе с тем необходимо отдавать себе отчет в возможных ограничениях применимости этого критерия. Механизм двойного замещения предсказывает наличие определенных обменных реакций, однако экспериментальное обнаружение этих обменных процессов еще не доказывает существования промежуточных соединений, содержащих ковалентно связанный фермент. Более того, ферменты, использующие механизм двойного замещения, не во всех случаях катализируют ожидаемые обменные раакции (разд. В, 5).
б. Арсенолиз
Сахарозофосфорилаза катализирует также реакцию расщепления сахарозы арсенатом и, кроме того, способствует быстрому расщеплению арсенатом (арсенолизу) глюкозо-1-фосфата до свободной глюкозы. Эту реакцию проще всего представить как образование глюкозилфермента в качестве промежуточного соединения. Продукт реакции — нестабильный глюкозо-1-арсенат (дополнение 7-А). Арсенолиз служит общим способом обнаружения реакционноспособных ферментсодержащих промежуточных соединений, которые в обычных условиях реагируют с фосфатными группами. Арсенат является одним из многих субстратных аналогов, который может быть использован также для того, чтобы направить реакционноспособные ферментсодержащие промежуточные соединения в русло побочных метаболических путей.
в. Кинетика
Механизм двойного замещения требует, чтобы фермент работал по челночному типу, осуществляя переход между свободным ферментом и промежуточным соединением, несущим остаток субстрата, т. е. гликозилферментом. Изучение кинетики реакций, катализируемых сахарозо- фосфорилазой, показывает, что зависимость скорости реакции от концентрации сахарозы и НРО2-4 подчиняется закономерностям, действующим в случае пинг-понг-механизма (гл. 6, разд. А, 10, а) [8].
а. Прямое выделение промежуточных продуктов
Методы выделения чистых ферментов и работы с очень малыми количествами веществ в настоящее время развиты настолько хорошо, что часто имеется возможность прямыми методами подтвердить существование постулированных ферментсодержащих промежуточных соединений. Так, было осуществлено выделение глюкозилфермента в денатурированной форме после проведения реакции между высокоочищенной сахарозофосфорилазой и меченной радиоактивным изотопом сахарозой [8]. Глюкозилфермент слишком лабилен, чтобы выдержать даже мягкое расщепление пептидной цепи и выделение меченного гликозилом фрагмента. Однако косвенные данные убедительно свидетельствуют о том, что —В: является карбоксилатной группой (—СОО-) [9].