БИОХИМИЯ - Л. Страйер - 1984
ТОМ 1
ЧАСТЬ I. КОНФОРМАЦИЯ И ДИНАМИКА
ГЛАВА 2. ОСНОВНЫЕ ПРЕДСТАВЛЕНИЯ О СТРУКТУРЕ И ФУНКЦИИ БЕЛКОВ
2.6. Последовательность аминокислот в белках уникальна и детерминируется генами
В 1953 г. Фредерик Сэнгер (Sanger) определил последовательность аминокислот в белковом гормоне - инсулине (рис. 2.25). Эта работа представляет собой веху в развитии биохимии, ибо в ней впервые было показано, что белок имеет строго определенную последовательность аминокислот. Кроме того, это достижение послужило стимулом для других исследователей подвергнуть аналогичному анализу большое множество белков. И действительно, к настоящему времени установлена полная последовательность аминокислот у нескольких сотен белков. Самое поразительное, что каждый белок имеет уникальную, точно определенную последовательность аминокислот. В серии остроумных работ, проведенных в конце50-х-начале 60-х годов было обнаружено, что последовательность аминокислот в белках детерминирована генетически. Последовательность нуклеотидов в ДНК-веществе наследственности - определяет комплементарную последовательность нуклеотидов в РНК, а последняя в свою очередь определяет последовательность аминокислот в белке (гл. 25). Более того, синтез всех белков из соответствующих аминокислот имеет единый механизм.
Рис. 2.25. Последовательность аминокислот в инсулине крупного рогатого скота

Определение последовательности аминокислот в белках представляет интерес по четырем причинам. Во-первых, такие данные имеют большое значение для выяснения молекулярной основы биологической активности белка. Сведения о последовательности аминокислот приобретают особую ценность при их сопоставлении с другими химическими и физическими характеристиками. Во-вторых, изучение последовательности аминокислот в сочетании с детальным анализом пространственной структуры необходимо для выяснения тех принципов, на основе которых из полипептидных цепей формируются высокоспецифичные трехмерные формы. При этом последовательность аминокислот в белке служит связующим звеном между генетической информацией, заложенной в ДНК, и трехмерной структурой белка, лежащей в основе его биологической активности. В-третьих, изменения в последовательности аминокислот могут привести к нарушению нормальной функции белка, а, следовательно, и к соответствующей болезни. В частности, такая тяжелая болезнь, как серповидноклеточная анемия, нередко приводящая к летальному исходу, возникает в результате замены всею лишь одной-единственной аминокислоты в одном-единственном белке. Таким образом, определение последовательности аминокислот относится к новой области медицины - молекулярной патологии. В-четвертых, данные о последовательности аминокислот в белке могут многое рассказать о его эволюции. Дело в том, что в неродственных белках эти последовательности совершенно различны. Белки лишь в том случае имеют сходную последовательность аминокислот, если они происходят от общего белка-предшественника. Следовательно, изучение последовательностей аминокислот в белках позволяет проследить эволюцию на молекулярном уровне.
Белки-называют также протеинами. Последний термин, введенный Барцелиусом в 1838 г., подчеркивает важное значение этого класса веществ. Термин образован от греческого слова ргоtеios, что означает «первостепенный». Термин «протеин» введен Мулдером (Lieben F. Geschichte der Physiologischen Chemie, Leipzig und Wien, I. Deutike, 1935, s. 359).- Прим. ред.
2.7. Экспериментальные методы определения последовательности аминокислот
Рассмотрим сначала, как можно определить последовательность аминокислот в коротком пептиде. Допустим, что пептид состоит из 6 аминокислотных остатков, расположенных в следующей последовательности: Аlа-Сlу-Аsр-Рhе-Аrg-Gly. (Для обозначения аминокислот использованы общепринятые сокращения, приведенные в табл. 2.1, стр. 23.) Прежде всего необходимо определить аминокислотный состав пептида. Для этого его гидролизуют до составляющих аминокислот нагреванием до 110°С в течение 24 ч в 6 н. НСl. Далее аминокислоты полученного гидролизата разделяют методом ионообменной хроматографии на колонке с сульфонированным полистиролом. Фракционированные аминокислоты определяют по окраске, образующейся при нагревании с нингидрином: α-аминокислоты дают с нингидрином интенсивное синее окрашивание, а иминокислоты, например, пролин-желтое. Метод ионообменной хроматографии обладает высокой чувствительностью:
с его помощью можно определить даже один микрограмм аминокислоты, т. е. примерно столько, сколько содержится в одном отпечатке пальца. Количество аминокислоты пропорционально оптической плотности раствора после нагревания с нингидрином. Если требуется определить еще меньшие количества аминокислоты - порядка нескольких нанограммов, то используют флуорескамин, который реагирует с α-аминогруппой, образуя сильно флуоресцирующее соединение. О природе аминокислоты судят по объему элюции, т. е. по объему буфера, использованному для вымывания данной аминокислоты с колонии (рис. 2.26). Сравнение результатов хроматографии гидролизата со стандартной смесью аминокислот свидетельствует о том, что исследуемый пептид имеет следующий аминокислотный состав:
(Ala, Arg, Asp, Gly2, Phe).
Скобки показывают, что речь идет о составе, а не последовательности аминокислот в пептиде.
Рис. 2.26. Аминокислоты, содержащиеся в гидролизате белка, разделяют методом ионообменной хроматографии на сульфонированном полистироле (например, дауэкс-50). Для элюции аминокислот с колонки используют буферы с возрастающим значением pH. Первым снимается с колонки аспартат, имеющий кислотную боковую цепь; аргинин с основной боковой цепью элюируется последним. По оси ординат отложено поглощение
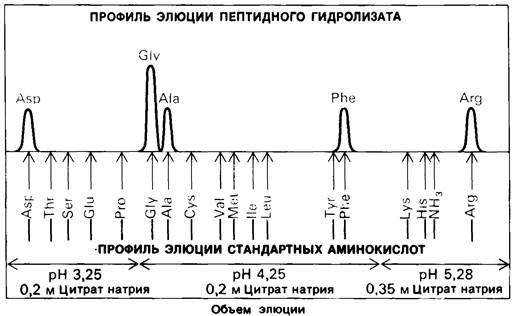
Рис. 2.27. Определение N-концевого остатка пептида. Пептид метят фтординитробензолом (реактив Сэнгера) и затем гидролизуют. ДНФ-производное аминокислоты (в приведенном примере ДНФ-аланин) идентифицируют по хроматографическим характеристикам
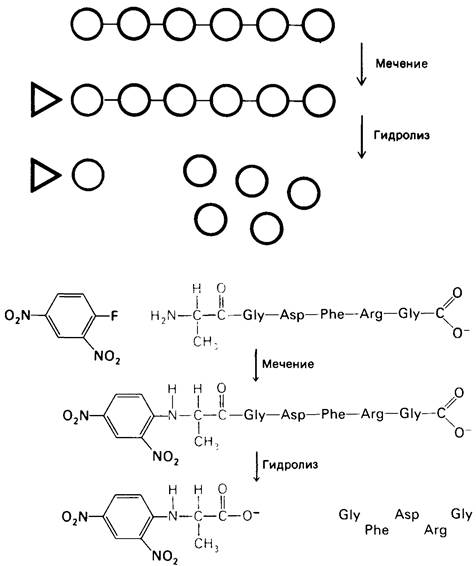
Для определения в белке или пептиде концевого остатка, несущего аминогруппу, его метят с помощью соединения, образующего стабильную ковалентную связь с азотом аминогруппы (рис. 2.27). Впервые для этой цели Сэнгер использовал фтординитробензол (ФДНБ), реагирующий с незаряженной α-NН2-группой с образованием динитрофенильного (ДНФ) производного пептида желтого цвета. Связь между ДНФ и концевой аминогруппой стабильна в условиях, используемых для гидролиза пептидных связей. Поэтому при гидролизе ДНФ-производного пептида Аlа-Сlу-Аsр-Рhе-Gly в 6 н. НСl высвобождается ДНФ-аминокислота, которую можно идентифицировать хроматографически как ДНФ-аланин.
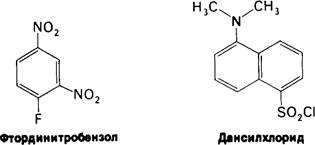
Для идентификации N-концевых аминокислот в настоящее время часто используют дансилхлорид, который при взаимодействии с аминогруппой дает стабильное, интенсивно флуоресцирующее сульфамидное производное. Этот метод позволяет выявить N-концевую аминокислоту (после кислотного гидролиза пептидных
связей), присутствующую в таком незначительном количестве, как несколько нанограммов.
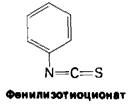
При всех достоинствах методов определения N-концевых аминокислотных остатков с помощью ДНФ или дансилхлорида их, к сожалению, нельзя использовать дважды применительно к одному и тому же пептиду, поскольку последний полностью распадается при кислотном гидролизе. Перу Эдману (Р. Еdman) удалось разработать метод маркирования N-концевого остатка и отщепления его от пептида без сопутствующего расщепления остальных пептидных связей. Деградация по Эдману (реакция Эдмана) состоит в ступенчатом (по одному) отщеплении аминокислотных остатков с аминоконца пептида (рис. 2.28). Фенилизотиоцианат реагирует с незаряженной концевой аминогруппой пептида с образованием фенилтиокарбамоильного производного. Далее в слабокислой среде происходит отщепление циклического производного N-концевой аминокислоты, а оставшийся неразрушенным пептид оказывается укороченным на один аминокислотный остаток. Указанное циклическое производное представляет собой фенилтиогидантоин-аминокислогу (ФТГ-аминокислоту). Его идентифицируют методом хроматографии. Далее аминокислотный состав укороченного пептида (Arg, Asp, Gly2, Phe) сравнивают с исходным: (Ala, Arg, Asp, Gly2, Phe).Оказывается, что различие состоит в одном остатке аланина. Следовательно, в исходном пептиде аланин занимает N-концевое положение. Деградацию по Эдману можно вновь повторить на укороченном пептиде. Исходя из аминокислотного состава после второй ступени деградации (Arg, Asp, Gly, Phe) можно прийти к выводу, что вторым остатком с N-конца является глицин. Это заключение подтверждают путем хроматографической идентификации ФТГ-глицина, полученного на второй ступени деградации пептида. Еще три ступени деградации по Эдману позволяют полностью раскрыть последовательность аминокислот во взятом пептиде.
Рис. 2.28. Деградация по Эдману. От пептидной цепи отщепляют меченый N-концевой остаток аминокислоты (ФТГ-аланин на первой ступени деградации). Остаток пептидной цепи при этом не гидролизуется. На второй ступени деградации определяют следующий N-концевой аминокислотный остаток. Еще три ступени деградации по Эдману позволят установить всю последовательность аминокислот во взятом пептиде
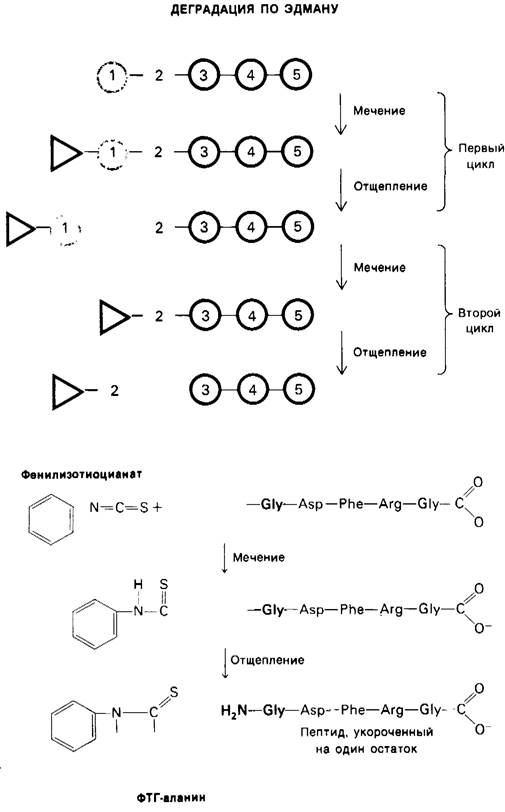
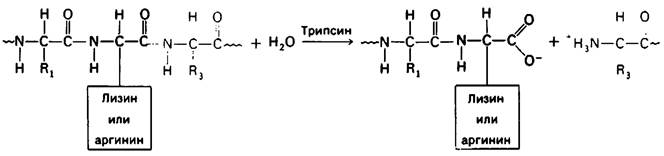
Стратегию анализа последовательности аминокислот в белках можно определить, как «разделяй и властвуй». Белок подвергают специфическому расщеплению на более короткие пептиды, последовательность аминокислот в которых определяют по Эдману. Специфическое расщепление можно производить химическими или ферментативным методами. Так, Б. Уиткоп (В. Witkop) и Э. Гросс (Е. Gross) обнаружили, что бромистый циан (CNBr) расщепляет полипептидную цепь только по пептидной связи, образованной карбоксильной группой остатка метионина (рис. 2.29). Если в белке содержится 10 метиониновых остатков, то после обработки бромистым цианом обычно получается 11 пептидов. Высокоспецифическое расщепление достигается также с помощью трипсина-протеолитического фермента поджелудочной железы. Трипсин расщепляет полипептидные цепи по пептидной связи, образованной карбоксильной группой остатков аргинина и лизина (рис. 2.30). В результате белок, содержащий 9 остатков лизина и 7 остатков аргинина, после расщепления трипсином распадается на 17 пептидов. Каждый из этих пептидов, кроме пептида, расположенною на карбоксильном конце белка, будет кончаться аргинином или лизином. Ряд других способов специфического расщепления полипептидных цепей приведен в табл. 2.2.
Рис. 2.29. Бромистый циан расщепляет полипептиды по карбоксильной группе метиониновых остатков
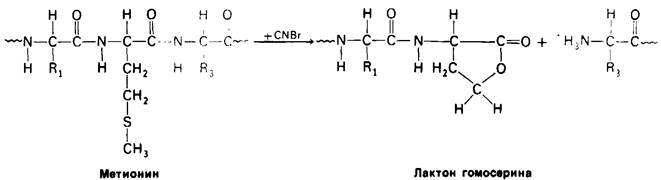
Рис. 2.30. Трипсин гидролизует полипептиды по карбоксильной группе остатков лизина и аргинина
Таблида 2.2. Специфическое расщепление полипептидов

Пептиды, полученные при специфическом химическом или ферментативном расщеплении белка, разделяют методами хроматографии. Далее последовательность аминокислот в каждом из пептидов определяют методом Эдмана. Таким образом, достигается этап, когда последовательность аминокислот в отдельных пептидах (фрагментах белка) известна, но остается невыясненной последовательность самих пептидов. Последнюю устанавливают с помощью так называемых перекрывающихся пептидов (рис. 2.31). При этом используют уже не трипсин, а какой-либо фермент, расщепляющий полипептидную цепь в других участках, например, химотрипсин, который расщепляет пептидные связи главным образом покарбоксильным группам ароматических и других больших неполярных аминокислотных остатков. Пептиды, образующиеся под действием химотрипсина, неизбежно перекрывают два или более триптических пептида, что используется для установления их последовательности. Таким путем полностью определяют последовательность аминокислот в белке.
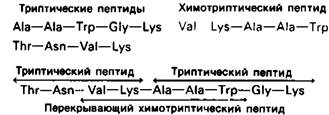
Рис. 2.31. Пептид, образующийся при химотриптическом расщеплении, перекрывает два триптических пептида; благодаря этому можно установить последовательность расположения пептидов
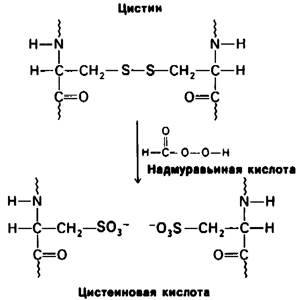
Описанные методы применимы к белкам, состоящим из одной полипептидной цепи, не имеющей дисульфидных связей. В тех же случаях, когда в белке имеются дисульфидные связи или более одной полипептидной цепи, то необходимы дополнительные методические приемы. Например, если белок содержит две или более полипептидные цепи, соединенные нековалентными связями, то, воздействуя денатурирующими агентами, такими, как мочевина или гуанидингидрохлорнд, вызывают диссоциацию цепей. Диссоциированные цепи разделяют и только после этого приступают к определению последовательности аминокислот в каждой из них. Если же полипептидные цепи соединены ковалентными дисульфидными связями, как это имеет место в инсулине, то их окисляют надмуравьиной кислотой; при этом дисульфидные связи разрываются и образуются остатки цистеиновой кислоты (рис. 2.32).
Рис. 2.32. Дисульфиды расщепляются надмуравьиной кислотой
Анализ структуры белков удалось значительно ускорить путем создания секвенатора-специального прибора для автоматического определения последовательности аминокислот. При таком определении белок в виде тонкой пленки помещают во вращающийся цилиндрический сосуд, где он подвергается деградации по Эдману. Реактивы и растворители проходят над иммобилизованной белковой пленкой, а высвобождающиеся ФТГ-аминокислоты подвергаются жидкостной хроматографии при высоком давлении и таким образом идентифицируются. Один цикл деградации по Эдману занимает при этом менее двух часов. С помощью секвенатора можно определить аминокислотную последовательность полипептида или белка, содержащего до ста аминокислотных остатков,