БИОХИМИЯ - Л. Страйер - 1984
ТОМ 2
ЧАСТЬ III. БИОСИНТЕЗ ПРЕДШЕСТВЕННИКОВ МАКРОМОЛЕКУЛ
ГЛАВА 22. БИОСИНТЕЗ НУКЛЕОТИДОВ
22.18. АТР-предшественник NAD+, FAD н кофермента А
Биосинтез никотинамидадениндинуклеоти- да (NAD+) начинается с образования рибо- нуклеотида никотиновой кислоты из никотината и ФРПФ. Никотинат (его также называют ниицином) происходит из триптофана. Организм человека способен синтезировать необходимое количество никотината, если с пищей поступает достаточно триптофана. Если же с пищей поступает мало триптофана, то организм нуждается также в экзогенном никотинате. Пеллагра- заболевание, связанное с недостатком
триптофана и никотината в пище.
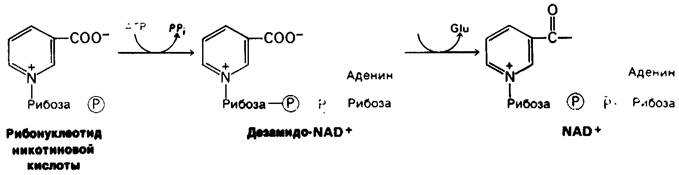
Остаток АМР переносится с АТР на ри- онуклеотид никотиновой кислоты, и в результате образуется дезамидо-NAD+. На последнем этапе амидогруппа глутамина переносится на карбоксильную группу никотиновой кислоты, давая NAD+ (рис. 22.25). NADP+ образуется из NAD + путем фосфорилирования 2-гидроксильной группы остатка рибозы аденина. Этот перенос фосфатной группы катализирует NAD+-киназа.
Рис. 22.25. Синтез NAD+ из рибонуклеотида никотиновой кислоты
Флавинадеииндинуклеотид (FAD) синтезируется из рибофлавина и двух молекул АТР. Рибофлавин фосфорилируется за счет АТР с образованием рибофлавин-5'-фосфата (называемого также флавипмононуклеотидом). После этого происходит перенос еще одного остатка АМР второй молекулы АТР на рибофлавин-5'-фосфат, и образуется флавинадеииндинуклеотид.
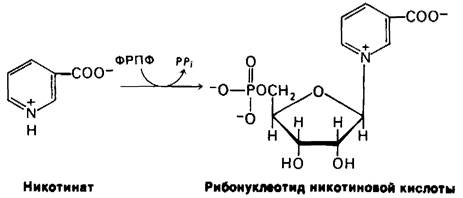
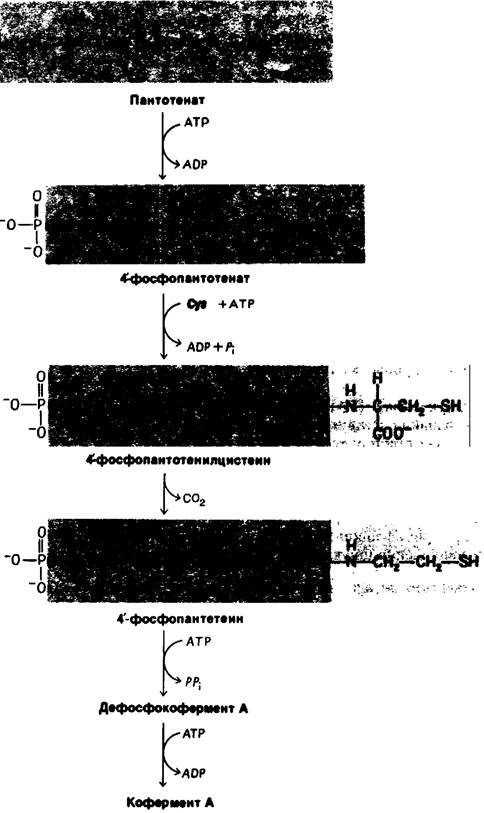
Рис. 22.26. Синтез кофермента А из пантотената
Рибофлавин + АТР → Рибофлавин-5'-фосфат + ADP,
Рибофлавин-5'-фосфат + АТР → Флавинадеииндинуклеотид + РРi.
Синтез кофермента А (СоА) в организме животных начинается с фосфорилирования пантотената (рис. 22.26). Животные нуждаются в поступлении пантогената с пищей, а растения и микроорганизмы сами ето синтезируют. Затем образуется пептидная связь между карбоксильной группой 4'-фосфопантогената и аминогруппой цистеина. Карбоксильная группа остатка цистеина отщепляется, и образуется 4'-фосфопантотеин. На этот промежуточный продукт переносится остаток АМР от АТР, и образуется дефосфокофермент А. Наконец фосфорилирование З'-гидроксильной группы дает кофермент А.
Общее в механизме биосинтеза NAD+, FAD и СоА-это перенос остатки АМР с АТР на фосфатную группу фосфорилированного промежуточного продукта. Пирофосфат, который образуется в этой реакции, гидролизуется до ортофосфата. Этот мотив постоянно повторяется в биохимии: движущей силой биосинтетических реакций часто служит гидролиз высвобождающегося пирофосфата.
22.19. В организме человека пурины распадаются до мочевой кислоты
В клетке происходит постоянный обмен нуклеотидов. Нуклеотидизы гидролитически расщепляют нуклеотиды до нуклеозидов. Фосфоролитическое расщепление нуклеотидов до свободных оснований и рибозо-1-фосфата (или дезоксирибозо-1- фосфата) катализируется нуклеозид-фосфорилазой. Рибозо-1-фосфат изомеризуется под действием фосфорибомутазы, превращаясь в рибозо-5-фосфат, субстрат синтеза ФРПФ. Некоторые азотистые основания используются повторно для синтеза нуклеотидов в реакциях синтеза из готовых остатков.
Расщепление АМР (рис. 22.27) включает еще один этап. АМР дезаминируется до IMP под действием аденилатдезаминазы. Последующие реакции, приводящие к образованию свободного основания гипоксантина, идут обычным путем. Ксанти- ноксидаза-флавопротеин, содержащий молибден и железо, окисляет гипоксантин до ксантина и затем до мочевой кислоты. В обеих реакциях в качестве окислителя используется молекулярный кислород. Он восстанавливается до Н2О2, а каталаза разлагает образующуюся перекись на Н2О и О2. Кроме того, ксантин-промежуточный продукт образования мочевой кислоты из гуанина. В организме человека мочевая кислота - конечный продукт расщепления пуринов; она выделяется с мочой.
Рис. 22.27. Распад АМР до мочевой кислоты

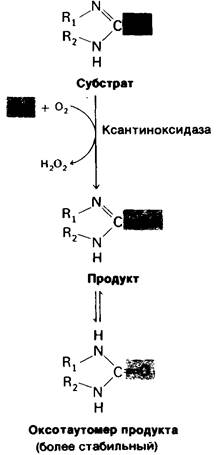
Рис. 22.28. Общая схема реакций окисления, катализируемых ксанти- ноксидазой
22.20. У некоторых организмов происходит дальнейший распад мочевой кислоты
У некоторых видов происходит дальнейшее расщепление пуринов (рис. 22.29). Млекопитающие, кроме приматов, выделяют аллантоин- продукт окисления мочевой кислоты. Костистые рыбы выделяют аллантоевую кислоту, которая образуется путем гидратирования аллантоина. У амфибий и большинства рыб расщепление идет еще дальше; аллантоевая кислота гидролизуется до двух молекул мочевины и одной молекулы глиоксилата. Наконец, некоторые морские беспозвоночные гидролизуют мочевину до NH4+ и СО2. По всей вероятности, ферменты, катализирующие все эти реакции, постепенно утрачивались по мере эволюции приматов.
Рис. 22.29. Распад, мочевой кислоты до NH4+ и СO2. Эти реакции катализируются ферментами уриказой (1), аллантоиназой (2), аллантоиказой (3) и уреазой (4)
