БИОХИМИЯ - Л. Страйер - 1984
ТОМ 2
ЧАСТЬ III. БИОСИНТЕЗ ПРЕДШЕСТВЕННИКОВ МАКРОМОЛЕКУЛ
ГЛАВА 20. БИОСИНТЕЗ МЕМБРАННЫХ ЛИПИДОВ И СТЕРОИДНЫХ ГОРМОНОВ
20.18. Отсутствие рецепторов ЛНП приводит к гиперхолестеролемин и преждевременному атеросклерозу
Исследования семейной гиперхолестеролемии указывают на важную роль рецепторов ЛНП. При этом нарушении общая концентрация холестерола и ЛНП в сыво-
ротке крови заметно увеличена. Это результат мутации в одном-единственном аутосомном локусе. Содержание холестерола в сыворотке гомозиготных больных составляет обычно 6,8 г/л, у гетерозиготных- 3 г/л, а в норме равно 1,75 г/л. Из-за того, что концентрация ЛНП, содержащих холестеролу в плазме крови увеличена, холе- стерол откладывается в различных тканях. Гранулы холестерола называют ксантомами; они часто встречаются в коже и сухожилиях. Более опасно отложение холестерола в бляшках на стенках артерий, приводящее к атеросклерозу. Большинство гомозиготных больных гиперхолестероле- мией погибает в детстве из-за поражения коронарных сосудов. У гетерозигот наблюдаются различные формы заболевания, и в целом оно протекает легче. В большинстве случаев семейной гиперхолестероле- мии молекулярное нарушение состоит в отсутствии или нехватке активных рецепторов ЛНП. У гомозигот таких рецепторов почти нет, а у гетерозигот их количество примерно вдвое меньше нормы. Вследствие этого проникновение ЛНП в клетки различных тканей вне печени нарушено, и содержание ЛНП в сыворотке крови увеличено. Кроме того, наследственная гиперхолестеролемия может возникать из-за нарушения переноса комплекса ЛНП—рецептор внутрь клеток.
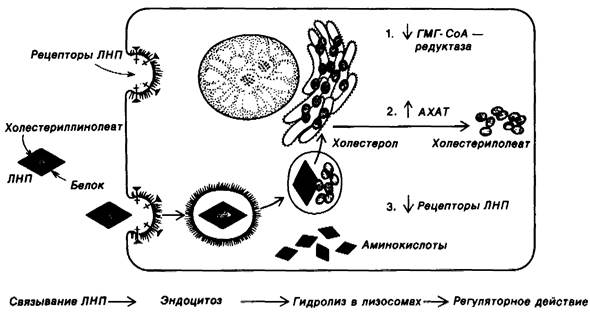
Рис. 20.17. Превращения липопротеинов низкой плотности в культивируемых фибробластах человека. ГМГ-СоА—редуктаза - 3 - гидрокси - 3 - метилглутарил- СоА—редуктаза; АХАТ-ацил- СоА : холестерол-ацилтрансфераза
20.19. Номенклатура стероидов
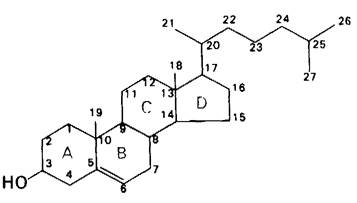
Прежде чем перейти к синтезу стероидных гормонов, необходимо сделать несколько замечаний о номенклатуре стероидов. Атомы углерода в стероидах нумеруются так, как указано на рис. 20.18 на примере холестерола. Кольца стероидной молекулы обозначаются латинскими буквами А, В, С и D. Холестерол содержит две боковые метильные группы: метильная группа С-19 присоединена к С-10, а метильная группа С-18-к С-13. Химические связи над С-10 и С-13 обозначают эти метильные группы. Метильные группы холестерола С-18 и С-19 по определению расположены над плоскостью четырех колец. Заместители, расположенные над плоскостью, называют β-ориентированными и соответствующую химическую связь изображают непрерывной чертой. Заместители, расположенные ниже плоскости колец, находятся в α- ориентации, и соответствующая связь изображается прерывистой линией.
Рис. 20.18. Нумерация атомов углерода в молекуле холестерола
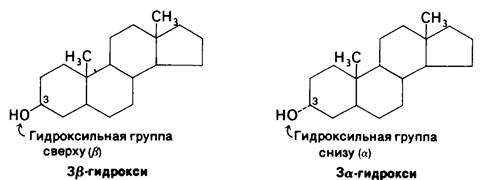
Атом водорода при атоме С-5 может находиться в α- или β-ориентации. Если этот атом водорода находится в α-ориентации, кольца А и В соединены в транс-конформации, тогда как при β-ориентации кольца образуют цис-сочленение. Если атом водорода при С-5 не обозначен, кольца образуют транс-сочленение. Во всех стероидных гормонах, имеющих атом водорода при С-5, он находится в α-ориентации. В молекулах желчных кислот, наоборот, атом водорода при С-5 находится в β-ориентации. Таким образом, цис-сочленение характерно для солей желчных кислот, тогда как транс-сочленение-для всех стероидных гормонов, у которых при С-5 имеется водород. Транс-сочленение колец дает почти плоскую структуру, тогда как цис-сочленение - изогнутую форму.
20.20. Стероидные гормоны образуются из холестерола
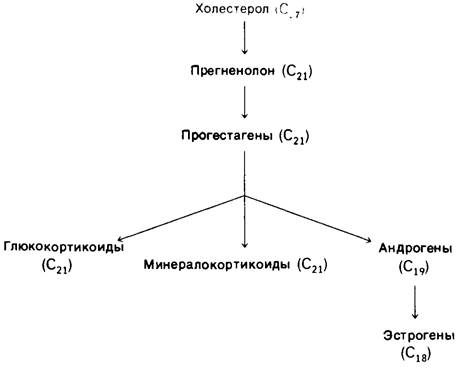
Холестерол-предшественник пяти основных классов стероидных гормонов: про- гестагенов глюкокортикоидов, минералокортикоидов, андрогенов и эстрогенов (рис. 20.19). Прогестерон, один из прогестагенов, подготавливает выстилающий слой матки к имплантации яйца. Кроме того, прогестерон имеет существенное значение для поддержания состояния беременности. Андрогены (например, тестостерон) отвечают за развитие у самцов вторичных половых признаков, а эстрогены (например, эстроп) необходимы для развития вторичных половых признаков у самок. Кроме того, эстрогены участвуют в овариальном цикле. Глюкокортикоиды (например, кортизол) стимулируют глюконеогенез и образование гликогена и способствуют расщеплению жиров и белков. Минералокортикоиды (такие, как альдостерон) увеличивают обратное всасывание ионов Na+, Сl- и НSО3- в почках, повышая таким образом объем крови и кровяное давление. Эти классы гормонов синтезируются в основном в следующих местах: прогестагены-в желтом теле; эстрогены-в яичниках; андрогены-в семенниках; глюкокортикоиды и минералокортикоиды-в коре надпочечников.
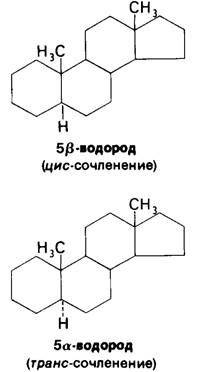
Рис. 20.19. Реакции биосинтеза стероидных гормонов
20.21. Стероиды гидроксилируются под действием монооксигеназ, использующих NADРН и кислород
Реакции гидроксилирования играют очень важную роль в синтезе холестерола из сквалена и в превращении холестерола в стероидные гормоны и желчные кислоты. Все эти реакции гидроксилирования идут при участии NАDРН и O2. Как показали опыты с использованием O2 и Н2O, меченных 18O, атом кислорода включенной гидроксильной группы происходит из O2, а не из Н2O. Один из атомов кислорода молекулы O2 включается в субстрат, а второй восстанавливается до воды. Ферменты, катализирующие подобные реакции, называются монооксигеназами (или оксигеназами со смешанной функцией). Напомним, что еще одна монооксигеназа участвует также в гидрок- силировании фенилаланина (разд. 18.16).
RН + O2 + NADPH + Н+ → RОН + Н2O + NADP+
Для реакции гидроксилирования необходимо активировать кислород. При синтезе стероидных гормонов и солей желчных кислот активация осуществляется с помощью особого цитохрома, названного Р450, поскольку комплекс этого цитохрома с СО имеет максимум поглощения при 450 нм. Цитохром Р450-конечный компонент цепи переноса электронов, обнаруженной в митохондриях надпочечников и в микросомах печени. Роль этой цепи состоит прежде всего в гидроксилировании, а не в окислительном фосфорилировании. Электроны NADPH, обладающие высоким энергетическим потенциалом, переносятся на флавопротеин этой цепи; затем они передаются на адренодоксин, белок, содержащий негемовое железо. Адренодоксин переносит электроны на окисленную форму цитохрома Р450. Затем восстановленная форма Р450 активирует O2.
Система, включающая цитохром Р450, играет важную роль в обезвреживании чужеродных (ксенобиотических) соединений. Например, гидроксилирование барбитурата фенобарбитала увеличивает его растворимость и облегчает его выведение. Точно так же и полициклические ароматические углеводороды гидроксилируются системой Р450. Введение гидроксильных групп позволяет присоединить к этим молекулам весьма полярные группы (например, глюкуронат или сульфат), которые заметно увеличивают растворимость модифицированных ароматических молекул. Однако действие системы Р450 не всегда полезно для организма. Последние исследования показали, что наиболее мощные канцерогены превращаются in vivo в химически активную форму. Этот процесс метаболической активации осуществляется обычно системой Р450.