БИОХИМИЯ - Л. Страйер - 1984
ТОМ 3
Часть IV ИНФОРМАЦИЯ
ГЛАВА 29. ЭУКАРИОТИЧЕСКИЕ ХРОМОСОМЫ И ВЫРАЖЕНИЕ ГЕНОВ У ЭУКАРИОТ
29.26. Талассемия - генетически обусловленное нарушение синтеза гемоглобина
Изучение гемоглобина внесло большой вклад в наши представления о структуре и функции белка (гл. 4 и 5). Точно так же исследования, посвященные генам гемоглобина и их выражению, оказались важным источником данных о функционировании эукариотических генов. В процессе внутриутробного развития происходит замена эмбриональных гемоглобинов гемоглобином плода (HbF, α2γ2), а затем гемоглобином взрослого типа (НbА, α2β2). Кроме того, во взрослом организме образуется небольшое количество гемоглобина НbА2, субъединичная структура которого α2δ2. Напомним, что HbF имеет более высокое сродство к кислороду, чем НbА, так как он менее прочно связывает бисфосфоглицерат (разд. 4.7). Это повышенное сродство к кислороду благоприятствует его переносу из кровеносной системы матери в кровеносную систему плода. В действительности HbF представляет собой смесь двух разновидностей, одна из которых содержит в положении 136 γ-цепи глицин, а другая - аланин. Эти разновидности обозначаются Gγ и Аγ соответственно.
Все гены гемоглобина картированы. На гаплоидный геном приходится два тесно сцепленных a-гена глобина. Эти гены у всех людей, за исключением редких мутантов, по-видимому, идентичны. Другие гены глобина сгруппированы в кластеры в другой хромосоме в следующем порядке: Gγ-Aγ-δ-β (рис. 29.37). Интересно было бы выяснить, почему эти функционально родственные гены расположены рядом друг с другом в одной хромосоме. Вполне возможно, что для переключения экспрессии с γ-генов на δ- и β-гены в ходе развития необходимо, чтобы они соседствовали. Не исключено также, что сцепление этих генов отражает историю их эволюции. По всей вероятности, γ-, δ- и β-гены имеют общего предка, который подвергся тандемным дупликациям и затем дивергировал.
Рис. 29.37. Карта генов γ-, δ- и β-глобина человека

Талассемии - группа наследственных анемий, при которых скорость синтеза одной из цепей гемоглобина понижена. Название болезни «талассемия» происходит от греческого слова, обозначающего «море», так как болезнь широко распространена у выходцев из Средиземноморья. Большая и малая талассемии наблюдаются у гомозиготных и гетерозиготных больных соответственно. Буквенное обозначение a или в указывает, какая цепь синтезируется с пониженной скоростью. В настоящее время в результате изучения глобиновой мРНК и клонированной глобиновой ДНК начинает проясняться причина этих заболеваний. Установлены молекулярные механизмы некоторых видов талассемий.
1. Делеция гена. При некоторых видах a-талассемий делетированы один или оба a-глобиновых гена.
2. Нестабильность мРНК. В гемоглобине Constant Spring a-цепь содержит 172 остатка вместо 141 из-за мутации, приводящей к замене стоп-кодона UAA в кодон глутамина САА. Трансляция участка, который в норме не является кодирующим, каким-то образом делает мутантную мРНК чувствительной к действию нуклеаз.
3. Нарушение инициации цепей. При некоторых видах β-талассемии инициирование трансляции происходит слишком медленно, что, возможно, объясняется дефектом в 5'-нетранслируемой области.
4. Преждевременная терминация цепи. Один из видов β-талассемии возникает в результате замены одного основания в кодоне лизина AAG, приводящей к образованию стоп-кодона UAG в 17-м положении.
5. Пониженное образование мРНК. При многих видах β-талассемии, как оказалось, ген β-глобина имеется, но β-глобиновой мРНК образуется очень мало. В настоящее время причина этого явления интенсивно изучается. Не исключена возможность, что при некоторых видах β-талассемии не происходит правильного вырезания вставочных последовательностей1.
29.27. Трансляция регулируется каскадом протеинкиназ, инактивирующим один из факторов инициации
В экстрактах ретикулоцитов происходит с высокой скоростью синтез субъединиц гемоглобина до тех пор, пока не иссякает гем. В отсутствие гема синтез белка останавливается из-за быстрого образования ферментативного ингибитора белкового синтеза. Этим ингибитором является протеинкиназа. Мишенью для киназы служит eIF-2 - фактор инициации, связывающий GTP и доставляющий Met-тРНК, к 40S-субчастице рибосомы2. Инактивация eIF-2 в результате фосфорилирования приводит к блокирова нию инициации синтеза белка. Каким же образом гем регулирует активность этой киназы? Действие это опосредуется еще одной киназой (рис. 29.38). Киназа eIF-2, модифицирующая фактор инициации, сама существует в двух формах - неактивной де- фосфорилированной и активной фосфорилированной. Фосфорилирование киназы eIF-2 катализируется зависимой от циклического AMPкиназой, состоящей из двух типов субъединиц - двух регуляторных (R) и двух каталитических (С). Неактивный комплекс R2C диссоциирует под действием циклического AMP на две каталитически активные С-субъединицы и две R-субъединицы. Гем блокирует процесс диссоциации, и как следствие этого активации двух киназ регуляторной системы не происходит. В результате фактор eIF-2 не фосфорилируется и сохраняет свою активность в инициации белкового синтеза. Этот каскад протеинкиназ напоминает регуляцию метаболизма гликогена (разд. 16.15). Эти процессы имеют еще и то общее, что в обоих случаях регуляторное действие этих киназ обращается специфическими фосфатазами.
1 В случае так называемой β+-талассемии это оказалось именно так, причем единственное отличие мутантного гена от гена дикого типа-замена одного-единственного нуклеотида в нитроне. Прим. перев.
2 Каскадный механизм регуляции, описанный автором и предложенный в лаборатории Очоа, оказался ошибочным. Хотя сАМР-зависимая протеинкиназа фосфорилирует многие белки. Oна не затрагивает eIF-2 и никак не влияет на активность протеинкиназы в физиологических условиях. Прим. перев.
Рис. 29.38. Каскад фосфорилирования, инактивирующий фактор инициации eIF-2

29.28. Дифтерийный токсин блокирует синтез белка у эукариот, ингибируя транслокацию
До появления эффективной иммунизации дифтерия была основной причиной детской смертности. Летальное действие этой болезни обусловлено главным образом токсином Corynebacterium diphteriae - бактерии, развивающейся в верхних дыхательных путях. Структурный ген токсина локализован в ли- зогенизирующем фаге, который содержат некоторые штаммы С. diphteriae. Несколько микрограммов этого токсина с массой 61 кДа обычно представляют собой летальную дозу для неиммунизированного человека, так как этой дозы достаточно для ингибирования синтеза белка. Дифтерийный токсин блокирует стадию элонгации синтеза белка у эукариот, инактивируя фактор элонгации, необходимый для транслокации. Этот фактор, называемый фактором элонгации 2 (EF-2) или транслоказой, выполняет у эукариот роль, аналогичную EF-G у бактерий. Транслоказа необходима для GTP-зависимого перемещения пептидил-тРНК из А-участка в Р-участок и одновременного перемещения информационной РНК сразу после образования пептидной связи. Особенно интересен механизм инактивации транслоказы дифтерийным токсином. Токсин катализирует ковалентную модификацию транслоказы. При этом NAD+ служит донором остатка аденозиндифосфатрибозы(ADPR); в результате реакции высвобождается никотинамид.
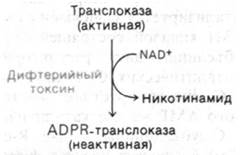
Молекула дифтерийного токсина состоит из двух частей. Ее можно расщепить на два фрагмента - с массой 21 кДа (фрагмент А) и 40 кДа (фрагмент В). Домен В связывается с поверхностью чувствительных клеток, а домен А катализирует ADP-рибозилирование транслоказы. Точнее, домен В связывается с ганглиозидом GM1 плазматической мембраны, что позволяет каталитическому домену проникнуть в клетку. При этом связанный токсин расщепляется, так что фрагмент В остается на поверхности клетки, а гидрофильный фрагмент А переносится в цитозоль. Интересно отметить, что многие другие токсины, например, холерный токсин (разд. 35.7), также состоят из домена, предназначенного для связывания с поверхностью клетки, и каталитического домена, который инактивирует какой-либо важный компонент клетки.
29.29. Рибосомы, связанные с эндоплазматическим ретикулумом, синтезируют секреторные и мембранные белки
В эукариотических клетках некоторые рибосомы свободно плавают в цитозоле, тогда как другие связаны с обширной системой мембран - эндоплазматическим ретикулумом (ЭР). Участки ЭР, связанные с рибосомами, называются шероховатым ЭР, так как на электронных микрофотографиях он покрыт бугорками (рис. 29.39), в отличие от гладкого ЭР, не содержащего рибосом. Клетки, секретирующие большое количество белка, например, ацинарные клетки поджелудочной железы, имеют сильно развитый шероховатый ЭР. В общем все известные секреторные белки синтезируются связанными с ЭР рибосомами. Кроме того, рибосомы, связанные с этой мембранной системой, синтезируют многие белки клеточной мембраны и таких органелл, как лизосомы.
Рис. 29.39. Электронная микрофотография шероховатого эндоплазматического ретикулума
Рис. 29.40. Электронная микрофотография кристаллических слоев, связанных с мембранами рибосом в ооцитах ящериц, впавших в зимнюю спячку

Связанные с мембранами рибосомы в ооцитах ящериц, впавших в зимнюю спячку, образуют кристаллические слои (рис. 29.40). Эти упорядоченные слои изучаются в настоящее время методами реконструкции трехмерного изображения. На карте низкого разрешения видно, что и большая (60S), и малая (40S) субчастицы лежат вблизи поверхности мембраны. На большой субчастице имеется выступ, вдающийся в мембрану (рис. 29.41). Шероховатый ЭР (в отличие от гладкого ЭР) содержит два трансмембранных белка, называемых рибофоринами, которые специфически взаимодействуют с большой рибосомной субчастицей.
Рис. 29.41. Связанная с мембраной рибосома. Это изображение низкого разрешения получено методом реконструкции на основе анализа ряда электронных микрофотографий упорядоченных рибосом, сделанных под различными углами

В связи с синтезом и дальнейшей судьбой белков, образованных на рибосомах ЭР, возникают три основных вопроса.
1. Существует ли два класса рибосом - свободные рибосомы цитозоля и связанные с мембранами рибосомы - или все рибосомы по сути одинаковы? Если существует только один класс рибосом, чем определяется, остается ли данная рибосома свободной или связывается с шероховатым ЭР?
2. Каким образом новообразованная полипептидная цепь, выходящая из связанной с мембраной рибосомы, преодолевает барьер проницаемости шероховатого ЭР? Например, такие секреторные белки, как проферменты поджелудочного сока (разд. 8.1), вскоре после синтеза обнаруживаются в полости ЭР.
3. Чем определяется судьба белка, синтезированного на связанной с мембраной рибосоме? Некоторые из этих белков экспортируются из клетки, тогда как другие предназначены для органелл внутри клетки. Кроме того, белки синтезированные шероховатым ЭР, обнаруживаются в качестве составной части плазматической и внутриклеточных мембран.