БИОЛОГИЯ Том 2 - руководство по общей биологии - 2004
17. КООРДИНАЦИЯ И РЕГУЛЯЦИЯ У ЖИВОТНЫХ
Раздражимость, или чувствительность — характерная черта всех живых организмов, означающая их способность реагировать на сигналы, или раздражители. Сигнал воспринимается рецептороми передается с помощью нервов и(или) гормонов к эффектору, который осуществляет специфическую реакцию, или ответ.
Животные в отличие от растений имеют две взаимосвязанные системы координации функций — нервную и эндокринную (гормональную). Сравнение их представлено в табл. 17.1. Разница между нервной и гормональной регуляцией хорошо прослеживается на примере регуляции секреции различных веществ в пищеварительном тракте (разд. 8.4). У животных и нервная, и гормональная системы развивались параллельно. У растений имеется только химическая координация функций, аналогичная эндокринной. Логично предположить, что дополнительное существование у животных нервной системы связано с особенностями их питания, а именно с потребностью в активном добывании пищи. Для этого же необходимы сенсорные и локомоторные органы, работа которых контролируется нервной системой.
Таблица 17.1. Сравнение нервной и гормональной регуляции у животных
Нервная регуляция |
Гормональная регуляция |
Электрическое и химическое проведение (нервные импульсы и нейромедиаторы в синапсах) |
Химическое проведение (гормоны) по кровеносной системе |
Быстрые проведение и ответ |
Более медленное проведение и отсроченный ответ (исключением является адреналин) |
В основном кратковременные изменения |
В основном долговременные изменения |
Специфический путь распространения сигнала (по нейронам) |
Неспецифический путь распространения (с кровью по всему телу) к специфической мишени |
Ответ часто узко локализован (например, одна мышца) |
Ответ может быть крайне генерализованным (например, рост) |
17.1. Нервная система
Нервная система состоит из высокоспециализированных клеток со следующими функциями:
1) восприятие средовых сигналов. У многоклеточных организмов для этого существуют модифицированные нервные клетки — рецепторы. Их структура и функция описаны в разд. 17.5;
2) преобразование сигналов в электрические импульсы — так называемая трансдукция;
3) проведение импульсов, часто на значительные расстояния, к другим специализированным клеткам — эффекторам, которые, получив сигнал, способны дать адекватный ответ. Структура и функция эффекторов вкратце описаны в разд. 17.5 и гл. 18.
Связь между рецепторами и эффекторами осуществляют особые клетки — нейроны. Они являются основными структурными и функциональными элементами нервной системы и их разветвленные отростки пронизывают все тело животного, образуя сложную сеть передачи сигналов.
Типы нейронов - резюме
Строение различных типов нервных клеток описано в разд. 6.6. Речь идет о сенсорных (афферентных), двигательных (эфферентных) и вставочных нейронах (рис. 6.27). Двигательные нейроны называют также мотонейронами, а вставочные нейроны — интернейронами. Во всех нервных клетках можно различить компактное тело (перикарион), содержащее ядро, и отходящие от тела тонкие отростки. Отросток, по которому нервные импульсы идут от перикариона, называется аксоном. Он оканчивается синаптическим вздутием, так называемой синаптической бляшкой. К перикариону импульсы поступают по дендрону, разделенному на тонкие ветви — дендриты, которые получают сигналы от других клеток нервной системы1. Многие аксоны окружены белково-липидной миелиновой оболочкой и называются миелинизированными. Иногда дендрон и аксон образуют единое волокно, отходящее от перикариона с одного бока. Другой особый тип нейронов — биполярный — описан в этой главе ниже. У него дендрон и аксон отходят от тела клетки с противоположных ее сторон.
1 Как правило, говоря об отростках нейрона, различают просто аксон и дендриты, поскольку во многих случаях границу между «дендроном» и перикарионом провести трудно. — Прим. перев.
17.1.1. Нервный импульс
Измерение электрической активности нейронов
То, что сигналы, вызывающие мышечное сокращение и секреторную активность желез, передаются по нейронам в форме электрических импульсов, известно уже более 200 лет. Однако механизм распространения этих импульсов был выяснен лишь в последние полвека, после того как у кальмара обнаружили аксоны толщиной около миллиметра. Такая толщина этих гигантских аксонов (они проводят импульсы, связанные с реакцией бегства) позволила вводить в них электроды и регистрировать импульсы, т. е. проводить электрофизиологические эксперименты.
На рис. 17.1 изображен прибор, используемый в настоящее время для изучения электрической активности нейронов. Его важнейшую часть составляет микроэлектрод — стеклянная трубочка, вытянутая на конце в тончайший капилляр диаметром 0,5 мкм и заполненная раствором электролита (например 3М КС1). Этот микроэлектрод вводят в аксон, а второй электрод, имеющий вид металлической пластинки, помещают в физиологический (солевой) раствор, омывающий нейрон. Оба электрода подсоединены к усилителю, замыкающему цепь. Сигнал, усиленный примерно в 1000 раз, передается на двухлучевой катодный осциллограф. Микроэлектрод перемещают с помощью микроманипулятора — специального устройства, снабженного винтами, напоминающими винты микроскопа. Вращая их, можно с большой точностью регулировать положение микроэлектрода.
Когда кончик микроэлектрода проходит сквозь плазматическую мембрану аксона, лучи осциллографа раздвигаются. Расстояние между лучами на экране показывает разность потенциалов между электродами в цепи. Разность потенциалов покоящейся клетки называется потенциалом покоя (см. ниже). В сенсорных клетках, нейронах и мышечных клетках измеряемая описанным способом величина меняется в зависимости от их активности, поэтому такие клетки называют возбудимыми. На мембранах всех остальных живых клеток тоже существует подобная разность потенциалов, известная как мембранный потенциал, но в этих клетках она остается постоянной, поэтому их называют невозбудимыми клетками.
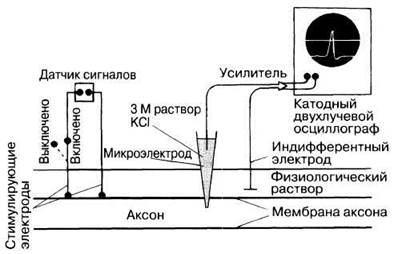
Рис. 17.1. Схема установки для регистрации электрической активности аксона изолированного нейрона. Датчик сигналов дает ток, генерирующий в аксоне потенциал действия, который воспринимается введенным в аксон микроэлектродом. Возникающий сигнал передается от него на двухлучевой катодный осциллограф.
Потенциал покоя
Разность потенциалов между наружной и внутренней поверхностями клеточной мембраны (трансмембранный потенциал) обычно, в том числе и у нейронов в покое, устанавливается таким образом, что внутренняя часть клетки заряжена отрицательно относительно окружающей ее среды. Этот феномен называют поляризацией мембраны. Потенциал покоя нейрона составляет примерно —70 мВ. Он поддерживается благодаря активному транспорту и диффузии ионов через мембрану, что было продемонстрировано Кертисом и Коулом в США и Ходжкином и Хаксли в Англии в конце тридцатых годов прошлого века на аксонах кальмара (табл. 17.2).
Таблица 17.2. Концентрация ионов (ммоль/л) во внеклеточной среде и внутриклеточной жидкости гигантского аксона кальмара (приблизительные значения из Hodgkin, 1958)
Ионы |
Вне клетки |
Внутри клетки |
К+ |
20 |
400 |
Na+ |
460 |
50 |
Cl- |
560 |
100 |
А- (органические анионы) |
0 |
370 |
В цитоплазме аксона (аксоплазме) больше ионов калия (К+) и меньше — натрия (Na+). В окружающей аксон среде наблюдается обратная картина, т. е. низкая концентрация К+ и высокая — Na+. (Распределение хлорид-ионов и других ионов в последующем описании не учитывается, поскольку оно не играет существенной роли в нервном проведении.) Таким образом, существуют трансмембранные электрохимические градиенты ионов, обусловленные их электрическими и химическими свойствами. Электрические свойства ионов определяются их зарядами: одноименные заряды отталкиваются, противоположные — притягиваются. На движение ионов влияет также их концентрация в растворе. Ион имеет тенденцию перемещаться по градиенту концентрации, т. е. туда, где она ниже. Результирующее движение зависит от соотношения зарядов и концентраций по обе стороны мембраны.
Потенциал покоя поддерживается активным транспортом ионов против их электрохимических градиентов с помощью натрий-калиевого (Na+, К+)-насоса. Он образован белками-пере- носчиками, встроенными в наружную клеточную мембрану (см. «Активный транспорт» в разд. 5.9.8 и рис. 5.21). Для работы этого насоса необходима энергия АТФ, а действует он по принципу антипорта: «выкачивание» трех ионов Na+ из аксона сопряжено с «закачиванием» в него двух ионов К+ (рис. 17.2).
Активному транспорту ионов противостоит их пассивная трансмембранная диффузия по электрохимическому градиенту через специфические ионные каналы, образованные особыми белками (см. рис. 17.2). Скорость этой диффузии определяется проницаемостью мембраны для данного иона. У аксона она в 20 раз выше для К+, чем для Na+. Следовательно, пассивная потеря аксоном К+ идет быстрее, чем пассивное поступление Na+ за счет диффузии. В результате в аксоне становится меньше катионов и создается отрицательный заряд. Это и есть потенциал покоя, величина которого определяется главным образом электрохимическим градиентом К+.
Теперь рассмотрим, как эти клетки генерируют нервные импульсы. В принципе нервные импульсы возникают при изменении проницаемости мембраны нервных клеток для К+ и Na+, что приводит к изменению разности потенциалов на мембране и к появлению так называемого потенциала действия.

Рис. 17.2. Активное и пассивное движение ионов через наружную мембрану аксона, приводящее к генерированию внутри него отрицательного потенциала, называемого потенциалом покоя. Активный транспорт обеспечивается натрий-калиевым насосом. Ионные каналы (каналообразующие белки) позволяют ионам пассивно перемещаться по их электрохимическим градиентам. Некоторые из этих каналов могут закрываться и открываться с помощью особых частей своих молекул — «ворот». Их закрытие вызывается, в частности, изменением трансмембранного электрического потенциала, как это происходит при распространении по аксону нервного импульса. Однако на эти изменения каналы реагируют с разной скоростью в зависимости от своих особенностей.
Потенциал действия
При стимуляции аксона электрическим током (рис. 17.3) потенциал на внутренней поверхности мембраны меняется с —70 на +40 мВ. Это изменение полярности носит название потенциаладействия и регистрируется на двухлучевом осциллографе в виде кривой, представленной на рис. 17.3.
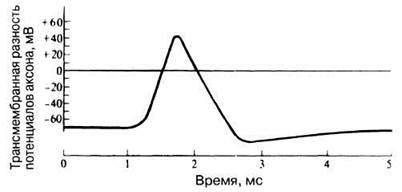
Рис. 17.3. Типичный потенциал действия в аксоне кальмара.
Причина такого явления — изменение натриевых каналов. Они (как и некоторые калиевые) снабжены воротами, т. е. могут открываться и закрываться особыми полипептидными цепями. При закрытых воротах проницаемость мембраны для ионов, проходящих через соответствующие каналы, падает, а при открытых — увеличивается. Когда клетка находится в состоянии покоя, натриевые ворота закрыты, поэтому ее мембрана в 20 раз более проницаема для ионов калия.
Потенциал действия возникает в результате внезапного кратковременного открывания натриевых ворот. Это происходит в ответ на сигнал, приводящий к пороговой деполяризации мембраны аксона, т. е. к уменьшению его трансмембранной разности потенциалов на небольшую, но достаточную для данной реакции величину. Открывание ворот увеличивает проницаемость мембраны для ионов натрия, и они поступают в клетку путем диффузии. Это увеличивает в ней количество положительных ионов, т. е. приводит к еще большей деполяризации: трансмембранный потенциал меняется с отрицательного до нулевого (полностью деполяризованное состояние), а затем становится положительным. Поскольку натриевые ворота чувствительны к деполяризации, в ходе нее их открывается все больше. Это в свою очередь усиливает поступление в клетку натрия и ведет к дальнейшей деполяризации. Таким образом, описанные два процесса стимулируют друг друга и развиваются по механизму так называемой положительной обратной связи. Происходит взрывообразное ускорение потока натрия внутрь аксона (важно помнить, что все эти события разворачиваются в течение тысячных долей секунды). Максимальная трансмембранная разность потенциалов достигает +40 мВ, как показано на рис. 17.4, А. Она соответствует максимальной концентрации ионов натрия внутри клетки. Амплитуда изменения разности потенциалов составляет от—70 до +40 мВ, т. е. равна 110 мВ. Как показывают расчеты, для этого нужно, чтобы в аксон поступило совсем небольшое количество ионов натрия — порядка одной миллионной доли уже находившихся внутри.
Вскоре после открывания натриевых ворот деполяризация мембраны заставляет открываться и калиевые ворота. В результате усиливается диффузия ионов калия из клетки (рис. 17.4, Б), а поскольку у них такой же заряд, как у ионов натрия, их выход делает внутреннюю среду аксона менее положительной — начинается процесс реполяризации, т. е. возвращения к исходному потенциалу покоя.
После достижения максимального уровня потенциала действия натриевые ворота начинают закрываться, и проницаемость мембраны для натрия снижается. Все это время натрий-калиевый насос не прекращает своей работы, в результате чего постепенно восстанавливается исходный потенциал покоя. Реполяризация приводит к снижению пика, или «спайка», потенциала действия (рис. 17.4, А) до исходного уровня. Фактически мембранный потенциал снижается до более отрицательного, чем в покое, значения. Происходит гиперполяризация, обусловленная тем, что калиевые ворота закрываются чуть позже натриевых, и клетка теряет через них «лишние» положительные заряды (ср. ход кривых для Na+ и К+ на рис. 17.4, Б). Однако ионы калия продолжают поступать в клетку, и постепенно восстанавливаются их трансмембранное электрохимическое равновесие и исходный потенциал покоя.
Из сказанного выше следует, что потенциал покоя определяется в основном ионами калия, а потенциал действия — ионами натрия (рис. 17.4).

Рис. 17.4. Изменения различных свойств наружной мембраны аксона при распространении по нему нервного импульса (потенциала действия). А. Изменения мембранного потенциала, т. е. изменения электрических свойств мембраны. Б. Изменения ионной проводимости. В. Суммарное распределение зарядов по обеим сторонам мембраны аксона во время возникновения потенциала действия.
Нервные импульсы представляют собой потенциалы действия, распространяющиеся вдоль аксона в виде волны деполяризации. Наружная поверхность аксона в месте возникновения потенциала действия заряжена отрицательно.
17.1. Назовите две причины стремительного поступления Na+ в аксон при повышении проницаемости мембраны аксона для Na+.
17.2. Если бы проницаемость мембраны для ионов натрия и калия увеличивалась одновременно, то как это сказалось бы на потенциале действия?
17.3. В 1949 г. Ходжкин и Катц исследовали влияние ионов натрия на возникновение потенциала действия в аксонах кальмара. Внутриклеточные микроэлектроды регистрировали потенциалы действия в аксонах, помещенных в изотонические растворы морской воды, содержащие разные концентрации ионов натрия. Результаты экспериментов приведены на рис. 17.5. Какие кривые соответствуют обычной морской воде и морской воде в разведениях 1:2 и 1:3? Объясните влияние этих растворов на потенциалы действия.

Рис. 17.5. Мембранные потенциалы в аксонах кальмара, помещенных в морскую воду с различной концентрацией ионов натрия.
Особенности потенциалов действия
РАСПРОСТРАНЕНИЕ (ПРОВЕДЕНИЕ) НЕРВНЫХ ИМПУЛЬСОВ. Нервный импульс представляет собой волну деполяризации, распространяющуюся по поверхности нейрона. Распространение происходит вследствие самогенерирования потенциалов действия за счет поступающих в аксон ионов натрия. Поступившие ионы натрия создают зону положительного заряда внутри клетки, что приводит к возникновению локальной электрической цепи, по которой течет местный ток между этой и соседней отрицательно заряженной зоной. Местный ток снижает мембранный потенциал в этой зоне, и в результате деполяризации здесь повышается проницаемость мембраны для натрия и в свою очередь генерируется потенциал действия. Последовательная деполяризация все новых и новых участков мембраны приводит к тому, что потенциал действия распространяется по аксону все дальше. Теоретически потенциалы действия могут передаваться на любые расстояния, иными словами, они не затухают. Причина этого кроется в том, что локальное изменение концентрации ионов в каждой точке обусловливает независимое самогенерирование потенциала действия. До тех пор пока снаружи и внутри аксона существует необходимая разница в концентрации ионов, потенциал действия в одной точке мембраны будет порождать потенциал действия в соседнем его участке.
ЗАКОН «ВСЕ ИЛИ НИЧЕГО» И КОДИРОВАНИЕ ИНТЕНСИВНОСТИ СИГНАЛА. Любое живое существо должно обладать каким-то механизмом, позволяющим различать силу получаемых сигналов. Один из теоретически возможных вариантов — это зависимость величины потенциала действия от силы сигнала. Для того чтобы проверить такой вариант, достаточно поставить опыт, в котором нейрон раздражают током разной силы, и измерить амплитуды возникающих в ответ потенциалов действия. Полученные результаты приведены на рис. 17.6. Можно видеть, что амплитуда потенциала действия не зависит от интенсивности сигнала, поэтому говорят, что потенциал действия подчиняется закону «все или ничего»; суть этого закона сводится к тому, что потенциал действия либо не возникает вовсе при низкой интенсивности сигнала, а коль скоро он возник, его амплитуда далее остается постоянной независимо от интенсивности сигнала. Иными словами, существует некая пороговая интенсивность сигнала, выше которой потенциал действия обязательно возникнет. Более того, показано, что постоянна и скорость распространения импульса по аксону.

Рис. 17.6. Ответ по типу «все или ничего». Чтобы в нейроне возник потенциал действия, раздражитель должен достигнуть некой «пороговой» силы. Дальнейшее увеличение силы раздражителя не приводит к увеличению амплитуды последующих потенциалов действия, однако при этом увеличивается частота их генерирования (на рисунке не показано).
Как же на самом деле организм различает силу раздражителя (сигнала)? Оказывается, что интенсивность сигнала влияет на число потенциалов действия, возникающих в единицу времени, т. е. чем сильнее сигнал (в определенных пределах), тем чаще генерируются нервные импульсы. Таким образом, речь идет о своего рода частотном коде.
Например, частота 10 имп/с в соответствующем аксоне поддерживает тонус (состояние частичного напряжения — готовности к быстрому действию) двуглавой мышцы (бицепса). Примерно 50 имп/с необходимы для ее нормального сокращения при движении руки. Большинство аксонов могут проводить сигналы в диапазоне 10—100 имп/с, хотя иногда в естественных условиях эта частота достигает 500 имп/с, а в экспериментальных условиях бывает еще больше.
СКОРОСТЬ ПРОВЕДЕНИЯ. У позвоночных подавляющая часть нервных волокон, особенно в спинномозговых и черепных нервах, окружены миелиновой оболочкой, образованной шванновскими клетками (рис. 6.30 и разд. 6.6.1). Миелин — это материал белково-липидной природы, обладающий высоким электрическим сопротивлением и действующий как изолятор, подобно резиновому или пластиковому покрытию электрического провода. Суммарное сопротивление мембраны аксона и миелиновой оболочки очень велико, но там, где в миелиновой оболочке имеются разрывы, называемые перехватами Ранвье, сопротивление току между аксоплазмой и внеклеточной жидкостью меньше. Только в этих участках замыкаются местные цепи, и именно здесь через мембрану аксона проходит ток, генерирующий следующий потенциал действия. В результате импульс перескакивает от одного перехвата Ранвье к другому и пробегает по миелинизированному аксону быстрее, чем серия меньших по величине местных токов в немиелинизированном нервном волокне. Такой способ распространения потенциала действия, называемый сальтаторным (от лат. saltare — прыгать), может обеспечивать проведение импульса со скоростью 120 м/с (рис. 17.7).
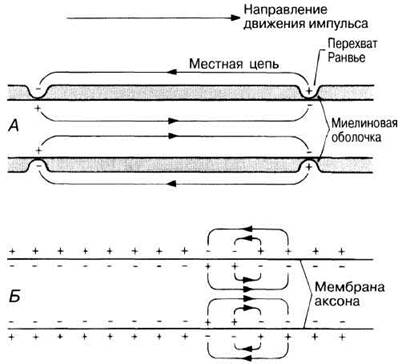
Рис. 17.7. Схема, объясняющая появление разных по протяженности местных цепей в миелинизированном (А) и немиелинизированном (Б) аксонах. В первом случае нервное проведение называют сальтаторным, т. е. скачкообразным, потому что потенциал действия быстро «перескакивает» между перехватами Ранвье.
В немиелинизированных аксонах, типичных для беспозвоночных, скорость распространения потенциалов действия зависит от сопротивления аксоплазмы. Это сопротивление в свою очередь зависит от диаметра аксона — чем меньше диаметр, тем больше сопротивление. В тонких аксонах (<0,1 мм) высокое сопротивление аксоплазмы влияет на проведение тока и снижает длину местных цепей, так что в них включаются только те участки, которые расположены непосредственно впереди потенциала действия. В результате скорость распространения импульсов в этих аксонах низка — всего около 0,5 м/с. Диаметр гигантских аксонов, свойственных многим кольчатым червям, членистоногим и моллюскам, равен примерно 1 мм, а скорость проведения по ним импульсов достигает 100 м/с. Этого вполне достаточно для передачи жизненно важной информации.
17.4. Объясните с точки зрения электрического сопротивления аксоплазмы и длины местных цепей, почему гигантские аксоны проводят импульсы быстрее, чем тонкие.
ВЛИЯНИЕ ТЕМПЕРАТУРЫ НА СКОРОСТЬ НЕРВНОГО ПРОВЕДЕНИЯ. По мере повышения температуры примерно до 40 °С скорость проведения импульсов возрастает.
17.5. Почему миелинизированные аксоны лягушки диаметром 3,5 мкм проводят импульсы со скоростью 30 м/с, тогда как аксоны кошки такого же диаметра - со скоростью 90 м/с?