Біофізика і біомеханіка - В. С. Антонюк - 2012
Розділ 3. МОЛЕКУЛЯРНА БІОФІЗИКА
3.3.Поняття нуклеїнових кислот. Їх основне призначення та біофізична функція
Нуклеїнові кислоти відкрив у 1869 р. Фрідеріх Мішер [7]. Понад 70 років інтерес до їх дослідження був незначний, і тільки після появи праць, у яких показано, що нуклеїнові кислоти відповідають за спадкову інформацію, і запропоновано механізм передавання спадкової інформації (модель подвійної спіралі ДНК Уотсона та Кріка), почали інтенсивно досліджувати нуклеїнові кислоти. Дві основні функції нуклеїнових кислот: 1) зберігання та передавання спадкової інформації; 2) біосинтез білків.
Структура мономерних компонентів нуклеїнових кислот. Нуклеїнові кислоти - це полімери, мономерними одиницями яких є нуклеотиди, які до того ж виконують інші функції в організмі (НАД, АДФ, цАМФ, АТФ тощо). Нуклеотид складається з трьох різних за хімічною природою сполук: гетероциклічної основи, вуглеводу та фосфорної кислоти. Гетероциклічні основи через атом азоту за допомогою утворення гліководного зв’язку з’єднані з вуглеводом з утворенням нуклеозиду.
Таким чином, утворюється п’ять нуклеозидів: аденозин (А), гуано- зин (Г), цитимін (Ц), тимідин (Т) та уридин (У). Перші чотири входять до складу ДНК. У РНК замість тимідину міститься уридин. Крім зазначених нуклеозидів до складу РНК і ДНК входять у невеликій кількості інші похідні пурину та піримідину.
Невеликі розбіжності в хімічній будові нуклеотидів призводять до істотних змін в їхній біологічній активності, тобто незначно відрізняючись хімічно, ці сполуки в організмі виконують принципово різні біологічні функції Наприклад, цАМФ регулює перебігання багатьох процесів, а АТФ є універсальним джерелом енергії в організмі (біосинтез різних сполук, м’язове скорочення тощо).
Найважливішою особливістю просторової будови нуклеозидів і нуклеотидів є взаємне розміщення залишків основ та вуглеводу, яке характеризується двома кутами.
Взаємне розміщення залишків основ та вуглеводів у нуклеотидах і нуклеозидах у розчині вивчається головним чином спектрополяриметричними методами та методом ядерного магнітного резонансу (ЯМР). У першому випадку вивчають ДОО чи КД розмірів нуклеозидів на ультрафіолетовій ділянці спектра, де в цих сполуках спостерігається характерний ефект Коттона.
Первинна структура нуклеїнових кислот. Послідовність нуклеотидів визначає первинну структуру нуклеїнових кислот (рис. 3.6, а). Отже, утворюються два класи нуклеїнових кислот: ДНК і РНК. Здебільшого генетичну інформацію містить ДНК, а у деяких вірусах - РНК. Полімери ДНК і РНК є лінійними. Майже всі РНК, за винятком деяких РНК вірусів, одноланцюгові, тим часом як ДНК майже всі дволанцюгові, побудовані за принципом комолементарності.
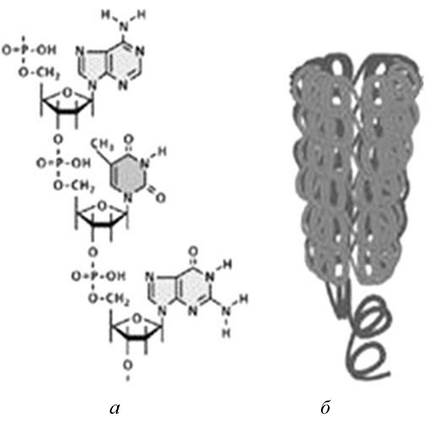
Рис. 3.6. Первинна (а) та вторинна (б) структури нуклеїнової кислоти
Довжина ланцюгів мононуклеїнових кислот не перевищує сотень мікрометрів. Найкоротші з транспортних мононуклеїнових кислот (тРНК), ступінь полімеризації яких становить 80. Найдовші РНК - це так звані гетерогенні ядерні РНК (гяРНК), містять до 2105 нуклеотидів. Довжина ДНК коливається в більш широких межах - від часток міліметра (декілька тисяч нуклеотидів) до сантиметрів (близько 109 нуклеотидів). Наприклад, молекули ДНК хромосоми людини містять 48...240 млн пар основ і мають довжину 1,6...8,2 см.
У нуклеїнових кислотах виявлено різноманітні типи структур [7]. Деякі з них тимчасові, тобто виникають унаслідок дії нуклеїнових кислот. Їх можна описати як одноланцюгові, дволанцюгові, дволанцюгові з одноланцюговими кінцями, розгалужені, циклічні одноланцюгові, циклічні дволанцюгові, структури типу катенанів.
Вторинна структура ДНК. Вторинну структуру ДНК запропонували Джеймс Уотсон, Френсіс Крік та Моріс Уілкінс (Нобелівська премія, 1962 р.) на основі узагальнення результатів вивчення нуклеїнових кислот та побудували модель ДНК у вигляді подвійної спіралі (рис. 3.6, б), а також висунули ідею про специфічну взаємодію комплементарних пар А і Т та Г і Ц.
Положення дифракційних максимумів (рефлексів) на рентгенограмі відповідає умові Вульфа-Бреггова: 2b sin φ = ηλ, де b - стала кристалічної ґратки (відстань між площинами); φ - кут дифракції; η = 0, 1, 2, 3... - порядок дифракції. На рентгенограмі ДНК виділяються дві сталі ґратки, які характеризують упорядковані структури, що розмішуються перпендикулярно до осі ДНК. Головна позитивна характеристика такої моделі полягає в її здатності пояснити, яким чином передається спадкова інформація.
Відновлення зруйнованої вторинної структури ДНК називається ренатурацією. Критеріями повноти ренатурації є збіжність: оптичних властивостей, гідродинамічних характеристик, рентгенограм.
Оптичні характеристики та гіперхромний ефект ДНК. Спектри поглинання ультрафіолетового світла мономерних нуклеозидів та нуклеотидів у разі нейтральних рН зливаються в одну широку смугу з λmax = 260 нм. Під час денатурації оптична густина ДНК збільшується приблизно на 30 %.
Явище отримало назву гіперхромного ефекту. Зворотний перехід, тобто збільшення поглинання ДНК під час ренатурації, називається гіпохромним ефектом:
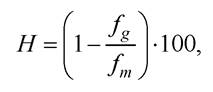
де fg і fm - сила осцилятора відповідно полімера та мономера, які безпосередньо залежать від величини моменту електронного переходу і визначені експериментально з площі смуги поглинання, що відповідає електронному переходу в спектрі.
Важливою властивістю подвійних спіралей ДНК є також значне питоме згортання площини поляризованого світла, яке приблизно в шість разів більше порівняно з мономерними нуклеотидами такої ж концентрації. Подвійна спіраль ДНК може бути зруйнована під дією різних факторів (зміна іонної сили, кислотності, температури). За деякими фізичними властивостями в цьому випадку спостерігається аналогія між спіраллю ДНК і кристалом: руйнування структур (плавлення) відбувається кооперативно за певної температури, а зростання кристала, чи ренатурація ДНК починається після утворення зародка.
Крім нуклеотидного складу, температура плавлення Тп ДНК залежить ще від багатьох факторів, з яких найбільш істотні такі:
- іонна сила: температура плавлення подвійних спіралей полінуклеотидів підвищується зі збільшенням іонної сили розчину. Наявність таких катіонів, як Cu, Cd, Pb зменшує температуру плавлення ДНК, тим часом як інші (Mg, Ba, Co, Mn, Ni, Zn) підвищують температуру плавлення ДНК;
- кислотність середовища: температура плавлення ДНК сильно залежить від кислотності. Якщо значення рН нижче ніж 7 і вище ніж 12, денатурація ДНК відбувається за кімнатної температури. В інтервалі рН від 5,5 до 8,5 температура плавлення ДНК мало залежить від рН середовища, вплив рН на температурну стабільність ДНК зумовлений іонізацією основ.
Біологічна функція нуклеїнових кислот:
- реплікація: кожна нитка подвійної спіралі ДНК є шаблоном для синтезу нових спіральних молекул ДНК, повністю тотожних вихідній молекулі;
- транскрипція: цей процес складається з декількох етапів. Перший етап - це реакція активування амінокислот та їх з’єднання з тРНК, другий - перенесення амінокислоти на тРНК. Далі тРНК бере участь у синтезі білка. Сполуку тРНК з амінокислотою цистеїном називають ферментом;
- трансляція - найскладніший багатоступеневий процес синтезу поліпептидного ланцюга. Трансляцію умовно поділяють на три стадії: ініціацію, елонгацію і термінацію.
Ґрунтуючись на загальних фізико-хімічних уявленнях про властивості білків і нуклеїнових кислот [7], можна виокремити такі типи взаємодій:
1) електростатичні взаємодії залишків фосфорної кислоти та аміногруп лізину і аргініну;
2) стекінг-взаємодії бокових груп ароматичних амінокислот та основ;
3) водневі зв’язки;
4) гідрофобні взаємодії неполярних амінокислот та основ.