Біофізика і біомеханіка - В. С. Антонюк - 2012
Розділ 3. МОЛЕКУЛЯРНА БІОФІЗИКА
3.4.Біологічні мембрани
3.4.1.Функції, структура та властивості біологічних мембран
Усі біологічні мембрани мають загальні структурні фрагменти. Вони є ансамблями ліпідних та білкових молекул, що утримуються разом за допомогою невалентних взаємодій. Товщина біологічних мембран становить 5...10 нм, проте їх частка в сухій масі клітин перевищує 50 %. Це пояснюється щільним пакованням компонентів мембран, а також їхвеликою сумарною площею. Основа структури мембрани - ліпідний бішар товщиною близько 5 нм. Клітинна мембрана містить ліпіди трьох типів: фосфоліпіди, холестерол та гліколіпіди. Усі вони є амфіпатичними молекулами, тобто мають гідрофільну та гідрофобну частини (рис. 3.7), які подані чотирма основними фосфоліпідами мембран тваринних клітин.
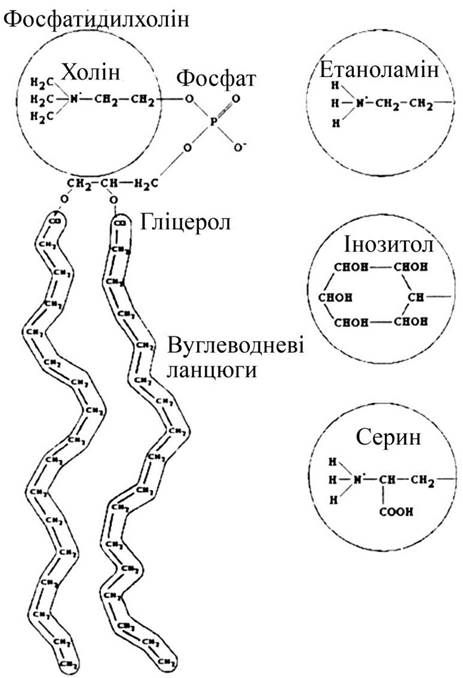
Рис. 3.7. Хімічна структура структурної організації, чотирьох основних фосфоліпідів, які містяться в плазматичних мембранах
Фосфоліпіди мають полярну ліофільну головку (яка добре взаємодіє з полярними розчинниками, зокрема з водою), заряджену негативно, і два гідрофобні вуглеводневі хвости (що не взаємодіють з водою). Один з хвостів зазвичай має одну або більше подвійних зв’язків (ненасичена жирна кислота), тоді як інший хвіст подвійних зв’язків не має (насичена жирна кислота).
Гідратовані ліпідні системи стабілізуються здебільшого в результаті гідрофобних взаємодій, а також за допомогою вандерваальсових сил між сусідніми гідрофобними ланцюгами та водневими зв’язками між полярними головками деяких ліпідів.
Під дією гідрофобних сил система набуває такої структурної організації, за якої неполярні ділянки ліпідних молекул контактують між собою, а не з водою. Ці сили мають ентропійну природу та обмежені пакованням молекул води навколо неполярних вуглеводнів.
Паковання молекул води складніше, але відомо, що воно стабілізується міжмолекулярними водневими зв’язками. У разі потрапляння неполярної молекули у воду порушується структура води навколо кожної молекули. Молекули води прагнуть орієнтуватися так, щоб збереглися міжмолекулярні водневі зв’язки. Таким чином, молекулам води доводиться набувати вищого ступеня впорядкованості (створювати структуру). Це призводить до зменшення ентропії системи. В результаті сумарна зміна вільної енергії для перенесення неполярної молекули з неполярного розчинника у воду термодинамічно невигідна через ентропійні ефекти, зумовлені порушенням структури води як розчинника. Термодинамічна невигідність взаємодії неполярних молекул з водою і є проявом гідрофобних сил.
У водному розчині ліпіди, що мають один жирнокислотний залишок, утворюють міцели (рис. 3.8), а в мембрані - гідрофільні пори, через які здатні проходити молекули води та іони, для яких в нормі проникність мембрани мала. Зміна проникності мембрани ДЛЯ речовин може призвести до порушення функціонування та загибель клітини. Іонізувальне випромінювання підсилює процеси перекисного окиснення ліпідів, а отже, сприяє утворенню пор, що є одним з механізмів ураження клітини під дією випромінювання. У результаті утворюється подвійний шар (бішар), в якому жирнокислотні хвости розміщені всередині шару, а полярні головки напрямлені назовні. Такі мембрани формують замкнені бульбашки - ліпосоми (або мультиламелярні везикули рис. 3.9), а також стабільні плоскі подвійні шари.
Рис. 3.8. Міцела
Ліпосоми використовують передусім як модельні системи, в які можна вбудовувати різні білки, а також у фармакології для створення систем транспортування лікарських препаратів в уражені тканини. Лікарську речовину поміщають у таку ліпідну капсулу для уникнення розбавлення в крові.
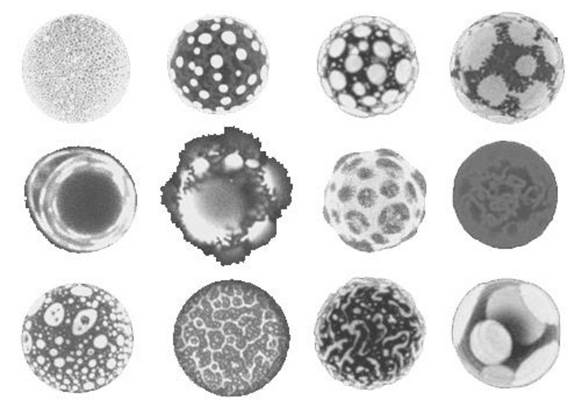
Рис. 3.9. Зовнішній вигляд сферичних ліпосом
Ліпіди активно беруть участь у процесах, що перебігають у мембранах. Вони утворюють стабільний бішар, у якому функціонують білки; деякі ліпіди беруть участь у процесах біосинтезу, інші - є важливими біорегуляторами; окремі ліпіди потрібні для підтримання активності ряду ферментів.
Гангліозиди, наприклад, відіграють важливу роль у регуляції зростання клітин, є специфічними рецепторами плазматичних мембран і відповідальні за клітинну адгезію.
Мембрани містять велику кількість різних білків. Їх кількість така велика, що поверхневий натяг мембрани ближчий до величини поверхневого натягу на межі розділу білок-вода (10 Н/м), ніж ліпід-вода (10 Н/м). Концентрація мембранних білків залежить від виду клітини.
Білки, що входять до складу мембран за їх положенням у мембрані поділяють на периферичні (зовнішні) та інтегральні (які проникають у мембрану). Багато мембранних білків є трансмембранними і повністю пронизують ліпідний бішар. Периферічні білки зв’язані з поверхнею мембрани слабкими електростатичними взаємодіями з полярними головками ліпідних молекул, або з молекулами інших білків. Інтегральні білки зв’язуються з ліпідами переважно невалентними гідрофобними взаємодіями. Проте є приклади ковалентного зв’язку мембранних білків ліпідами. Багато білків плазматичних мембран рослинних і тваринних клітин (наприклад, глікофорин) належать до класу глікопротеїнів. Вуглеводневі залишки цих білків розміщені із зовнішнього боку плазматичної мембрани.
За функціональними характеристиками можна виділити структурні транспортні, регуляторні, ферментативні, рецепторні білки та ін. Саме білки забезпечують унікальність функцій кожної мембрани. З ферментативних білків, головними є аденозинтрифосфорні кислоти (АТФ). Крім них, у мембранах окремих клітин можуть бути інші ферменти (флавіни, цитохроми, дегідрогеназа тощо), які беруть активну участь у метаболізмі клітин. Співвідношення між кількістю білків та ліпідів у мембрані неоднакове і залежить від функціонального призначення клітини. Так, у мембранах еритроцитів 75 % площі займають ліпіди, а 25 % - білки. У мембранах деяких бактерій білків у 5-6 разів більше, ніж ліпідів, а в мієліновій мембрані навпаки - білків у 2,6 разу менше, ніж ліпідів.
Ще в 1925 р. Гортер і Грендел припустили, що ліпіди в мембрані еритроцитів утворюють бімолекулярний шар. Ця концепція була надалі розвинута в запропонованій в 1935 р. моделі Девсона-Данієлі, або моделі «сендвіча», в якій передбачалося, що білки покривають поверхню ліпідного бішару (рис. 3.10, а).
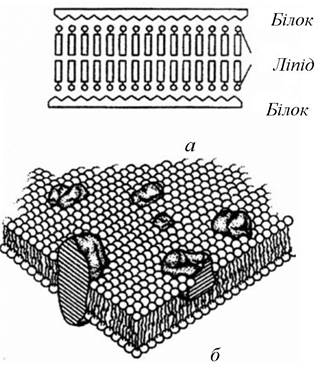
Рис. 3.10. Моделі структурної організації біологічних мембран: а - модель Девсона-Данієлі; б - модель рідинно-мозаїчної мембрани Сингера та Ніколсона
Експериментальні дані, отримані за допомогою дифракції рентгенівських променів і електронної мікроскопії, підтвердили її адекватність [35; 38].
Проте електронно-мікроскопічні дослідження із застосуванням методу заморожування-сколювання показали, що в мембрани вбудовані глобулярні частинки - білки. Причому для мембранних білків характерний високий вміст α-спіралей, і вони утворюють глобули, а не поділяються у вигляді моношару на поверхні ліпідного бішару.
У 1972 р. Сингер та Ніколсон створили рідинно-мозаїчну модель. Мембрана цієї моделі являє собою плинний фосфоліпідний бішар, у який занурено вільно дифундувальні білки (рис. 3.10, б).
Отже, згідно із сучасними уявленнями [24] клітинні мембрани є мозаїчними структурами, що містять у замкненому подвійному шарі ліпідні молекули, орієнтовані білкові молекули, гліколіпіди, глікопротеїни та полісахариди.
Біофізика мембран вивчає структуру біологічних мембран, транспорт речовин через них, генерацію та поширення нервового імпульсу, процеси рецепції та перетворення енергії, більшість яких перебігають на біомембранах.
Біологічні мембрани виконують в організмі такі функції: обмежують клітину (плазмалеми) і клітинні органели, які розділяють клітину на окремі ділянки (компартаменти), що дозволяє підтримувати нерівноважний стан організму; формують міжклітинні контакти; забезпечують механічний захист клітин, виборчий і регульований транспорт речовин, проведення нервового імпульсу; беруть участь у синтезі АТФ, забезпечують оптимальне розміщення в просторі мембранних білків, а також роботу рецепторів та імунної системи.