ФІЗІОЛОГІЯ ТА БІОХІМІЯ РОСЛИН
Опорний конспект лекцій
6. ДИХАННЯ РОСЛИН
Утворені в результаті фотосинтезу цукри та інші органічні сполуки використовуються клітинами рослинного організму як поживні речовини. Найважливішим етапом живлення органічними речовинами на клітинному рівні виступає процес дихання.
Клітинне дихання - це окиснюючий (з участю кисню) розпад органічних поживних речовин, що супроводжується утворенням хімічно активних метаболітів і звільненням енергії, які використовуються клітиною для процесів життєдіяльності.
Загальні положення та рівняння дихання
У природі існують два основні процеси, у ході яких енергія сонячного світла, що була акумульована рослиною в органічній речовині, звільняється, це - дихання та бродіння.
Дихання - це аеробний окиснювальний розпад органічних сполук на прості, неорганічні, що супроводжується виділенням енергії.
Бродіння - анаеробний процес розпаду органічних речовин на простіші (органічні), що також супроводжується виділенням енергії.
У разі дихання акцептором електронів в окисно-відновних реакціях є кисень, тоді як під час бродіння - органічні сполуки.
Наукові основи про роль О2 в диханні були закладені працями А. Лавуазьє, Я. Інгенхауза, І. Бородіна, О. Баха, К. Енглера. У другій половині 19 ст. спільними зусиллями вчених запропоновано загальне рівняння цього процесу:
С6Н12О6 + 6О2 = 6СО2 + 6Н2О + Е (2875 кДж/моль).
Одночасно О.М. Бах наголошував на тому, що біологічне окиснення пов'язане з відніманням від субстрату електронів чи протонів.
Ця гіпотеза О.М. Баха надалі була розвинена В.І. Палладіним у струнку теорію хімізму дихання. Положення його теорії про анаеробну й аеробну фази дихання та про роль води у цих процесах повністю підтвердилися.
Основні положення теорії біологічного окиснення (теорії Баха-Палладіна):
✵ обов’язковим учасником дихання є вода;
✵ вода разом із субстратом окиснення виконує функцію донора водню;
✵ у процесі дихання беруть участь специфічні активатори водню, які вилучають водень із субстрату;
✵ перші етапи дихання є анаеробними і не вимагають наявності молекулярного кисню;
✵ молекулярний кисень необхідний на завершальному етапі дихання для регенерації акцепторів водню з утворенням води.
Експериментальні дані про участь води в окисненні субстрату дихання й роль О2 як кінцевого акцептора водню були отримані у 50-х рр. минулого століття і висвітлені в працях Б. Вартапетяна й А. Курсанова.
Завдяки дослідженням Костичева, Нейберга стало очевидно, що дихання та всі види бродіння пов'язані між собою через піровиноградну кислоту і що існує генетичний зв'язок між диханням та бродінням.
Дихання є одним із проявів обміну речовин між організмом і навколишнім середовищем, у результаті чого відбувається генерування енергії у вигляді АТФ, відновлювальних еквівалентів (НАД-Н2, НАДФ-Н2) та формування проміжних продуктів для різноманітних біосинтетичних реакцій рослинного організму. Процес дихання складається з трьох етапів:
✵ гліколізу,
✵ циклу трикарбонових кислот (цикл Кребса),
✵ дихального ланцюга.
На перших двох етапах (гліколіз, цикл трикарбонових кислот) відбувається відновлення коферментів (НАД·Н2, НАДФ·Н2), які на третьому етапі окиснюються киснем повітря в дихальному ланцюзі мітохондрій.
Внаслідок дихання в організмі виникає взаємозв’язок між розкладом і синтезом основних хімічних сполук, які беруть участь у процесах обміну. Також відбувається газообмін із навколишнім середовищем: кисень поглинається, а виділяється вуглекислий газ.
Основні шляхи окиснення дихальних субстратів
Окиснення субстратів (S) у ході дихання здійснюється ферментами (ф). Ферменти, як біокаталізатори, мають декілька особливостей: високу активність, специфічність та лабільність. Ці властивості забезпечують можливість тонкої регуляції обміну речовин на рівні ферментів.
Існує 4 способи окиснення:
1. віднімання е- (Fe2+ → Fe3+);
2. віднімання водню (гідрохінон → хінон + 2е- + 2Н+);
3. приєднання О2 (2Н2 + О2→ 2Н2О);
4. утворення проміжної гідратованої сполуки з подальшим відніманням двох електронів і протонів:
СН3 — СОН + Н2О → СН3 - СН(ОН)2→ (-2е-, -2Н+) СН3СООН
Оксидоредуктази
Оскільки окиснення однієї речовини - Д (донора е- чи Н+) пов'язане з відновленням іншої сполуки - А (їх акцептора), то ферменти, які каталізують ці реакції, називають окисно-відновними ферментами, або оксидоредуктазами. Усі вони належать до першого класу ферментів і поділяються на 17 підкласів:
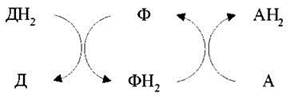
Існує декілька груп оксидоредуктаз: анаеробні дегідрогенази, аеробні дегідрогенази, оксидази та оксигенази.
Анаеробні дегідрогенази - передають електрони різним проміжним акцепторам, але не О2. Це двокомпонентні ферменти, коферментом яких може бути НАД+ (алкоголь-, лактат-, малатдегідрогенази) або НАДФ+ (ізоцитрат-, глюкозофосфатдегідрогенази). При окисненні субстрату НАД+ (НАДФ+) перетворюється у відновлену форму НАДН (НАДФН), а другий протон субстрату дисоціює у середовище. Окислені й відновлені форми коферментів анаеробних дегідрогеназ можуть взаємоперетворюватися:
НАД1Н + НАД2+⇔ НАД1+ + НАД2Н.
Анаеробні дегідрогенази передають водень, тобто е- і Н+, різним проміжним переносникам і аеробним дегідрогеназам.
Аеробні дегідрогенази - транспортуванняють е- до різних акцепторів, в тому числі й до О2. Це також двокомпонентні ферменти - флавопротеїни. Крім білка, до їхнього складу входить міцно зв'язана простетична група - похідне рибофлавіну (вітамін В2).
Розрізняють два коферменти цієї групи: флавінмононуклеотид (ФМН), або жовтий дихальний фермент Варбурга, і флавінаденіндинуклеотид (ФАД) (сукцинатдегідрогеназа). Активною групою цих ферментів є ізоаллоксазин. Акцептори електронів для аеробних дегідрогеназ - це хінони, цитохроми, О2.
Оксидази - здатні передавати е- лише кисню. При цьому утворюється:
вода - на О2 переноситься 4е- (цитохромоксидаза, поліфенолоксидаза);
пероксид водню - на О2 переноситься 2е- (флавопротеїнові оксидази);
супероксидний аніон кисню (О-2) - на О2 переноситься 1е- (ксантиноксидаза).
Н2О2 і О-2 - токсичні і в клітинах швидко трансформуються на воду й кисень. Серед оксидаз важливу роль відіграють залізовмісні ферменти й переносники, які належать до цитохромної системи. До неї входять цитохроми (в, с1, с) і цитохромоксидаза (цит. а+а3). Уся система передає е- від флавопротеїнів на молекулу кисню. В ланцюгу дихання напрям передачі е- визначається величиною окисно-відновного потенціалу цитохромів:
цит. в → цит. с1 → цит. с → цит. а+а3→ О2.
Усі компоненти цитохромної системи містять залізопорфіринову простетичну групу. Інгібіторами цитохромоксидази є СО, ціанід, азид. У рослинних мітохондріях існує оксидаза, яка не пригнічується цими речовинами і називається альтернативною оксидазою.
Рослинні тканини містять також немітохондріальні оксидази:
- поліфенолоксидаза (перенос електронів і протонів від фенолів на кисень);
- аскорбатоксидаза (окиснює аскорбінову кислоту до дегідроаскорбінової кислоти);
- група пероксидаз (використовують як окиснювач пероксид водню: АН2 + Н2О2→ А + 2Н2О; можуть функціонувати як оксидази, або анаеробні дегідрогенази);
- каталаза (розкладає пероксид з утворенням молекулярного кисню: 2Н2О2 → 2Н2О + О2 ↑).
Оксигенази - активують кисень, у результаті чого він сполучається з органічними речовинами:
- диоксигенази приєднують два атоми кисню;
- гідроксилази приєднують один атом кисню (монооксигенази).
Донором е- для оксигеназ слугують НАД(Ф)Н, ФАДН2 та ін. сполуки. Ці ферменти беруть участь у гідроксилюванні багатьох ендогенних сполук (амінокислот, фенолів, стеринів), а також у детоксикації чужорідних токсичних речовин.
Гідроксилази здійснюють реакцію гідроксилювання за схемою:
АН + О2 + ДН2→ АОН + Д + Н2О.
Диоксигенази приєднують два атоми кисню в найрізноманітніші групи:
НАН + О2→ НО-А-ОН
НО-А-ОН + О2→ НОО-А-ООН
А + О2 +ДН2→ НО-А-ОН + Д та ін.
Гліколіз
Гліколіз - процес анаеробного розпаду глюкози, що проходить із вивільненням Е, кінцевим продуктом якого є піровиноградна кислота (ПВК). Гліколіз - загальний спільний етап аеробного дихання і всіх видів бродіння.
Реакції гліколізу протікають у розчинній частині цитоплазми і в хлоропластах. У цитозолі гліколітичні ферменти організовані в мультиензимні комплекси на активних філаментах цитоскелету, що забезпечує векторність процесу. Англійський біохімік А. Гарден і російський фізіолог Л. Іванов установили, що глюкоза піддається анаеробному розпаду лише після фосфорилювання. Повністю весь процес гліколізу розшифрували німецькі біохіміки Г. Ембден і О. Меєргоф та радянський біохімік Я. Парнас.
Етапи гліколізу (біохімія процесу)
Ланцюг реакцій гліколізу можна розподілити на три етапи.
1. Підготовчий етап - фосфорилювання гексози та її розщеплення на дві фосфотріози. Глюкоза (піранозна форма молекули) фосфорилюється АТФ з участю гексокінази, перетворюючись у глюкозо-6-фосфат, який ізомеризується глюкозофосфатізомеразою у фруктозо-6-фосфат. Цей перехід необхідний для утворення більш лабільної фуранозної форми молекули гексози. Фруктозо-6- фосфат фосфорилюється за участю АТФ фосфофруктокіназою. В результаті утворюється фруктозо-1,6-дифосфат.
Фруктозо-1,6-дифосфат - лабільна форма із симетрично розміщеними фосфатними групами, що несуть від'ємний заряд і відштовхуються один від одного електростатично. Така структура легко розщеплюється альдолазою. Таким чином, суть підготовчого етапу полягає в активації стабільної глюкози за рахунок подвійного фосфорилювання і переходу у фуранозну форму з подальшим розпадом на 3-фосфогліцериновий альдегід (3ФГА) і фосфодіоксіацетон (ФДА), які легко перетворюються один в одного (тріозофосфатізомераза).
2. Перше субстратне фосфорилювання, яке починається з 3ФГА і завершується утворенням 3-фосфогліцеринової кислоти (3ФГК).
Фермент дегідрогеназа фосфогліцеринового альдегіду (НАД-залежний БН- фермент) утворює з 3ФГА фермент-субстратний комплекс, в якому відбувається окиснення субстрату та передача е- і Н+ на НАД+. У ході окиснення ФГА у фермент-субстратному комплексі виникає меркаптанний високоенергетичний зв’язок (зв’язок із високою вільною енергією гідролізу).
Фосфороліз цього зв'язку звільняє SH-фермент, а до залишку карбоксильної групи субстрату приєднується неорганічний фосфат (зберігаючи Е окиснення 3ФГА). В результаті утворюється 1,3-диФГК.
Високоенергетична фосфатна група з допомогою фосфогліцераткінази передається на АДФ і утворюються АТФ і 3ФГК.
Таким чином, на другому етапі гліколізу на кожну окиснену тріозу синтезуються 1 молекула АТФ і 1 молекула відновленого НАДН.
3. Друге субстратне фосфорилювання, при якому 3ФГК за рахунок внутрішньомолекулярного окиснення віддає фосфат з утворенням АТФ.
3ФГК за допомогою фосфогліцератмутази перетворюється в 2ФГК. Дальше енолаза каталізує відщеплення молекули води від 2ФГК, що супроводжується перерозподілом Е в молекулі. В результаті цього утворюється фосфоенолпіруват - сполука, яка містить високоенергетичний фосфатний зв'язок. Цей фосфат з участю піруваткінази передається на АДФ, а енолпіруват переходить до більш стабільної форми - піруват.
Енергетичний вихід гліколізу
На 2 і 3-му етапах утворюється 4 мол. АТФ і 2 мол. НАДН, на першому етапі витрачається 2 мол. АТФ. Окиснення 1 мол. НАДН = синтезу 3-х мол. АТФ. Таким чином, у процесі гліколізу утворюється 8 молекул АТФ.
Вільна енергія гідролізу 1 молекули АТФ = 41, 87 кДж/моль (10 ккал), а 8 молекул АТФ дають 335 кДж/моль (80 ккал).
Зворотність гліколізу визначається зворотністю дії більшості ферментів. Однак реакції фосфорилювання глюкози й фруктози, а також реакція утворення піровиноградної кислоти, які здійснюються за допомогою кіназ, вимагають затрати енергії макроергічних зв’язків. На цих ділянках зворотний процес може відбуватися завдяки використання обхідних шляхів.
Функції гліколізу в клітині:
- здійснює зв'язок між субстратами дихання й циклом Кребса;
- постачає на потреби клітини АТФ і НАДН (в умовах аноксії - основне джерело АТФ);
- продукує інтермедіати, необхідні для синтетичних процесів у клітині;
- у хлоропластах - дає АТФ; метаболізує крохмаль у тріози, які експортуються до цитозолю.
Цикл Кребса
Враховуючи результати своїх попередників (Т. Тунберга, А. Сент-Дьєрди) та власні дослідження, англійський біохімік Г.А. Кребс запропонував схему окиснення ди- і трикарбонових кислот до СО2 через »цикл лимонної кислоти» за рахунок віднімання водню. Таким чином у 1937 р. на тваринних об'єктах був відкритий цикл Кребса, а в 1939 р. англійським дослідником А. Чібнелом була доведена його наявність у рослин.
У циклі Кребса при наявності кисню піруват повністю окиснюється до СО2 і Н2О. Усі ділянки цього процесу локалізовані в матриксі або на внутрішній поверхні мітохондрій. Виділяють 8 етапів.
1) Безпосередньо в циклі окиснюється не сам піруват, а його похідне - ацетил-КоА. Тому перший етап - це утворення активного ацетилу в ході окисного декарбоксилювання. Цей процес здійснюється з участю піруватдегідрогеназного мультиферментного комплексу (входять 3 ферменти і 5 коферментів: тіамінпірофосфат, ліпоєва кислота, коензими А, ФАД і НАД+). У ході складних перетворень через проміжні сполуки з коферментами із ПВК утворюються ацетил-КоА (що містить високоенергетичний тіоефірний зв'язок), СО2 і НАДН.
2) Цикл Кребса починається із взаємодії ацетил-КоА з енольною формою щавлево-оцтової кислоти (оксалоацетату), які при дії цитратсинтази перетворюються в лимонну кислоту. При цьому витрачається Е тіоефірного зв'язку.
3) Наступний етап циклу містить дві реакції і каталізується ферментом аконітатгідратазою:
- перша - в результаті дегідратації лимонної кислоти (цитрату) утворюється цис-аконітова;
- друга - аконітат гідратується і синтезується ізолимонна кислота.
4) Ізолимонна кислота під дією НАД-залежної ізоцитратдегідрогенази окиснюється в нестійку сполуку - щавлевобурштинову кислоту (оксалосукцинат), яка декарбоксилюється з утворенням α-кетоглутарової кислоти.
5) α-кетоглутарат піддається реакції окиснювального декарбоксилювання → α-кетоглутарат-дегідрогеназний мультиферментний комплекс — у результаті чого виділяється СО2, утворюється НАДН і сукциніл-КоА - високоенергетичний тіоефір.
5’) За участю сукциніл-КоА-синтетази із сукцинілу-КоА, АДФ і Н3РО4 утворюється бурштинова кислота, АТФ (субстратне фосфорилювання), регенерує молекула КоА.
6) Бурштинова кислота (сукцинат) окиснюється до фумарової - ФАД- залежна сукцинатдегідрогеназа.
7) Фумарова кислота при дії фумаратгідратази, приєднуючи Н2О, перетворюється в яблучну (малат).
8) Яблучна кислота з допомогою НАД-залежної малатдегідрогенази окиснюється в щавлевооцтову, яка самочинно переходить в енольну форму, реагуючи з черговою молекулою ацетил-КоА, і цикл повторюється.
Цикл Кребса практично незворотний, оскільки в ньому є дві сильно екзергонічні реакції - цитрат-синтетазна [2-га реакція] і сукциніл-КоА-синтетазна [5-та реакція]. Протягом одного обороту циклу при окисненні пірувату виділяється 3 молекули СО2 [1, 4, 5 реакції], відбувається залучення 3-х молекул Н2О [2, 5', 7 реакції] і видалення 5-ти пар атомів водню [1, 4, 5, 6, 8 реакції].
Значення та енергетичний вихід
Цикл Кребса відіграє дуже важливу роль в обміні речовин рослинного організму. Він служить кінцевим етапом окиснення не лише вуглеводів, але й білків, жирів та інших сполук. У ході реакцій циклу звільняється основна кількість енергії, яка міститься в субстраті, і більша її частина утилізується у високоенергетичних фосфатних зв’язках.
У ході окиснення пірувату мають місце 5 дегідрувань, при цьому утворюються 3НАДН [1, 5, 8 реакції], НАДФН [4 реакція] і ФАДН2 [6 реакція] (1ФАДН2 = 2АТФ), + 1 мол. АТФ при субстратному фосфорилюванні (5’ реакція) → всього 15 молекул АТФ, а для 2-х молекул ПВК = 30 молекул АТФ.
Отже, при окисненні глюкози в процесі дихання за функціонування гліколізу й циклу Кребса утворюється 38 молекул АТФ, що дорівнює 1591 кДж/моль (380 ккал/моль). Це становить 55% усієї енергії глюкози.
Значення циклу Кребса цим не вичерпується. Багато проміжних продуктів циклу використовується для синтезу різноманітних сполук (амінокислот, жирів, вуглеводів, поліізопренів і т. д.)
Цикл Кребса займає центральне місце в метаболізмі клітини. Через нього встановлюється зв'язок між обміном трьох найважливіших груп сполук - білків, жирів і вуглеводів.
Гліоксилатний цикл
Вперше описаний у 1957 р. Г. Корнбергом, Г. Кребсом. Відсутній у тварин. Гліоксилатний цикл можна розглядати як модифікацію циклу Кребса. Функціонує в проростаючому насінні олійних культур і в тих об'єктах, де запасні жири перетворюються в цукри (глюконеогенез).
Схема циклу:

Гліоксилатний цикл (цикл гліоксилової кислоти) локалізований у спеціальних мікротілах — гліоксисомах. У циклі беруть участь дві молекули ацетил-КоА і перша використовується для синтезу бурштиновоної кислоти. Бурштинова кислота виходить з гліоксисом, перетворюється на ЩОК і бере участь у глюконеогенезі (зворотній гліколіз) та інших біохімічних процесах. Цикл містить, як мінімум, 6 реакцій.
Гліоксилатний цикл дозволяє утилізувати запасні жири, при розпаді яких утворюється велика кількість молекул ацетил-КоА. Крім цього, на кожні 2 молекули ацетил-КоА в гліоксилатному циклі відновлюється 1 молекула НАДН.
Пентозофосфатний шлях окиснення глюкози (ПФШ)
У рослинних клітинах існує ще один спосіб метаболізму гексоз - пентозофосфатний шлях (ПФШ), або апотомічне окиснення.
Усі реакції протікають у розчинній частині цитоплазми клітини, у пропластидах і хлоропластах. Цей шлях особливо активний у тих клітинах, де інтенсивно проходять синтетичні процеси. При ПФШ АТФ не утворюється.
Етапи ПФШ
І. Окиснення глюкози - каталізується дегідрогеназнодекарбоксилюючою системою, яка складається з трьох ферментів:
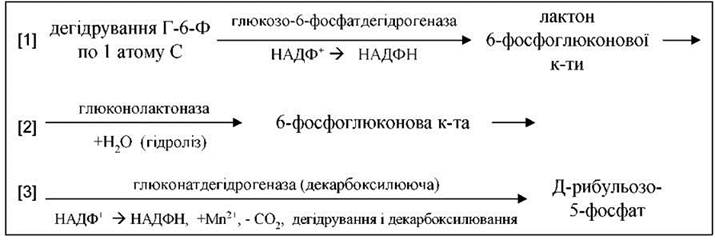
Таким чином, при окисненні кожного атома вуглецю (дегідрування) утворюється два НАДФН.
ІІ. Рекомбінація сахарів для регенерації вихідного субстрату.
З рибульозо-5-фосфату під дією епімерази утворюється ксилульозо-5-фосфат, а під дією ізомерази - рибозо-5-фосфат.
Рекомбінація цукрів з участю транскетолази і трансальдолази призводить до появи 3-ФГА і седогептульозо-7-фосфату, потім еритрозо-4-фосфату й фруктозо-6-фосфату.
Нарешті утворюються фруктозо-6-фосфати, які ізомеризуються (гексозофосфатізомераза) у глюкозо-6-фосфат.
Вкінці з шести молекул глюкозо-6-фосфату регенерує п’ять молекул глюкозо-6- фосфату. Сумарне рівняння ПФШ має такий вигляд:
6Глюкозо6Ф +12 НАДФ+ + 7Н2О → 5Глюкозо6Ф + 6СО2 + 12НАДФН + 12Н+ + Н3РО4
Енергетичний вихід ПФШ і його значення
При апотомічному окисненні глюкозо-6-Ф утворюється НАДФН, який окиснюється повільніше, ніж НАДН. Зазвичай атоми водню передаються з НАДФН на НАД+, а лише потім - до електронно-транспортного ланцюга.
Енергетичний вихід ПФШ = 12НАДФН = 12 · 3 АТФ = 36 АТФ. Однак головне значення ПФШ не в енергетичному, а в пластичному обміні. Тут можна виділити декілька аспектів:
1) ПФШ служить головним немітохондріальним джерелом НАДФН, який використовується переважно в синтетичних реакціях (синтез жирів, ізопреноїдів, відновлення SН-сполук).
2) У ході ПФ циклу синтезуються пентози, які входять до складу нуклеотидів, АТФ, коферментів НАД+, ФАД, коферменту А та ін. сполук.
3) ПФШ є джерелом вуглеводів із різною кількістю вуглецевих атомів - від С3 до С7, які є попередниками ароматичних амінокислот, вітамінів, дубильних, ростових та ін. речовин.
4) Компоненти ПФШ беруть участь у темновій фіксації СО2. ПФШ є, по суті, зворотним циклом Кальвіна.
5) У хлоропластах ПФШ у темноті постачає НАДФН, а також 3ФГК і, т.ч., АТФ, підтримуючи їх кількість на певному рівні.
Окиснення глюкози по ПФШ йде 12-ма реакціями, а дихотомічний (гліколітичний) шлях через ПВК охоплює більше 30 реакцій. Усі ці цикли й шляхи між собою пов'язані.
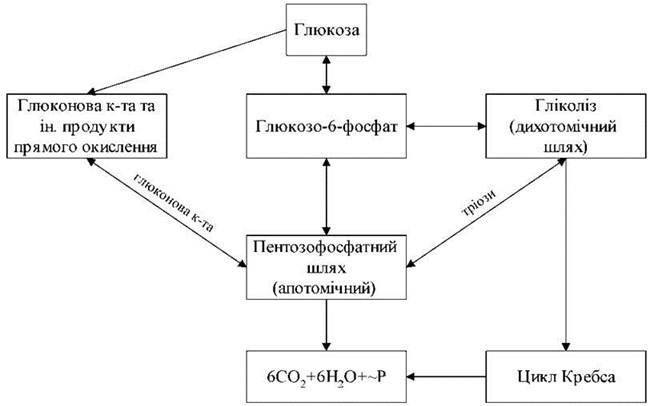
Рис. 15. Взаємозв'язок різних шляхів дисиміляції глюкози.
Пряме окиснення цукрів
У бактерій, грибів, тварин і водоростей виявлено шлях прямого окиснення глюкози без фосфорилювання.
Окиснення глюкози до глюконової килоти здійснюється специфічною ФАД- залежною оксидазою. Глюконова кислота через фосфорилювання і низку перетворень розпадається на тріози, які можуть поступати до інших циклів (цикл Кребса, ПФШ).
Взаємозв'язок різних шляхів дисиміляції глюкози
Біохімічні перетворення при диханні - гліколіз, цикл Кребса, ПФШ, пряме окиснення цукрів - система взаємопов'язаних процесів. На малюнку 1. представлена схема цих взаємозв'язків.
У клітині гліколіз і ПФШ просторово не роз’єднані, мають спільні субстрати. В нормі частка ПФШ у загальному обміні дихання становить приблизно 10-40 % і залежить від типу тканини і її стану.
В анаеробних умовах гліколіз домінує, а в хлоропластах активність апотомічного шляху окиснення вища. Активність ПФШ збільшується і при несприятливих умовах. У цитоплазмі велика частина продуктів ПФШ метаболізується через гліколіз.