БОТАНИКА ТОМ 2 - ФИЗИОЛОГИЯ РАСТЕНИЙ - 2007
6. ФИЗИОЛОГИЯ ОБМЕНА ВЕЩЕСТВ
6.9. Хемоавтотрофия
К хемоавтотрофным организмам (см. табл. 6.1) относятся исключительно прокариоты, лишенные хлорофилла (бактерии и некоторые архебактерии, которые восстанавливают СО2при помощи Н2). Хемо- автотрофы используют разность электрохимических потенциалов неорганических окислительно-восстановительных реакций для производства АТФ, первичными донорами электронов являются также неорганические вещества. Вещества, подлежащие окислению, поглощаются из среды клетками, которые затем выделяют продукты окисления обратно.
Хемоавтотрофные организмы отличаются от фотоавтотрофных способом производства АТФ и НАДН + Н+. В то время как у хемоавтотрофных бактерий метаболизм углерода точно такой же, как и у автотрофных, либо очень на него похож, архебактерии занимают особое положение. У них отсутствует цикл Кальвина, поэтому в дальнейшем мы будем останавливаться только на транспорте электронов и связанном с ним фосфорилировании у хемоавтотрофов.
6.9.1. Поставляющие энергию реакции
• Нитрификация. Нитрифицирующие бактерии являются строгими аэробами и окисляют NH3 или NH+4 с промежуточным образованием нитрита до нитрата (см. рис. 6.87). При этом работают две группы бактерий, тесно связанные экологически: виды нитрозогруппы (например, Nitrosomonas) преобразуют NH3 в нитрит, виды нитрогруппы (например, Nitrobacter) — нитрит в нитрат:
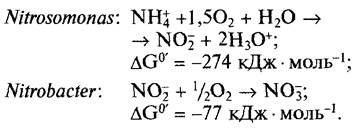
Тесное сотрудничество этих двух родов (парабиоз), с одной стороны, необходимо потому, что Nitrosomonas поставляет для Nitrobacter субстрат, а с другой стороны, также потому, что нитрит для Nitrosomonas (как и для других организмов) ядовит Немедленное удаление выделенного нитрита осуществляется во время нитрификации благодаря тому, что Nitrobacterнамного «голоднее», чем Nitrosomonas, ему для производства того же количества энергии необходимо переработать гораздо больше субстрата. Нитрифицирующие бактерии в почве сосуществуют с бактериями гниения, которые высвобождают NН+4 из органического материала. Нитрификация — важнейший почвенный процесс для производства нитрата, который является основным источником азота для высших растений. При недостатке кислорода в насыщенных водой почвах нитрификация затормаживается, но она возможна у поверхности корней, которые снабжаются кислородом при помощи межклетников и аэренхимы и частично выделяют его в окружающую среду
• Окисление серы. Богатая формами группа бесцветных серных бактерий обитает, например, в насыщенных питательными веществами лужах со стоячей водой, прежде всего на оросительных полях, предназначенных для очистки сточных вод. Они могут окислять соединения серы, например, образующийся в процессе разложения органического материала или при восстановлении сульфата Н2S (при бактериальном восстановлении сульфата в глубоких, бедных кислородом зонах Черного моря)
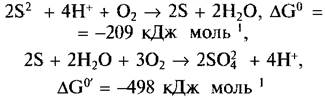
Эта реакция проводится, например, цианобактерией Веggiatoa и бактерией Тhiothrix, которые также временно запасают в клетках элементарную серу Виды в большинстве облигатного хемоавтотрофного рода Тhiobacillus окисляют различные соединения серы до сульфата. Наряду с Н2S, сульфидами и серой эти бактерии окисляют также сульфит (SО2-3), тиосульфат (S2O2-3), ди-, три- и тетратионаты (S2O2-6, S3О26, S4O26) и тиоцианат (SCN ), поэтому в очистке промышленных сточных вод естественным способом они играют очень важную роль Тhiobacillus thiooxidans, производя огромные количества Н2SO4, легко переносит высокую кислотность (до 1 Н серной кислоты)
• Бактерии, окисляющие железо и марганец.
Виды рода Thiobacillus (например, T ferrooxi- dans) окисляют двухвалентное железо
![]()
Что касается давно известных железобактерий Galhonetta ferruginea и Leptothrix ochracea, то еще не вполне понятно, являются ли они настоящими хемоавтотрофами или только запасают соединения железа. Поскольку окисление железа дает очень мало энергии, перерабатываются колоссальные объемы субстрата, железобактерии, например, принимают участие в образовании бурого железняка
Марганцевые бактерии (например, Pedomicrobium manganicum) окисляют Мn2+ до соответственно Мn4+.
Распространенные в почве водородные бактерии, в отличие от нитрифицирующих, некоторых тиобацилл и ферробацилл, являются не облигатными, а факультативными автотрофами, они могут питаться также органическими соединениями Некоторые виды родов Pseudomonas (например, Р facilis) и Alcalgenes (например, A eutrophus) окисляют с помощью гидрогеназы молекулярный водород (реакция, аналогичная взрыву гремучего газа)
![]()
Метанобактерии (например, Methilomonas) окисляют метан до СО, еще одна группа бактерий — СО до СО2, а именно аэробы (например, Pseudomonas carboxydovorans) и анаэробы (например, Rhodopseudomonas gelatinosa).
Анаэробы, метанобразующие бактерии, используют для восстановления СO2 водород, который появляется в результате деятельности Н2-продуцирующих микроорганизмов или из геохимических источников.
6.9.2. Транспорт электронов и фосфорилирование в хемосинтезе
Окислительно-восстановительные потенциалы субстратов у хемоавтотрофов очень сильно различаются, этим объясняется и большое различие у разных форм электрон-транспортных цепей. Как правило, в них задействованы, по- видимому, цитохромы с-типа и цитохромоксидаза (исключение составляют архебактерии, не имеющие цитохрома) Конечным акцептором электронов у аэробных форм служит кислород, а у анаэробов — окисленное неорганическое соединение (например, SO2-4, NO-3). В процессе транспорта электронов синтезируется АТФ, поэтому формально преобразование энергии в хемосинтезе похоже на фосфорилирование в дыхательных цепях (6.10.3.3). Однако электрон- транспортные цепи при хемосинтезе и при дыхании различны и могут находиться в одних и тех же клетках рядом друг с другом. АТФ, полученная хемосинтетически, используется для фиксации СO2.
В качестве восстановителя для СO2 хемоавтотрофы, как и фотоавтотрофы, используют НАДН + Н+. Электроны для восстановления НАД+ также заимствуются из соответствующего неорганического субстрата хемосинтезирующих организмов. Чем более отрицателен окислительно-восстановительный потенциал донора по сравнению с таковым НАД+ (Е0' = -0,32 В), тем меньше сложностей возникает на пути переноса электронов (например, при использовании Н2 в качестве субстрата). Если же окислительно-восстановительный потенциал больше -0,32 В (например, Е0' = +0,77 В для Fе2+/Fе3+), то транспорт электронов начинает использовать энергию в форме АТФ. Последняя наряду с АТФ, необходимой для фиксации СO2, появляется в результате окислительной реакции.
Субстраты поставляют электроны, а не протоны, поэтому нужные для восстановления НАД+ протоны дает вода. Она не теряет электроны, поэтому не подвергается окислительному расщеплению.