Фізіологія людини - Вільям Ф. Ґанонґ 2002
Ендокринна система, метаболізм і репродуктивна функція
Статева диференціація і розвиток
Жіноча статева система - Регулювання функцій яєчників
Гіпофізарний ФСГ відповідає за раннє дозрівання фолікулів у яєчниках, а разом з ЛГ - за їхнє остаточне дозрівання. Від спалаху виділення ЛГ (див. рис. 23-30) залежить овуляція та початок формування жовтого тіла. Зазначимо також, що виділення ФСГ дещо зростає в середині циклу. Значення цього до кінця не з’ясовано. ЛГ стимулює виділення естрогену і прогестерону жовтим тілом.
Гіпоталамічні компоненти
Гіпоталамус відіграє ключову роль у регулюванні виділення гонадотропіну. Гіпоталамічне регулювання полягає у впливі на виділення ГнРГ в портальні гіпофізарні судини (див. Розділ 14). ГнРГ стимулює виділення як ФСГ, так і ЛГ. Малоймовірно, що є спеціальний ФРГ.
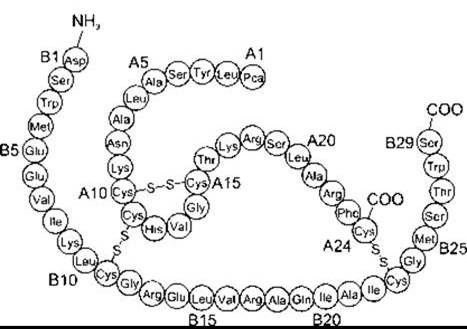
Рис. 23-36. Структура лютеїнового та спермального релаксину людини. Простежується подібність зі структурою інсуліну, ІФР-І, ІФР-ІІ (див. рис. 22-9); Рса-піроглютамінова кислота (модифіковано і відтворено за дозволом з Winslow JW et al; Human seminal relaxin is a product of the same gene as human luteal relaxin. Endocrinology 1992; 130:2660).
У нормі виділення ГнРГ відбувається епізодичними спалахами, які спричинюють епізодичні піки секреції ЛГ (див. вище). Вони потрібні для нормального виділення гонадотропінів. Якщо ГнРГ призначають для постійного введення, то кількість рецепторів до ГнРГ у передній частці гіпофіза зменшується (див. Розділ 1), і виділення ЛГ прямує до нуля. Проте якщо ГнРГ призначають епізодично з розрахунку одна доза за годину, то це стимулює виділення ЛГ, що відбувається навіть тоді, коли секреція ендогенного ГнРГ припиняється внаслідок ураження вентрального гіпоталамуса.
Тепер зрозуміло, що не тільки епізодичне виділення ГнРГ є загальним явищем, а також коливання частоти та амплітуди спалахів виділення ГнРГ важливі у виникненні інших гормональних змін, відповідальних за місячний цикл. Частоту виділення збільшують естрогени і зменшують прогестерон і тестостерон. Частота зростає у пізній фолікулярній фазі циклу, що веде до підвищеного виділення ЛГ. Під час секреторної фази частота зменшується внаслідок дії прогестерону (рис. 23-37), однак якщо виділення естрогену і прогестерону зменшується наприкінці циклу, то частота знову збільшується.
Під час ЛГ-хвилі у середині циклу чутливість гонадотропінів до ГнРГ значно зростає (внаслідок власної незахищеності до кількості ГнРГ) з частотою, яка є в цей час. Цей ефект самоіндукції ГнРГ важливий для забезпечення максимальної відповіді ЛГ.
Усе ще не з’ясована природа і точна локалізація генератора ГнРГ у гіпоталамусі. У загальних рисах відомо, що норадреналін і, очевидно, адреналін збільшують частоту виділення ГнРГ у гіпоталамусі, і навпаки, опіоїдні пептиди, такі як енкефаліни і ß-ендорфін, зменшують її. Зменшення кількості гіпофізарних рецепторів і, відповідно, виділення ЛГ, зумовленого постійним підвищенням ГнРГ, веде до використання аналогів ГнРГ тривалої дії для пригнічення виділень ЛГ у разі передчасного статевого дозрівання та раку простати (див. нижче).

Рис. 23-37. Епізодичне виділення ЛГ і ФСГ під час фолікулярної (угорі) і лютеїнової (унизу) стадій місячного циклу. Цифри біля кожного графіка означають кількість виділень ЛГ за 12 год, а також концентрації естрадіолу Е2 і прогестерону П у плазмі під час цих двох періодів циклу (відтворено за дозволом з Marshall JC, Kelch RO: Gonadotropin-releasing hormone: role of pulsatile secretion in the regulation of reproduction. N Engl J Med 1986; 315:1459).
Зворотний зв’язок
Зміни рівнів ЛГ, ФСГ, статевих стероїдів та інгібіну в плазмі під час місячного циклу показано на рис. 23-30, а шляхи їхнього зворотного зв’язку - на рис. 23-38. Під час початкової стадії фолікулярної фази рівень інгібіну В низький, а ФСГ помірно підвищений, що сприяє росту фолікула. Виділення ЛГ стримуване шляхом негативного зворотного зв’язку на фоні зростання рівня естрогену у плазмі. На 36-48-й годині до овуляції зворотний зв’язок естрогену стає позитивним, і це зумовлює спалах виділення ЛГ, що спричинює овуляцію. Овуляція відбувається через 9 год після максимального рівня ЛГ. Виділення ФСГ також максимально зростає, незважаючи на незначне збільшення інгібіну, очевидно, завдяки сильному стимулюванню гонадотропінів ГнРГ. Під час лютеїнової фази виділення ЛГ і ФСГ є низьким завдяки високим концентраціям естрогену, прогестерону та інгібіну.
Зазначимо, що помірний постійний рівень циркулювального естрогену має негативний зворотний ефект на виділення ЛГ, тоді як під час циклу підвищений його рівень має позитивний зворотний ефект і стимулює виділення ЛГ. Виявлено, що у мавп також є мінімальний час підвищення рівня естрогену для позитивного зворотного зв’язку. Зі збільшенням циркулювального естрогену до близько 300% за 24 год виявлено тільки негативний зворотний зв’язок; та якщо він збільшувався на 300% за 36 год чи більше, то після короткочасного зменшення виділень наставав спалах секреції ЛГ, що подібне до підвищення всередині циклу. У випадку високого рівня циркулювального прогестерону пригнічується позитивний зворотний ефект естрогенів. Є докази, що у приматів як негативний, так і позитивний ефекти естрогенів відбуваються у медіобазальному гіпоталамусі, проте не з’ясовано, як саме у лютеїнову фазу негативний зворотний зв’язок стає спочатку позитивним, а далі - знову негативним.
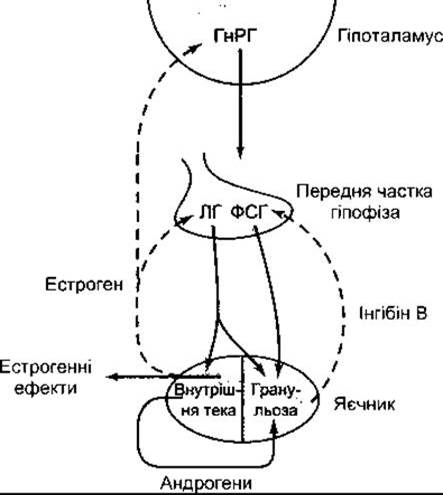
Рис. 23-38. Регулювання функції яєчників шляхом зворотного зв’язку. Клітини внутрішньої теки постачають андрогени до клітин ґранульози і клітини теки, що продукують циркулювальні естрогени, які пригнічують виділення ГнРГ, ЛГ і ФСГ. Інгібін, який походить з клітин ґранульози, пригнічує виділення ФСГ. ЛГ регулює клітини теки, тоді як клітини ґранульози регульовані ЛГ і ФСГ. Штриховими лініями позначено інгібіторну дію, а суцільними - стимулювальну. Порівняйте з рис. 18-13, 20-20, 22-11 і 23-24.
Регулювання циклу
Важливе значення має те, що регресія жовтого тіла (лютеолізис), яка починається за три-чотири дні до місячної, Є ключем місячного циклу. ПГF2a є фізіологічним лютеолізином, однак цей простагландин активований за наявності ендотеліальних клітин, які продукують ЕТ-1 (див. Розділ 31). Тому лютеолізис, принаймні у деяких видів, спричинюваний поєднаною дією ПГF2а і ЕТ-1. У деяких домашніх тварин окситоцин, що його виділяє жовте тіло, має локальний лютеолітичний ефект, очевидно, тому, що зумовлює виділення простагландинів. Коли починається лютеолізис, рівні естрогену та прогестерону знижуються, а секреція ФСГ та ЛГ посилюється. Розвивається новий набір фолікулів, а далі внаслідок дії ФСГ і ЛГ з них дозріває один домінантний. Приблизно всередині циклу збільшується виділення естрогену з фолікула, що підвищує чутливість гіпофіза до ГнРГ і спричинює хвилю виділення ЛГ. Після овуляції формується жовте тіло, послаблюється виділення естрогену, однак далі одночасно підвищуються рівні прогестерону та естрогену разом із інгібіном В. Підвищені рівні тимчасово пригнічують виділення ФСГ і ЛГ, проте знову настає лютеолізис, і починається новий цикл.
Рефлекторна овуляція
Самки котів, зайців, норок і деяких інших тварин мають тривалі періоди еструсу, під час яких овуляція настає тільки після копуляції. Таку рефлекторну овуляцію зумовлюють аферентні імпульси зі статевих органів, очей, вух і носа, які сходяться у вентральному гіпоталамусі і стимулюють виділення ЛГ з гіпофіза, що спричинює овуляцію. У таких видів, як щурі, мавпи, а також у людини овуляція відбувається самовільно і періодично, однак у цьому процесі задіяні також нейромеханізми. У щурів овуляцію можна затримати на 24 год, призначивши пентобарбітал чи інші нейроактивні ліки за 12 год до очікуваного розриву фолікула. У жінок на місячний цикл значно впливають емоційні подразники.
Контрацепція
Методи, які широко використовують для запобігання заплідненню, а також їхні недоліки, перелічені у табл. 23-8. Якщо запліднення відбулося, то викидень можна спровокувати за допомогою такого антагоніста прогестерону, як міфепристон (див. вище). Чоловіча контрацепція розглянута в іншій частині цього розділу.
Уведення сторонніх тіл у матку спричинює зміни тривалості статевого циклу у багатьох ссавців. У людини такі сторонні тіла не змінюють місячного циклу, однак діють як ефективний контрацептивний засіб. Внутрішньоматкову імплантацію шматків металу чи пластику (внутрішньо- маткові спіралі (ВМС)) використовували у програмах контролю за збільшенням кількості населення. Хоча механізм дії ВМС поки що до кінця не з’ясований, уважають, що загалом вони запобігають заплідненню яйцеклітини сперматозоїдом. Ті з них, які містять мідь, мають сперматоцидну дію. ВМС, які повільно виділяють прогестерон чи синтетичні прогестини, мають додатковий ефект загущення цервікального слизу, що перешкоджає проникненню сперматозоїдів у матку. ВМС можуть зумовлювати внутрішньоматкові інфекції, однак це трапляється переважно у перший місяць після їхнього введення та у жінок із захворюваннями, що передаються статевим шляхом. Жінки, які піддаються довготривалому лікуванню високими дозами естрогенів, не мають овуляцій, очевидно, тому, що у них пригнічене виділення ФСГ, і простежуються численні нерегулярні спалахи виділення ЛГ, а не одне максимальне виділення посередині циклу. Жінки, яких лікують такими самими дозами естрогенів разом із прогестагенами, не овулюють, оскільки в них пригнічене виділення обох гонадотропінів. Крім того, прогестини сприяють загущенню цервікального слизу, що перешкоджає рухові сперматозоїдів та заплідненню. Для пероральної контрацепції використовують такий естроген, як етинілестрадіол (див. рис. 23-34) у поєднанні з синтетичним прогестином - норетиндроном. Таблетки призначають на 21- й день з перервою на п’ять-сім днів, щоб пропустити місячну кровотечу, після чого їх знову треба приймати. Як і етинілестрадіол, норетиндрон має етинільну групу у 17- му положенні стероїдного ядра. Тому він резистентний до печінкового метаболізму і його можна призначати для перорального застосування. Водночас, будучи прогестином, він частково метаболізується до етинілестрадіолу, і тому також має естрогенову активність. З’ясовано, що ефективними є як низькі, так і високі дози естрогенів (див. табл. 23-8). Використання малих доз зменшує ризик тромбозів та інших ускладнень. Прогестини також можна застосовувати з метою контрацепції, хоча вони ефективніші у поєднанні з естрогенами.
Таблиця 23-8. Відносна ефективність контрацептивних методів, які найчастіше використовують1
Кількість вагітностей |
|
Метод |
на 100 жінок/рік |
Вазектомія |
0,02 |
Перев’язування труб і подібні |
0,13 |
процедури |
|
Оральні контрацептиви |
|
>50 мкг естрогену і прогестину |
0,32 |
<50 мкг естрогену і прогестину |
0,27 |
Тільки прогестин |
1,2 |
ВМС |
|
Cooper 7 |
1,5 |
Loop D |
1,3 |
Діафрагма |
1,9 |
Презерватив |
3,6 |
Перерваний статевий акт |
6,7 |
Спермациди |
11,9 |
Ритмічний |
15,5 |
1 Відтворено за дозволом з Vessey М, Lawless М, Yeates D: Efficacy of different contraceptive methods. Lancet 1982; 1:841).
Імплантати, виготовлені із прогестинів, таких як левоноргестрел, теж почали широко використовувати. Їх уводять під шкіру, що дає змогу запобігати настанню вагітності протягом п’яти років. Однак вони часто спричинюють аменорею, та поза цим ефективні, і їх добре переносять.