Фізіологія людини - Вільям Ф. Ґанонґ 2002
Функції нервової системи
Стан тривоги, сон та електрична активність мозку
Фізіологічна основа ЕЕГ, свідомості та сну
ЕЕГ є записом електричної активності невральних одиниць кори в об’ємному провіднику (див. Розділ 2). Зазвичай її записують від шкіри голови або черепа, тому вона має значно менший вольтаж, ніж у випадку, якби записували безпосередньо з кори головного мозку. Як зазначено вище, записування з поверхні кори чи шкіри голови реєструє позитивну хвилю, якщо струм напрямлений до електрода, і негативну, якщо цей напрям від поверхні.
![]()
Рис. 11-5. ЕЕГ кори кролика, показано стан реакції тривоги, зумовлений нюховим подразником.
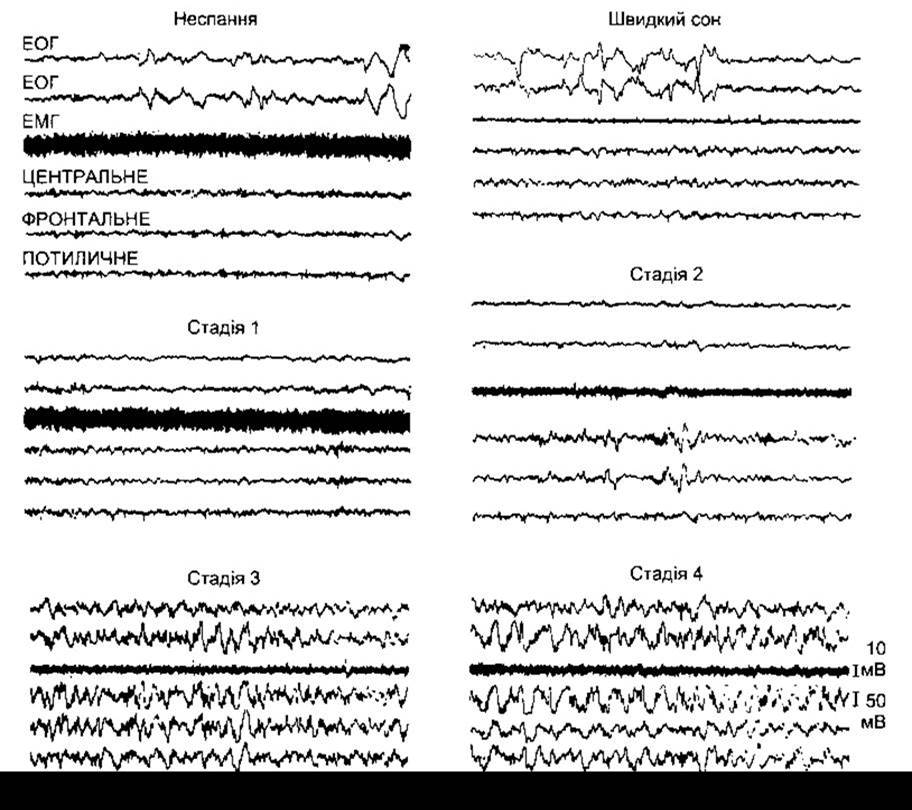
Рис. 11-6. ЕЕГ та м’язова активність під час різних стадій сну. ЕОГ - електроокулограма, що реєструє рухи очей; ЕМГ - електроміограма, що реєструє активність скелетних м’язів; ЦЕНТРАЛЬНЕ, ФРОНТАЛЬНЕ, ПОТИЛИЧНЕ розташування трьох електродів ЕЕГ. Зверніть увагу на низький м’язовий тонус поряд з екстенсивними рухами очей у разі швидкого сну (відтворено за дозволом з Kales A et al: Sleep and dreams: Recent research on clinical aspects. Ann Intern Med. 1968;68:1078).
Диполі кори
У всіх випадках наявність хвиль на ЕЕГ свідчить про те, що активність у ділянці кори головного мозку, виміряна ЕЕГ, то підвищується, то знижується. Однак якби активність була хаотичною, то не виникали б розряди, і, як наслідок, хвилі. Впливу цих ритмів на поведінкові стани і навіть на свідомість досі не з’ясовано. Водночас є серйозні докази того, що ці хвилі зумовлені осциляційною активністю в корі та коливаннями у механізмах зворотного зв’язку між таламусом і корою.
Дендрити клітин кори - це деревоподібні однаково орієнтовані, щільно укладені одиниці в поверхневих шарах кори головного мозку (див. рис. 11-1). Поширювані потенціали можуть генеруватися у дендритах (див. Розділ 4). Окрім того, на дендритах у поверхневих шарах закінчуються зворотні колатералі аксонів. Щоправда, дендрити переважно є місцем непоширювальних гіпополяризувальних місцевих потенціалів. Коли збуджувальні та гальмівні закінчення на дендритах кожної клітини стають активними, то вони стають джерелом або приймачем біострумів для решти дендритних відростків і тіла клітини. Отже, між клітиною та дендритом є постійно змінна двополярність. Потік імпульсів у цьому диполюсі виробляє хвилеподібні коливання потенціалу в об’ємному провіднику (рис. 11-7). Якщо загальна дендритна активність від’ємна щодо клітини, то клітина стає гіпополяризованою та гіперзбудливою, якщо ж вона позитивна, то клітина гіперполяризована й менш збудлива. Дві інші частини ЦНС, у яких багато складних паралельних дендритних відростків розташовані під м’якою мозковою оболонкою над шаром клітин, - це кора головного мозку та морський коник. На обидвох ділянках простежується характерне ритмічне коливання поверхневого потенціалу, подібне до того, яке спостерігають на кірковій ЕЕГ.
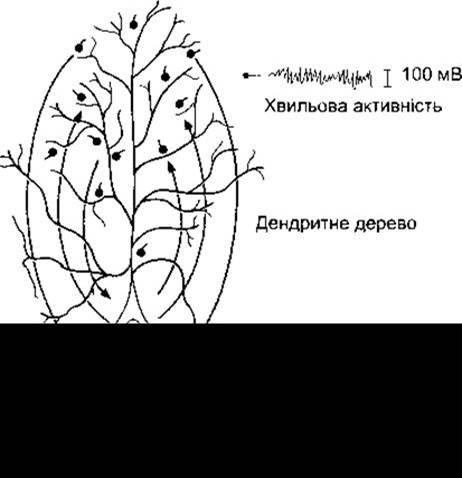
Рис. 11-7. Схематичне порівняння електричних реакцій аксона та дендритів великого кіркового нейрона. Потік біопотенціалів через активні синаптичні бляшки на дендритах зумовлює хвильову активність, тоді як «все або нічого» потенціали дії переходять уздовж аксона.
Таламокіркові коливання
Ще одним джерелом хвиль ЕЕГ є зворотна коливальна активність між серединними ядрами таламуса та корою головного мозку (рис. 11 -8). Нейрони таламуса гіперполяризовані і змінюють заряд лише у веретеноподібних фазних спалахах під час повільнохвильового сну. У стані свідомості вони частково деполяризовані і тонічно «спалахують» з великою швидкістю. Це пов’язано з вищою швидкістю «спалахування» кіркових нейронів.
Стан нейронів таламуса змінюється з гіперполяризованого фазного «спалахування» на деполяризоване тонічне внаслідок сенсорного подразнення, що зумовлює збудження. І навпаки, стан нейронів змінюється від деполяризації до гіперполяризації шляхом стимулювання зон сну (див. нижче). Є підстави вважати: якщо нейрони гіперполяризовані і «спалахують» тільки під час фазового вибуху, то активність у таламокіркових коливаннях запобігає прийманню чи опрацюванню нейронами кори специфічних вхідних сигналів.
Механізми, що зумовлюють ЕЕГ збудження
Заміна ритмічного типу ЕЕГ низьковольтною високою активністю відбувається внаслідок стимулювання специфічних сенсорних систем до рівня середнього мозку. Водночас стимулювання цих систем над середнім мозком, подразнення специфічних сенсорних релейних ядер таламуса чи стимулювання самих приймальних ділянок кори не спричинює реакції тривоги. З іншого боку, високочастотне стимулювання середньомозкової ретикулярної формації зумовлює ЕЕГ реакцію тривоги (рис. 11-9) і пробуджує сплячу тварину. Значні двосторонні ушкодження бічної та верхньої ділянок середнього мозку, що переривають медіальні петлі й інші висхідні специфічні сенсорні системи, не запобігають появі «тривожної» ЕЕГ, спричиненої сенсорними подразненнями, натомість ураження в покришці середнього мозку, що впливають на РАС, у разі неушкоджених специфічних систем, пов’язані з повільнохвильовим синхронізованим типом ритму, на який не діють сенсорні подразнення. Тварини з першим типом ушкодження перебувають у стані неспання, з другим - у стані коми впродовж тривалого періоду. Пацієнти з ушкодженням, що перериває РАС, також перебувають у стані сну чи коми. Отже, висхідна активність, що відповідає за ЕЕГ реакцію тривоги, внаслідок сенсорних подразнень надходить через специфічні сенсорні системи до середнього мозку, потрапляє до РАС через колатералі і через внутрішньоламінарні ядра таламуса та неспецифічну таламічну систему проекцій - до кори великого мозку.
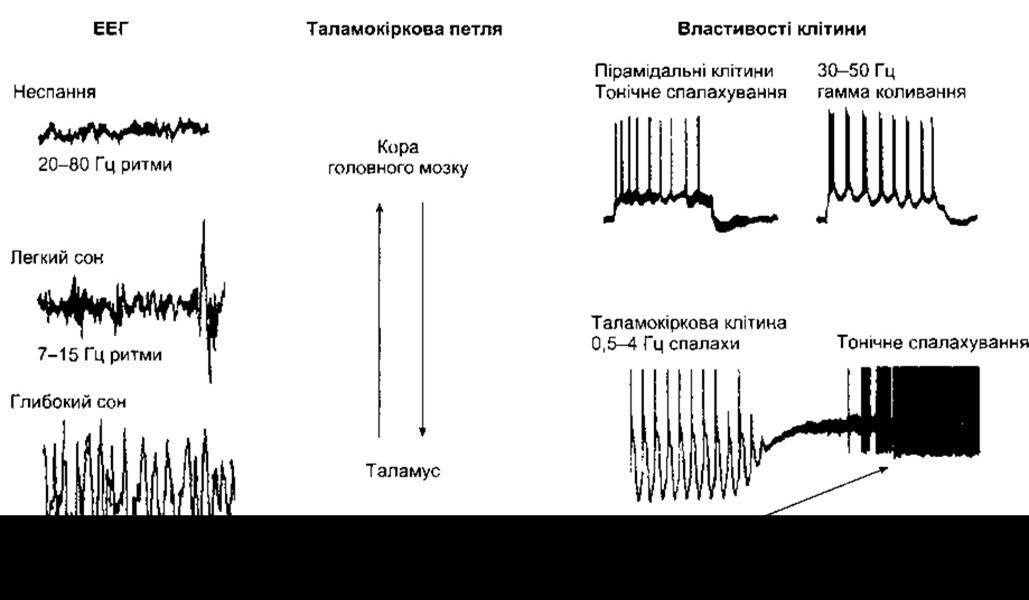
Рис. 11-8. Зв’язок між поведінковими станами, ЕЕГ та клітинними реакціями в корі головного мозку і таламусі (модифіковано та відтворено з McCormick DA: Are thalamocortical rhythms the Rosetta stone of a subset of neurological disorders? Nat Med. 1999; 12:1349).
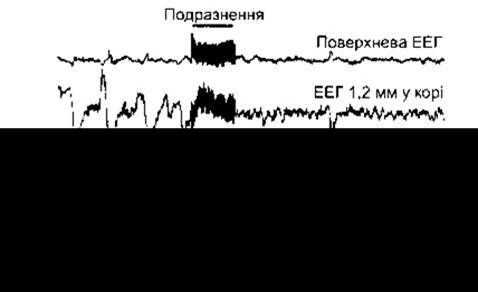
Рис. 11-9. Одночасне записування поверхневої ЕЕГ, ЕЕГ на 1,2 мм у корі та реакції кіркових нейронів, зареєстровані внутрішньоклітинним електродом у кота під легкою анестезією. Подразнення ретикулярної формації середнього мозку (РФСМ) частотою 300 Гц зумовило реакцію тривоги. Зверніть увагу на те, що рівень зміни потенціалів внутрішньокіркового нейрона збільшується під час та після подразнення (відтворено за дозволом з Steriage М, Amzica F, Contreras D: Synchronization of fast (30-40 Hz) spontaneous cortical rhythms during brain activation. J Neurosci. 1996,16:392).
Походження повільнохвильового сну
Повільні хвилі на ЕЕГ та їхній вплив на поведінку, а також повільнохвильовий сон, можуть бути зумовлені стимулюванням щонайменше трьох підкіркових зон.
Сонна зона проміжного мозку міститься в задній частині гіпоталамуса і сусідніх внутрішньоламінарних та передніх таламічних ядрах. Частота подразника повинна становити приблизно 8 Гц; швидші стимули спричинюють збудження. Важливо, що низько- і високочастотне стимулювання зумовлюють різні реакції. Іншою зоною є медулярна синхронізувальна в ретикулярній формації довгастого мозку на рівні ядра солітарного шляху. Подразнення її низькими частотами подібне до стимулювання сонної зони проміжного мозку і спричинює сон, а високими - збудження. Механізми, за допомогою яких це відбувається, нез’ясовані, однак припускають, що у ньому задіяні шляхи, що ведуть до таламуса. Ще одна синхронізувальна ділянка - це базальна передньомозкова зона сну. Вона охоплює передоптичну ділянку та діагональну смугу зони Брока і відрізняється від інших двох тим, що стимулювання базальної передньомозкової зони зумовлюють повільні хвилі й сон, незалежно від частоти стимулювання. Нейрони у вентролатеральній частині передоптичної зони мають проекції до горбово-сосочкового ядра - частини заднього гіпоталамуса, що перебуває в діенцефальній зоні сну.
Зазначимо, що подразнення аферентів через механорецептори шкіри з частотою 10 Гц чи менше також спричинює сон у тварин; відомо також, що внаслідок дії регулярних повторюваних монотонних стимулів засинають люди.
З іншого боку, повільнохвильовий сон перебуває під вираженим циркадним контролем. Роль супрахіазматичних ядер гіпоталамуса в регулюванні сну та інших циркадних ритмів описано в Розділі 14.
Гострі суперечки були щодо впливу серотонінергічних нейронів у мозку (див. Розділ 15) на сон, однак сьогодні з’ясовано, що агоністи серотоніну пригнічують сон, а антагоніст серотоніну ритансерин посилює повільнохвильовий сон у людей. Концентрація аденозину збільшується в холінергічних ділянках базального переднього мозку та мезомостових холінергічних ядрах (див. нижче) упродовж періоду неспання і зменшується під час сну. Ці дві ділянки пов’язані зі сном, отже, аденозин може бути чинником, що зумовлює сон. Такий висновок не суперечить загальновідомим збуджувальним впливам кофеїну, що є антагоністом аденозину.
Відповідно до ще однієї гіпотези, вивільнення простагландину Д2(ПГД2; див. Розділ 17) у медіальній передоптичній ділянці гіпоталамуса посилює повільнохвильовий сон та ШРО, тоді як ПГЕ2 - неспання. Вважають, що ліпід, вироблений мозком, має властивості стимулювання сну. Деякі дослідники доводили, що за сон відповідає пептид, вироблений мозком. Щоправда, наразі нема єдиного погляду, який саме пептид є цим пептидом сну і яка його фізіологічна роль, якщо він її взагалі відіграє.
Фактори, що сприяють сну в разі ШРО
Люди, яких розбудили в період, коли на ЕЕГ у них були характерні для швидкого сну показники, як звичайно стверджують, що бачили сон, тоді як особи, яких розбудили під час повільнохвильового сну, його не бачили. Це спостереження, а також інші докази свідчать про те, що швидкий сон та сновидіння тісно пов’язані. Скреготіння зубами (бруксизм), що трапляється в окремих осіб, також зумовлене сновидінням. Швидкий сон притаманний усім вивченим видам ссавців та птахів, однак він, очевидно, не властивий іншим класам організмів.
Якщо людей будити щоразу під час швидкого сну, а згодом дозволяти їм спати, то тривалість у них швидкого сну протягом кількох ночей значно збільшиться порівняно з нормою. Відповідно, тривала депривація ШРО не має зворотного фізіологічного ефекту. Щоправда, піддослідні тварини, яких повністю позбавляли швидкого сну на тривалий час, втрачали масу і зрештою вмирали, а це свідчить, що швидкий сон відіграє ще не до кінця зрозумілу, однак важливу гомеостатичну роль. З іншого боку, депривація повільнохвильового сну спричинює подібні наслідки, отже, можна вважати, що вони не стосуються власне швидкого сну.
Походження швидкого сну
Низьковольтний швидкий ритм кори головного мозку під час швидкого сну подібний до того, який зафіксовано у вигляді ЕЕГ реакції тривоги, і ймовірно, генерований таким самим способом. Головна відмінність між швидким сном та станом неспання полягає в тому, що сонній свідомості властиві дивні образні та нелогічні думки, і сни, як звичайно, не запам’ятовуються. Причина такої відмінності невідома. Щоправда, ПЕТ сканування в людей у стані швидкого сну відображає підвищену активність у мостовій ділянці, мигдалеподібному тілі та передній поясній звивині, однак знижену - у передлобовій та тім’яній корі. Активність у ділянках візуальних асоціацій є підвищеною, проте знижена активність зафіксована в первинній зоровій корі. Все це узгоджується з підвищеним збудженням та дією закритих нейрональних систем, відрізаних від ділянок, що пов’язують активність мозку із зовнішнім світом. Механізми, які спричинюють швидкий сон, розташовані в ретикулярній формації мосту. МКП піки походять з латеральної ретикулярної покришки і відповідають за зміну заряду холінергічних нейронів. З’ясовано, що зміна заряду норадренергічних нейронів у голубій плямці та серотонінергічних нейронів у середньомозковому шві спричиняє безсоння, і що ці нейрони неактивні, коли холінергічні МКП піки спричинюють швидкий сон. Резерпін, який зменшує вміст серотоніну та катехоламінів, блокує повільнохвильовий сон і деякі аспекти швидкого сну, однак підвищує активність МКП піків. Барбітурати зменшують тривалість швидкого сну.
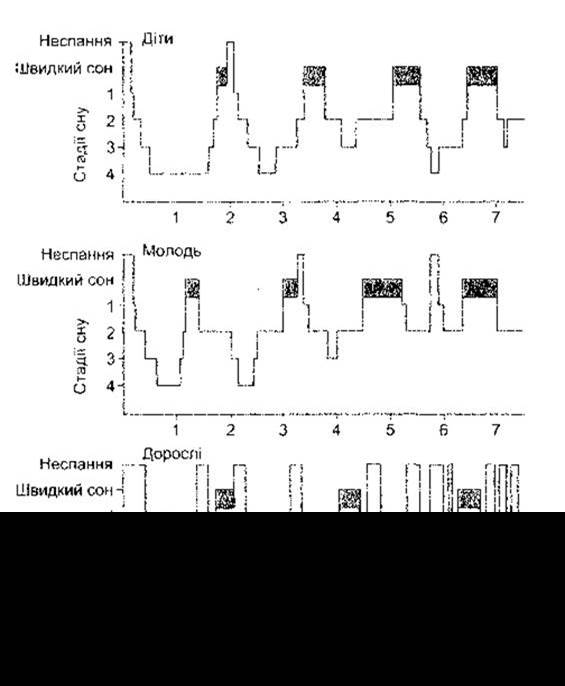
Рис. 11-10. Цикли нормального сну в осіб різного віку. Швидкий сон позначено ділянками темнішого кольору (відновлено за дозволом з Kales AM, Kales JD: Sleep disorders. N Engl J Med. 1974;290:487).
Розподіл стадій сну
Під час типового нічного сну молода людина спочатку перебуває у стадії сну НШРО, згодом переходить у першу і другу стадії, а протягом 70-100 хв - третю і четверту. Далі сон полегшується і настає період швидкого сну. Цей цикл повторюється з інтервалом приблизно до 90 хв упродовж ночі (рис. 1-10). Цикли майже подібні, хоча ближче до ранку третя і четверта стадії стають коротшими, а швидкий сон - довшим. Отже, протягом ночі буває від чотирьох до шести періодів швидкого сну. Такий сон становить 80% від загальної тривалості сну у недоношених немовлят (рис. 11-11) та 50% у доношених. Надалі відсоток швидкого сну зменшується, стає на рівні 25% і знову зменшується вже в старому віці. У дітей загальна тривалість сну та тривалість четвертої стадії довша, ніж у дорослих.
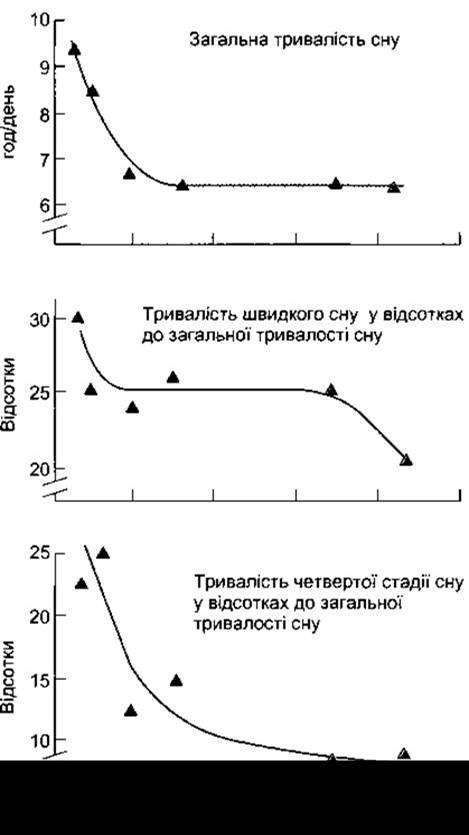
Рис. 11-11. Вікові зміни сну людини. На кожному графіку показано дані для віку 6, 10, 21, 30, 69 та 84 роки (дані з Kandel ER, Schwartz JH, Jessel TM [editors]: Principles of Neural Science, 3rd ed. McGraw-Hill Companies, Inc. 1991).
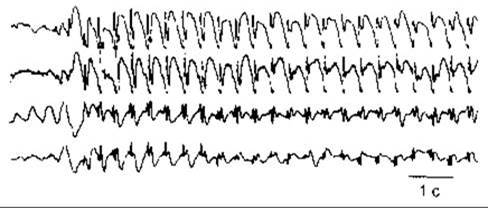
Рис. 11-12. Малий епілептичний напад. Запис чотирьохелектродної ЕЕГ у шестирічного хлопчика під час одного з нападів, за якого він не усвідомлював, де перебуває, і кліпав очима. Час показано горизонтальною лінією (Відтворено за дозволом з Waxman SG: Correlative Neuroanatomy, 24th ed. McGraw-Hill, 2000).
Розлади сну
Безсоння, яке можна означити як суб’єктивну проблему, пов’язану з недостатнім чи невідновлювальним сном, незважаючи на наявність потрібних для нього умов, буває майже у всіх дорослих людей. Тривале ж безсоння зумовлене багатьма різними ментальними та медичними станами. Тимчасово його можна полегшити за допомогою снодійного, наприклад бензодіазепіну. Однак тривале вживання будь-яких із цих таблеток недоцільне, оскільки вони впливають також на діяльність людини в денний час і призводять до звикання.
Фатальне родинне безсоння - це хвороба, спричинена пріонами, яка прогресує і виявляється в успадкованих та спорадичних формах. Воно супроводжується безсонням, що прогресує, погіршенням автономних та рухових функцій, деменцією та смертю. У пацієнтів з цією хворобою відбувається раптова втрата нейронів, простежується гліоз у вентральних і медіодорсальних ядрах таламуса, оливах та довгастому мозку. Хвороби, спричинені пріонами, - це енцефалопатії, що можуть переходити до тварин і виявляються в людей у кількох формах: хвороба Крейтцфельда-Якоба, хвороба Ґерстмана-Штройслера-Шайнкера та куру, що пов’язана з ритуальним канібалізмом.
Ходіння уві сні (сомнабулізм), нічний енурез та нічні страхи трапляються під час пробудження від повільнохвильового сну. Вони не пов’язані зі швидким сном. Випадки ходіння уві сні частіше бувають у дітей, ніж у дорослих, переважно в осіб чоловічої статі й можуть тривати кілька хвилин. Сомнабули ходять з розплющеними очима й оминають перешкоди на шляху, однак якщо їх розбудити, то не можуть пригадати епізоди ходіння уві сні.
Нарколепсія є хворобою, за якої виникає епізодична раптова втрата м’язового тонусу та фактично непереборна схильність до засинання впродовж дня. У деяких випадках це починається раптовими напливами швидкого сну. У здорових осіб швидкий сон майже ніколи не передує повільно-хвильовому. Спадковість цього стану в людей - рідкісне явище, натомість успадковані форми у собак зумовлені мутацією в одному чи двох рецепторах орексину - поліпептиду, задіяного в регулюванні апетиту (див. Розділ 14).
Асфіксію уві сні спричинює обструкція дихальних шляхів під час вдихання. Детально це описано в Розділі 37. Якщо такий стан повторюється неодноразово, як це часто трапляється в людей похилого віку, то втрата сну зумовлює втому і млявість упродовж дня. Такий стан можна полегшити, відівчивши хворих спати на спині, а також уникаючи вживання респіраторних депресантів, гіпнотичних препаратів та алкоголю, а в разі гострих форм - за допомогою позитивного тиску дихальних шляхів під час сну.
Розлад поведінки у разі швидкого сну є нещодавно виявленим станом, під час якого не розвивається гіпотонія. Як наслідок, стан таких пацієнтів нагадує стан котів з експериментальним ушкодженням голубої плямки - він «діє в контексті своїх снів»: вони неспокійні і можуть навіть зіскочити з ліжка, готові боротися з удаваним супротивником. Цей розлад, як звичайно, лікують бензодіазепінами. Інші специфічні розлади сну описано також у науково-лабораторних дослідженнях сну.
Клінічне застосування ЕЕГ
Інколи ЕЕГ корисна для виявлення патологічних процесів. Якщо внаслідок накопичення рідини перекрито ділянку кори головного мозку, то активність над такою зоною може бути знижена. Цей факт дає змогу діагностувати та виявляти субдуральні гематоми. Ушкодження в корі спричинюють локальне утворення нерегулярних чи повільних хвиль, які може вловлювати ЕЕГ. Епілептогенні осередки інколи генерують високовольтні хвилі, які також можна виявити.
Епілепсія - це синдром, який може бути зумовлений багатьма причинами. У випадку деяких форм простежується характерний вигляд ЕЕГ під час нападів, щоправда у періоди між ними ці аномалії важко відобразити. Загалом напади поділяють на такі, що походять з однієї півкулі головного мозку (часткові, чи локальні, напади), і ті, що стосуються обидвох півкуль одночасно (глобальні напади). Кожна з категорій має підкатегорії. Напади тонічно-клонічного типу (великі судомні напади) супроводжуються раптовою втратою свідомості. Далі настає тонічна фаза з безперервним скороченням м’язів кінцівок, згодом - клонічна фаза з симетричним посмикуванням кінцівок, а внаслідок цього - альтернаційне скорочення та розслаблення. У разі тонічної фази активність ЕЕГ висока. Під час кожного клонічного посмикування виникають повільні хвилі, вслід за кожною з яких настає пік. Повільні хвилі тривають упродовж короткого проміжку часу після нападу. Подібні зміни простежуються у піддослідних тварин під час конвульсій, зумовлених електрошоком. Напади короткотривалої втрати свідомості (малі епілептичні напади) є однією з форм хвороби з одномоментною втратою реактивності. Вони пов’язані з триразовим подвоєнням, кожне з яких складається з типового піка та заокругленої хвилі (рис. 11-12).