Общая микробиология - Шлегель Г. 1987
Типы брожения
Маслянокислое и ацетоно-бутиловое брожение; клостридии
Масляная кислота (бутират), н-бутанол, ацетон, 2-пропанол и ряд других органических кислот и спиртов являются типичными продуктами сбраживания углеводов анаэробными спорообразующими бактериями (клостридиями). Поэтому клостридии, а также некоторые специализированные виды, сбраживающие только этанол, аминокислоты или иные вещества, рассматриваются здесь в связи с маслянокислым брожением, которое они вызывают.
Признаки. Род Clostridium относится к семейству Васillасеае. Как и другие представители этого семейства (Bacillus, Sporolactobacillus, Desulfotomaculum и Sporosarcina), клостридии грам-положительны. Благодаря перитрихально расположенным жгутикам они очень подвижны. Вегетативные клетки палочковидные, однако форма их может изменяться в зависимости от условий среды. Овальные или шарообразные эндоспоры изменяют форму палочковидной материнской клетки, так как их диаметр, как правило, больше толщины этой клетки. Споры терморезистентны.
Физиологически клостридии отличаются резко выраженным бродильным типом метаболизма, а также чувствительностью к кислороду: они растут только в анаэробных условиях. Однако существуют, по-видимому, все переходные формы - от строго анаэробных видов (Clostridium pasteurianum, С. kluyveri) до почти аэротолерантных (например, С. histolyticum, С. acetobutylicum). Клостридии, как правило, не содержат гемопротеинов (цитохромов, каталазы). Некоторые виды способны, однако, образовывать цитохромы, если в питательной среде содержатся их предшественники. Из запасных веществ широко распространены крахмалоподобные полисахариды.
Температурный оптимум для роста большинства известных видов Clostridium лежит между 30 и 40°С. Наряду с этими мезофильными представителями встречается много термофильных видов с оптимумом 60-75°С, таких как С. thermoaceticum и С. thermohydrosulfuricum. Подобно другим представителям Bacillaceae, клостридии способны расти только при нейтральной (или щелочной) реакции среды. Поэтому их рост, часто нежелательный, может быть полностью подавлен при подкислении (например, в квашеной капусте, силосе, фруктовых консервах, сырых колбасах).
Субстраты. Клостридии весьма сильно различаются в отношении субстратов, которые они могут использовать и сбраживать. Некоторые виды мало разборчивы и используют широкий круг веществ, другие узко специализированы и способны сбраживать лишь один или несколько субстратов. В целом же клостридиям доступно множество различных природных соединений. Они способны разлагать полисахариды (крахмал, гликоген, целлюлозу, гемицеллюлозы, пектины), нуклеиновые кислоты, белки, аминокислоты, пурины и пиримидины. Одним клостридиям нужны сложные питательные среды или ростовые вещества, другие в них не нуждаются. Некоторые могут обходиться молекулярным азотом как единственным источником этого элемента; азот они связывают с большой скоростью (Clostridium pasteurianum)1.
1 В последние годы установлено, что некоторые виды Clostridium способны к автотрофному росту с использованием молекулярного водорода. Таковы С. thermoautotrophicum, С. aceticum и С. thermoaceticum (см. разд. 9.5). - Прим. ред.
По способности использовать различные субстраты клостридии можно подразделить на ряд групп. Сахаролитические клостридии расщепляют преимущественно полисахариды или сахара. Пептолитические клостридии расщепляют белки, пептоны и аминокислоты. Группы в свою очередь объединяют на основе типов брожения и его продуктов (табл. 8.7 и 8.8).
Для получения накопительных культур видов Clostridium можно воспользоваться некоторыми их особенностями. Поскольку их споры терморезистентны, инокулят предварительно пастеризуют. Создавая строго анаэробные условия, заранее исключают рост всех аэробных бактерий. Так как некоторые бактерии, расщепляющие полисахариды, прикреплены к поверхности частиц, например к крахмальным зернам или к частицам целлюлозы в рубце жвачных или каких-то осадках, эти частицы можно сначала промыть, чтобы освободить их от других бактерий, а затем использовать как материал для инокуляции. Для поддержания способности к интенсивному брожению нужно и в последующей работе с выделенными штаммами всегда пользоваться пастеризованными инокулятами.
Биохимия брожения и его продукты. При брожении образуются в разных соотношениях кислоты (масляная, уксусная, молочная), спирты (бутанол, этанол, 2-пропанол), а также ацетон и газообразные продукты (Н2 и СO2). Клостридии расщепляют глюкозу по фруктозобисфосфатному пути. Водород, освобождающийся при дегидрировании глицераль- дегидфосфата, переносится, как правило, на органические кислоты или кетоны, образуемые из пирувата или ацетил-СоА. Прототипом брожения, осуществляемого клостридиями, можно считать сбраживание глюкозы Clostridium butyricum и С. acetobutylicum; при этом образуются бутират, ацетат, бутанол, этанол, ацетон, 2-пропанол, СО2 и Н2. Выход продуктов варьирует в зависимости от условий.
Таблица 8.7. Клостридии, различающиеся по характеру брожения
|
Типы брожения и виды бактерий |
Субстраты |
Продукты брожения |
|
I. Маслянокислое брожение С. butyricum С. tyrobutyricum С. pasteurianum С. pectinovorum |
Глюкоза, крахмал, декстрин Глюкоза или лактат (глицерол) + ацетат Глюкоза, крахмал, маннитол, инулин Пектин, крахмал, гликоген, декстрин |
Бутират, ацетат, СO2, H2 Бутират, ацетат, СO2, H2 Бутират, ацетат, СO2 Бутират, ацетат |
|
II. Образование бутанола С. butylicum С. acetobutylicum |
Глюкоза Глюкоза, глицерол, пируват |
Бутират, ацетат, бутанол, 2-пропанол, СO2, H2 Бутират, ацетат, бутанол, ацетон, ацетони, этанол, СO2, Н2 |
|
III. Образование пропиоиовой кислоты С. propionicum |
Аланин, треонин |
Ацетат, пропионат, СО2 |
|
IV. Образование капроновой кислоты С. kluyveri |
Этанол + ацетат + СО2 |
Капронат, бутират, Н2 |
|
V. Осуществление реакции Стикленда С. botulinum С. histolyticum С. sporogenes С. sticklandii |
Белки, аминокислоты |
Ацетат, лактат, NH3, Н2 |
|
VI. Наличие особых метаболических путей С. aceticum С. tetanomorphum С. acidi-urici |
(СО2 + Н2), фруктоза Глутамат, гистидин Мочевая кислота, ксантин |
Ацетат Бутират, ацетат, NH3, СО2, Н2 Ацетат, формиат, СО2, NH3 |
Масляная кислота (бутират) - продукт конденсации двух молекул ацетил-СоА при участии тиолазы с образованием ацетоацетил-СоА и его последующим восстановлением (рис. 8.4). Ацетоацетил-СоА восстанавливается за счет NADH2при участии ß-гидроксибутирил-СоА-дегидрогеназы до ß-гидроксибутирил-СоА. От последнего с помощью кротоназы отщепляется вода. Кротонил-СоА под действием флавинового фермента бутирил-СоА-дегидрогеназы восстанавливается до бутирил-СоА. От бутирил-СоА с помощью СоА-трансферазы СоА может переноситься на ацетат; при этом освобождается масляная кислота, которая выходит в среду. Из ацетил-СоА при участии фосфотрансацетилазы и ацетаткиназы может быть получен свободный ацетат, что сопровождается синтезом АТР из ADP (см. также стр. 264).
![]()
Таблица 8.8. Особые виды брожения
|
Вид бактерий |
Субстраты |
Продукты брожения |
|
Eubacterium limosum (Butyribacterium rettgeri) |
Глюкоза, лактат, пируват |
Бутират, ацетат, СО2. Н2; лактат (при использовании глюкозы) |
|
Peptococcus anaerobius (Diplococcus glycinophilus) |
Глицин |
Ацетат, СО2, Н2, NH3 |
|
Fusobacterium nucleatum |
Аминокислоты |
Ацетат, лактат, этанол, СО2, NH3 |
|
Clostridium oroticum |
Оротовая кислота |
Ацетат, сукцинат, СО2, NH3 |
При чистом маслянокислом брожении образующийся при окислении пирувата водород выделяется в газообразном виде. Когда глюкоза сбраживается согласно уравнению
Глюкоза → Бутират + 2СО2 + 2Н2
баланс водорода сходится; на один моль глюкозы образуются три моля АТР.
Бутанол, бутират, ацетон и 2-пропанол образуются при сбраживании глюкозы клетками Clostridium acetobutylicum. При этом вначале выделяется также масляная кислота; однако по мере подкисления среды (рис. 8.5) начинают синтезироваться ферменты (в том числе ацетоацетатдекарбоксилаза), действие которых приводит к накоплению ацетона и бутанола. Процессы образования этих веществ тесно связаны между собой. В результате декарбоксилирования части ацетоацетата утрачивается потенциальный акцептор водорода, который при восстановлении в бутират мог бы дважды присоединить 2[Н]. Этот водород так или иначе должен быть передан другим акцепторам, в том числе и только что образовавшемуся бутирату. Для восстановления до бутанола бутират должен быть сначала активирован путем превращения в бутирил-СоА. Реакции, происходящие при образовании бутирата, ацетона и бутанола, представлены на рис. 8.4. При брожении в щелочной среде (например, в присутствии СаСО3; табл. 8.9) С. acetobutylicum ведет себя как C. butyricum. Некоторые штаммы восстанавливают ацетон и выделяют 2-пропанол.
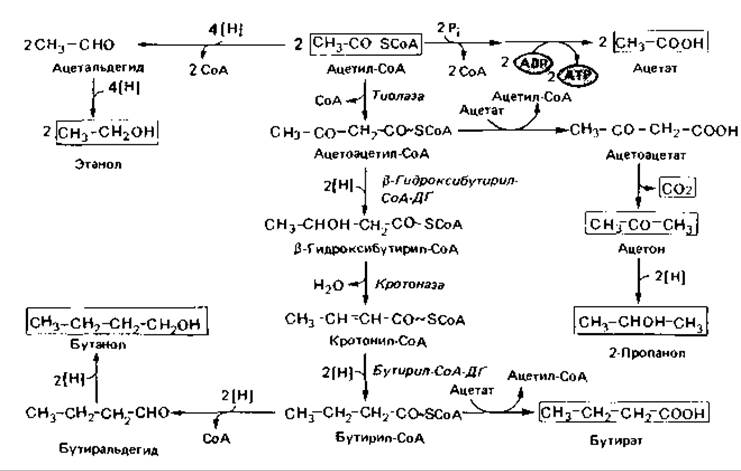
Рис. 8.4. Образование ацетата, этанола, н.бутанола, бутирата, ацетона и 2-пропанола при брожениях, осуществляемых клостридиями. Начальное расщепление глюкозы идет по фруктозобисфосфатному пути; пируват дегидрируется при участии пируват: ферредоксин-оксидоредуктазы. На схеме представлены только последовательности реакций, начинающиеся от ацетил-СоА. ДГ - дегидрогеназа.
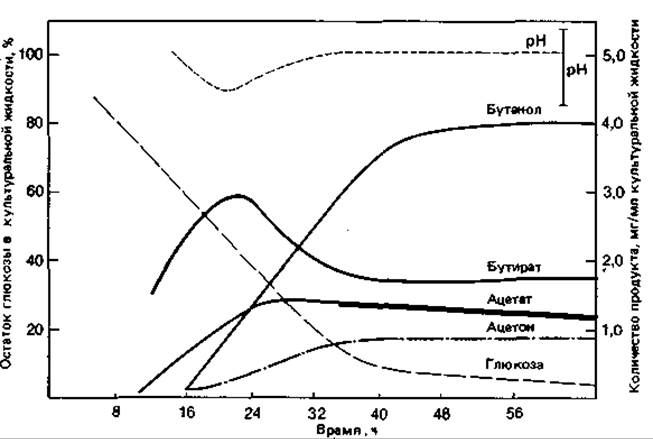
Рис. 8.5. Динамика сбраживания глюкозы бактерией Clostridium acetobutylicum. (Davis R., Stephenson M., Biochem. J., 35 [1941], 1320.)
Таблица 8.9. Ацетоно-бутиловое брожение, осуществляемое Clostridium acetobut ylicum в присутствии и в отсутствие СаСO3, (Bernhauer et al., Biochem. Zeitschrift, 287 [1936], 61)
|
Продукт брожения |
Количество продукта, мг на 50 мл сброженного 6%-ного затора |
|
|
Без СаСO3 |
В присутствии СаСO3 |
|
|
Масляная кислота |
32,4 |
630 |
|
Бутанол |
411,5 |
45,7 |
|
Уксусная кислота |
102,1 |
230,7 |
|
Этанол |
44,5 |
22,4 |
|
Ацетон |
222,3 |
13,2 |
Этанол образуется в результате восстановления ацетил-СоА.
Молекулярный водород может происходить из NADH2, образующегося как при расщеплении пирувата, так и при дегидрировании глицеральдегидфосфата (см. стр. 265). Чем больше водорода может быть образовано при этом, тем меньше нужно синтезировать акцепторов водорода (ацетоацетил-СоА). Таким образом, энергия связи ацетил-СоА может быть сохранена в форме АТР. Значит, если при сбраживании глюкозы С. butyricum на один моль глюкозы образуется больше двух молей Н2 и поэтому меньше бутирата и соответственно больше ацетата, то выход АТР может превышать 3 моля (см. ниже о Ruminococcus).
Поскольку ацетон, 2-пропанол и бутанол служат важными органическими растворителями, брожение, осуществляемое клостридиями, имеет большое техническое значение. Именно в связи с получением этих веществ перед промышленносью впервые встала задача проведения микробиологических синтезов в условиях, исключающих возможность всякого загрязнения.
Сбраживание этанола и ацетата. Из накопительных культур Methanobacterium omelianskii, содержавших в качестве субстрата этанол, была выделена анаэробная спорообразующая бактерия, которая наряду с этанолом нуждается и в ацетате. Эта бактерия - Clostridium kluyveri - превращает смесь уксусной кислоты и этанола в масляную и капроновую кислоты и молекулярный водород (рис. 8.6). Ацетат служит дополнительным акцептором водорода, и он образуется в ходе брожения. АТР синтезируется только при ацетаткиназной реакции.
Сбраживание лактата и ацетата. Из накопительных культур, содержащих в качестве субстрата лактат, была выделена бактерия Clostridium tyrobutyricum, которой тоже необходим ацетат как дополнительный акцептор водорода, если главным субстратом служит лактат или глицерол:
![]()
С. tyrobutyricum сбраживает глюкозу по схеме, известной для С. butyricum, не нуждаясь в экзогенном акцепторе водорода.
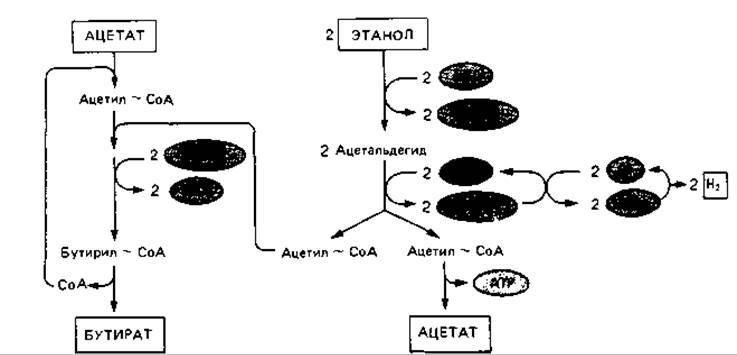
Рис. 8.6. Сбраживание этанола и ацетата с образованием бутирата и молекулярного водорода Clostridium kluyveri. Fd - ферредоксин.
Сбраживание глутаминовой кислоты. Из множества процессов брожения, при которых аминокислоты в анаэробных условиях превращаются в жирные кислоты, СO2 и аммиак, мы рассмотрим только расщепление глутамата бактерией Clostridium tetanomorphum. Это брожение привлекло к себе внимание потому, что на его примере была выяснена биохимическая функция витамина В12. С. tetanomorphum обычно выделяют из накопительной культуры с гистидином в качестве субстрата. Гистидин расщепляется через глутамат. При сбраживании глутамата образуются масляная и уксусная кислоты, аммиак, СO2 и молекулярный водород. Путь катаболизма глутамата включает ряд необычных реакций (рис. 8.7). Сначала разрываются связи между углеродными атомами 2 и 3 и образуются связи между атомами 2 и 4, и в результате получается аминокислота- с разветвленной цепью - метиласпарагиновая кислота. В этом участвует кофермент - производное витамина В12. Лишь на этой стадии происходит дезаминирование. К ненасыщенной мезаконовой (метилфумаровой) кислоте присоединяется вода, а образующаяся цитрамалевая (2-метил-яблочная) кислота расщепляется затем на уксусную и пировиноградную кислоты. Уксусная кислота выделяется, а пировиноградная рассмотренным выше путем превращается в масляную кислоту и СO2.
Сопряженное сбраживание двух аминокислот (реакция Стикленда).
Пептолитические клостридии (табл. 8.7, V) гидролизуют белки и затем используют аминокислоты. Многие аминокислоты сбраживаются толь ко вместе с какими-нибудь другими. Как установил Стикленд (1934), Clostridium sporogenes быстро сбраживает смесь аланина и глицина, но не может использовать ни ту ни другую из этих аминокислот в отдельности. Судя по суммарному уравнению
Аланин + 2 Глицин + 2Н2О → 3 Ацетат + 3NH3+ СO2
аланин служит донором водорода, а глицин-акцептором:
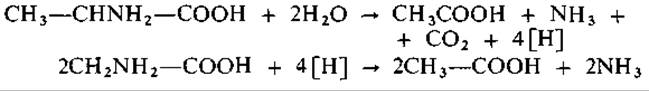
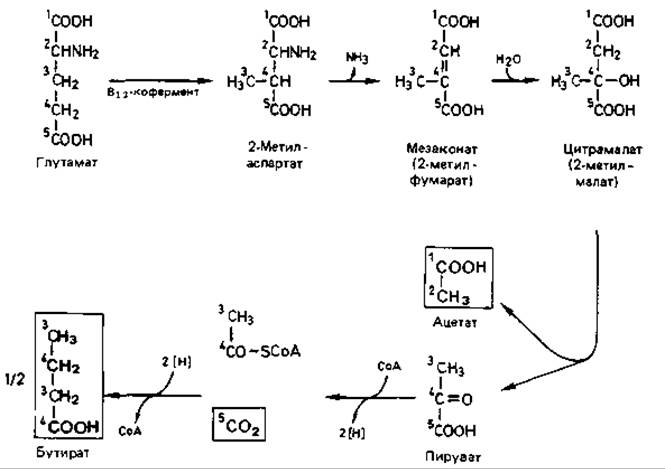
Рис. 8.7. Сбраживание глутамата бактерией Clostridium tetanomorphum по мезаконатному пути.
Источником энергии, очевидно, служит сопряженная реакция окисления - восстановления. Роль донора водорода могут выполнять, например, аланин, лейцин, изолейцин, валин, серин, метионин и т.д. Акцепторами водорода могут служить глицин, пролин, аргинин, триптофан и т.д. Аминокислота - донор дезаминируется в оксокислоту, которая затем в результате окислительного декарбоксилирования превращается в жирную кислоту. Этот этап сопряжен с фосфорилированием и, таким образом, представляет собой реакцию, доставляющую энергию. Водород, перенесенный при этом на ферредоксин, снова связывается при восстановительном дезаминировании аминокислоты-акцептора. Однако не все аминокислоты используются всеми пептолитическими клостридиями.
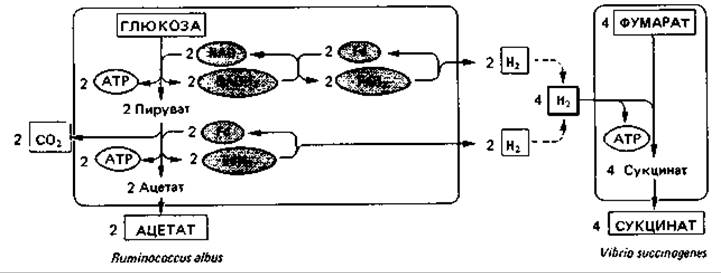
Рис. 8.8. Сбраживание глюкозы бактерией Ruminococcus albus и использование образовавшегося водорода в смешанной культуре с Vibrio succinogenes. (Пример симбиоза с передачей продукта одного вида другому виду.) Fd - ферредоксин.
Маслянокислое и уксуснокислое (ацетатное) брожение1, осуществляемое неспорообразующими бактериями. Некоторые роды анаэробных бактерий близки к клостридиям по продуктам брожения; они, однако, не образуют спор, и многие из них грам-отрицательны. Большинство таких бактерий, образующих масляную и уксусную кислоты, было выделено из рубца, где они участвуют в разложении целлюлозы, крахмала и других углеводов. Они выделяют много молекулярного водорода и СО2 и создают метаногенным бактериям условия для образования метана. Из бактерий рубца, образующих масляную кислоту, следует особо упомянуть Bytyrivibrio fibrosolvens, а из обитающих в рубце продуцентов уксусной кислоты - Ruminococcus albus. Этот последний вид - строгий анаэроб, использующий целлюлозу и ксилан, а также многие сахара. Он способен превращать 1 моль глюкозы в 2 моля ацетата, 2 моля СO2 и 4 моля Н2 - правда, при условии, что концентрация выделенного водорода поддерживается на низком уровне. Это возможно в смешанной культуре с какой-либо бактерией, использующей водород, например Vibrio succinogenes (рис. 8.8). Из приведенной схемы видно, что при чистом ацетатном брожении может быть образовано 4 моля АТР на 1 моль глюкозы. Столь высокая эффективность регенерации АТР возможна, однако, лишь в том случае, если все возникающие при расщеплении глюкозы восстановительные эквиваленты будут освобождаться в виде молекулярного водорода (см. выше).
Клостридии - возбудители болезней и продуценты токсинов. Некоторые пептолитические клостридии могут быть возбудителями болезней при раневой инфекции (газовая гангрена и столбняк), а также причиной пищевых отравлений. Споры их очень распространены в почве. Если споры Clostridium histolyticum или С. septicum попадают в открытую рану, к которой нет доступа воздуха или где аэробные бактерии, потребляя кислород, создают анаэробные условия, то эти клостридии начинают расти, расщеплять с помощью протеиназ коллаген и другие белки, вызывать образование дурно пахнущих продуктов брожения и газа. С такого рода газовой гангреной («госпитальной гангреной») в прежние времена можно было бороться только путем ампутации пораженной конечности. С раневой инфекцией связан и до сих пор еще нередко встречающийся столбняк. Его вызывает Clostridium tetani. Эта бактерия при своем росте выделяет очень сильный нейротоксин, вызывающий тонические судороги мышц.
1 С уксуснокислым брожением не следует смешивать аэробный процесс, осуществляемый уксуснокислыми бактериями - Прим. перев.
Наиболее тяжелую форму пищевого отравления - ботулизм - вызывает Clostridium botulinum. Это широко распространенная почвенная бактерия, которая может развиваться в недостаточно простерилизованных мясных продуктах и бобовых консервах. Она получила свое название потому, что встречается в колбасе (лат. botulus - колбаса). Образуемый ею токсин в случае потребления зараженного продукта может вызвать смерть вследствие нервного паралича, в частности паралича дыхания. Токсин этот, к счастью, термолабилен и быстро (за 15 мин) инактивируется при кипячении.