Биологические мембраны - А. Н. Огурцов 2012
Электрогенез биомембран
Механизмы межклеточной сигнализации
Кальциевая регуляция экзоцитоза нейротрансмиттеров
Нейротрансмиттеры высвобождаются в синаптическую щель по механизму регулируемого экзоцитоза, в котором синаптические пузырьки сливаются с терминальной мембраной аксона (рисунок 125). Экзоцитоз нейротрансмиттеров из синаптических везикул использует механизмы адресного везикулярного транспорта и слияния, которые характерны для внутриклеточного везикулярного транспорта (п. 8.4).
Отличие нейросекреции от других секреторных механизмов заключается в том, что
1) нейросекреция происходит только тогда, когда потенциал действия достигает терминалей аксона,
2) синаптические везикулы после слияния с плазматической мембраной и высвобождения содержимого в синаптическую щель не становятся частью плазматической мембраны терминаля аксона, а вновь используются для заполнения нейротрансмиттерами.
На рисунке 153 изображен полный цикл функционирования везикулы, в котором синаптический пузырёк заполняется молекулами нейротрансмиттеров, высвобождает содержимое в синаптическую щель и рециклируется вновь. Полный цикл такого синаптического пузырька продолжается порядка 1 минуты.
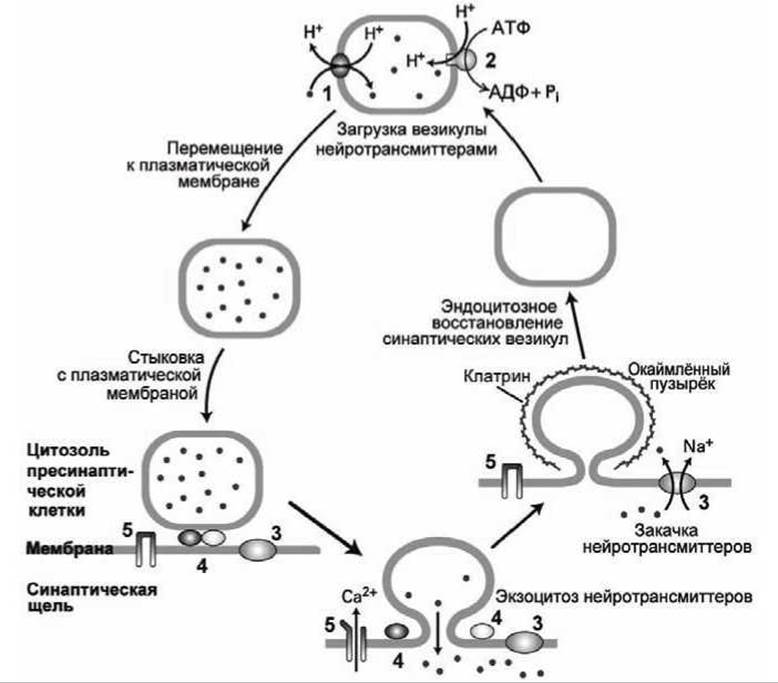
Рисунок 153 - Циклирование нейротрансмиттеров и синаптических везикул в терминалах аксонов: 1 - Н+-сопряжённый антипортёр нейротрансмиттеров; 2 - протонная помпа V-типа; 3 - Na+-сопряжённые симпортёры нейротрансмиттеров; 4 - Са2+-чувствительные стыковочные белки; 5 - потенциалочувствительные Са2+-каналы
Примечательно, что ацетилхолин, в отличие от остальных нейротрансмиттеров, не рециклируется по схеме, представленной на рисунке 153.
Сама по себе деполяризация плазматической мембраны не может заставить синаптические везикулы слиться с плазматической мембраной. Для запуска такого процесса слияния потенциал действия должен быть превращён в химический сигнал, а именно, в локальное повышение цитозольной концентрации ионов Са2+.
Такими преобразователями электрического потенциала действия в химический сигнал-активатор экзоцитоза являются потенциалочувствительные Са2+-каналы, находящиеся в пресинаптической части синапса. Деполяризация мембраны вследствие прихода потенциала действия открывает эти каналы, и ионы кальция входят в терминаль аксона. Концентрация катионов кальция возрастает от < 0,1 мкМ (в состоянии покоя) до 1-100мкМ. Именно связывание ионов Са2+ с белками, которые присоединяют синаптические пузырьки к плазматической мембране аксона (стыковочные белки (4) на рисунке 153) индуцирует слияние мембран и последующий экзоцитоз нейротрансмиттеров.
Последующее выкачивание избытка ионов кальция из цитозоля нейрона Са2+-АТФазами плазматической мембраны быстро снижает уровень кальция в цитозоле до исходного, позволяя терминалям аксона реагировать на приход следующих импульсов потенциала действия.
В терминалях аксонов разделяют два типа синаптических везикул: (1) "пристыкованные" к плазматической мембране и (2) зарезервированные в "активной зоне" вблизи синаптической щели. Каждый всплеск концентрации Са2+-ионов стимулирует экзоцитоз у -10% пристыкованных синаптических пузырьков.
Те мембранные белки, которые необходимы для заполнения синаптических везикул нейротрансмиттерами и пристыковки к плазматической мембране, возвращаются в синаптические везикулы по эндоцитозному механизму, который аналогичен ретроградному транспорту (рисунок 83), и который осуществляется с помощью клатринового окаймления везикул (рисунок 84). После деполимеризации клатринового окаймления эндоцитозная везикула быстро заполняется нейротрансмиттерами. Тот факт, что многие нейроны способны возбуждаться более чем 50 раз в секунду свидетельствует о том, что рециклирование мембранных белков везикул происходит очень быстро.
Сразу после высвобождения нейротрансмиттеров в синаптическую щель и передачи этого химического сигнала постсинаптической клетке, молекулы нейротрансмиттеров должны быть удалены из синаптической щели, иначе постсинаптическая клетка будет постоянно возбуждаться этими нейротрансмиттерами.
Снятие возбуждения может произойти вследствие диффузии молекул нейротрансмиттеров из синаптической щели. Однако это очень медленный процесс, и он не обеспечивает физиологически необходимой скорости очистки синаптической щели от нейротрансмиттеров.
Вместо диффузии используется один или несколько более быстрых способов удаления нейротрансмиттеров из синаптической щели.
Передача сигнала с помощью ацетилхолина прерывается вследствие гидролиза молекул ацетилхолина на холин и уксусную кислоту в синаптической щели ферментом ацетилхолинэстераза (см. [9] п. 13.2). Образующийся при этом холин возвращается назад в пресинаптический аксон с помощью Na+/холин симпортёров и вновь используется для синтеза ацетилхолина. Работа этого симпортёра аналогична работе симпортёров глюкозы (рисунок 103).
В отличие от ацетилхолина все остальные нейротрансмиттеры не модифицируются, а удаляются из синаптической щели закачиванием их обратно в пресинаптический аксон, как изображено на рисунке 153.
Первыми были детально исследованы четыре Na+/нейтотранс-миттер-симпортёра для GABA (у-аминомасляной кислоты), норадреналина, дофамина и серотонина. Все эти симпортёры на 60-70% имеют идентичные аминокислотные последовательности и имеют по 12 трансмембранных а-спиралей.
Так же, как и у других Na+-симпортёров, источником энергии для закачивания нейротрансмиттеров обратно в цитозоль пресинаптического аксона является перемещение ионов Na+ по электрохимическому градиенту через плазматическую мембрану. Для сохранения электронейтральности, как правило, параллельно с переносом ионов Na+ и молекул нейротрансмиттеров происходит транспорт анионов С1 через ионные каналы.