Молекулярная биология: Структура и функции белков - Степанов В.М. 2005
Выделение белов
Разделение белков по молекулярной массе. Гель-хроматография (гель-фильтрация)
В этом методе используют гранулированные гели поперечно-сшитых гидрофильных материалов, например декстрана (сефадекс, сефароза и их аналоги), полиакриламида (биогели и их аналоги), поливинилового спирта (тойоперл). Гранулы образованы трехмерной сеткой полимера, которая непроницаема для крупных молекул, частично проницаема для молекул промежуточного размера и хорошо проницаема для небольших молекул, солей и воды. В зависимости от среднего размера ячейки полимерного геля и геометрии молекулы последней доступна большая или меньшая часть общего объема гранул геля.
При движении раствора, содержащего белки и другие молекулы, по колонке, которая заполнена набухшими гранулами геля, компоненты смеси, проникшие в гель, задерживаются в нем. Таким образом, они отстают от более крупных молекул, которые не могут войти внутрь гранул и находятся только в омывающем их растворе. Не будучи включенными в гель, крупные молекулы появляются в элюате, как только через колонку пройдет «свободный» объем раствора V0, равный объему раствора, заключенному между гранулами геля. Последний определяется плотностью упаковки и геометрией гранул. Для сферических частиц, в виде которых обычно и выпускаются материалы для гель-хроматографии, свободный объем составляет 30-35% общего объема колонки Vt.
Если размеры молекул белка таковы, что они могут проникать в поры, составляющие некоторую часть объема гранул, то будет наблюдаться задержка элюции и белок появится в объеме Ve, связанном с коэффициентом доступности Kдост (долей объема гранул, доступной данному виду молекул) соотношением
![]()
где Vt — полный объем колонки, за вычетом той его части, которая приходится на сам гельобразующий полимер.
Каждому белку в зависимости от размеров его молекулы соответствует свое значение Кдост, на чем и основано разделение при гель-хроматографии. Понятно, что если объем элюции Ve близок к свободному объему Е0, то Kдост стремится к нулю и разделение белков, молекулы которых практически не входят в поры геля, не произойдет. Точно так же молекулы небольших размеров, для которых проницаем весь объем геля (Ve близок к Vt и Кдост стремится к единице), в геле с данными характеристиками не разделятся. Наилучшее разрешение получается, если Кдост находится в пределах 0,4-0,6. Разумеется, пределы разделения можно расширить, используя для высокомолекулярных белков крупнопористые, а для небольших — мелкопористые гели.
Строго говоря, при гель-хроматографии разделение белков определяется не молекулярной массой, а геометрическими размерами молекулы. Соответственно молекулы вытянутой формы за счет «кувыркания» в растворе труднее проникают в гели, чем сферические молекулы такой же молекулярной массы. Этим объясняется ранняя элюция денатурированных белков, которые ведут себя как неупорядоченный рыхлый клубок, а не как компактная глобула.
Простая зависимость между объемом элюции и молекулярной массой белка (справедливая, конечно, только для компактных сферических молекул) и легкость эксперимента сделали гель-хроматографию излюбленным методом определения молекулярной массы белков. Для этой цели колонку, заполненную соответствующим гелем, калибруют набором белков с известными молекулярными массами, после чего определяют объем элюции изучаемого белка и вычисляют его молекулярную массу интерполяцией (рис. 3.1). Точность метода не очень велика, но вполне достаточна для большинства практически встречающихся задач.
При использовании данного метода необходимо учитывать ограничения, возникающие из-за того, что гельобразующий материал не вполне инертен, как это предполагает теория метода, и может взаимодействовать с разделяемыми веществами, что искажает зависимость объема элюции от размера молекулы. Это особенно сказывается при разделении малых количеств белка, так как сорбционная емкость матрицы геля невелика и в крупномасштабных опытах ее взаимодействие с белком мало отражается на процессе.
Связывание белков гельобразующими материалами может быть вызвано ионообменными взаимодействиями, в частности содержанием отрицательно заряженных групп в полисахаридных матрицах (сефароза, сефадекс), а также в полиакриламидных материалах В последних карбоксильные группы возникают при спонтанном гидролизе амидов, в полисахаридах же они могут образовываться в результате окисления. Задержка при гель-хроматографии, вызванная ионообменными взаимодействиями с матрицей, особенно характерна для катионных белков, например лизоцима и некоторых субтилизинов. Нередко она весьма значительна и может даже препятствовать отделению солей от белка. В аналитических опытах такое удерживание удается подавить значительным повышением ионной силы раствора.
Еще одна причина аномального удерживания веществ при гель-хроматографии особенно заметная при выделении небольших молекул, например пептидов, — гидрофобное связывание с матрицей геля. Гидрофобные элементы включаются в гидрофильные полисахаридные матрицы при обработке их сшивающими агентами, в частности эпихлоргидрином, при синтезе сефадекса. Пептиды, содержащие гидрофобные, в особенности ароматические, остатки (фенилаланина, триптофана), иногда удерживаются матрицей столь значительно, что появляются в элюате позже неорганических солей.
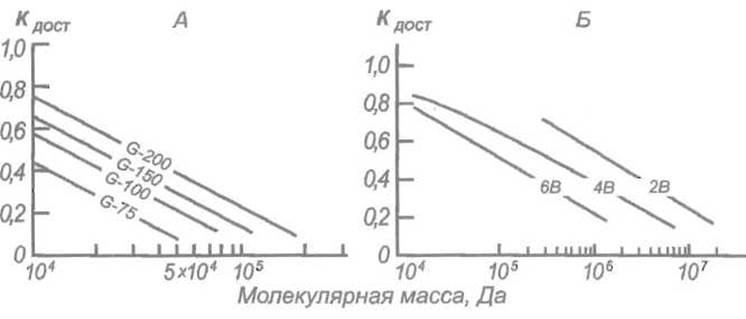
Рис. 3.1. Графики зависимости между молекулярной массой белков и коэффициентом доступности для сефадексов серии G («сверхтонких») (А) и сефарозы 2В, 4В и 6В (Б). Наилучшие результаты достигаются, если Kдост для выделяемого белка лежит в диапазоне 0,4-0,6
Разрешающая способность метода не очень велика, в то же время простота проведения и мягкость условий эксперимента являются его бесспорными преимуществами. Применимость метода на первых этапах очистки ограничивается тем, что для удовлетворительного фракционирования белков объем наносимого раствора не должен превышать 3-5% общего объема колонки. Ввиду этого к гель-хроматографии обычно прибегают в середине или на завершающих этапах выделения белка. Разумеется, при отделении низкомолекулярных примесей, в частности при обессоливании, объем образца может быть значительно большим, поскольку не требуется высокого разрешения. В таком упрощенном варианте гель-фильтрацию используют особенно часто.
Несмотря на указанные ограничения, гель-хроматография — удобный способ фракционирования белков. Его применяют и для отделения от белков низкомолекулярных примесей, в том числе солей.
В последнее время наряду с гельобразующими материалами для разделения белков по размерам начали применять макропористые неорганические носители — макропористые стекло и силикагель. Обычно поверхность этих материалов покрывают гидрофильными органическими веществами, чтобы исключить необратимую сорбцию белков. Жесткость этих материалов позволяет разделять белки по размеру молекул при повышенных давлениях, что ускоряет процесс и снижает помехи со стороны диффузии.