БІОНЕОРГАНІЧНА ТА БІООРГАНІЧНА ХІМІЯ - М.В. Яцков - 2014
II. ПРЕДМЕТ, ЗАВДАННЯ, МЕТОДИ ТА ОСНОВНІ НАПРЯМКИ ДОСЛІДЖЕНЬ БІООРГАНІЧНОЇ ХІМІЇ
2.4. Білкові речовини
До даної групи умовно відносяться біологічно активні речовини різної складності будови своїх молекул - амінокислоти, пептиди і білки.
2.4.1. Амінокислоти. Класифікація і окремі представники
Амінокислоти - похідні карбонових кислот, у радикалі яких один або декілька атомів Гідрогену заміщено на аміногрупу - NH2.
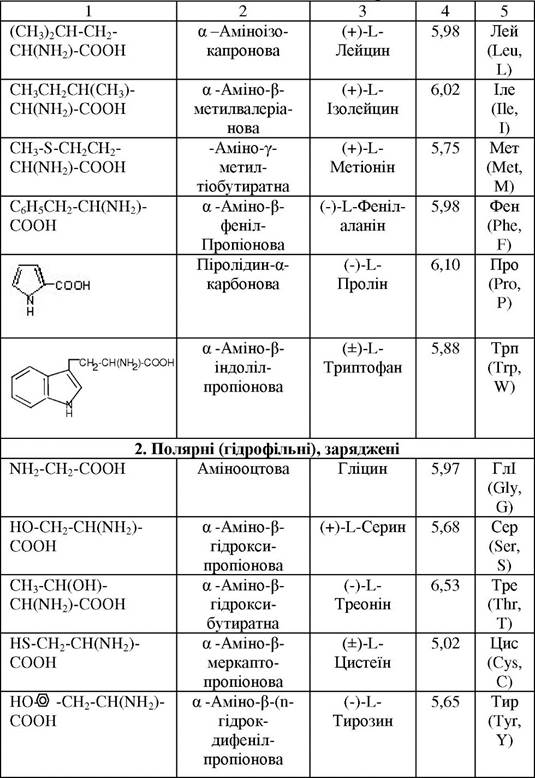
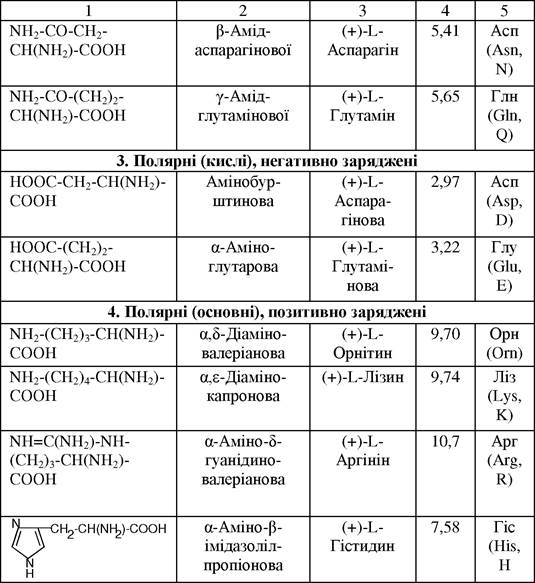
Відомо більше 200 індивідуальних амінокислот, що одержані з природної сировини і синтетичними методами. До складу білків найчастіше входять 20 амінокислот та 2 аміди амінокислот (див. табл. 18). За біологічними значеннями розрізняють замінні (синтезуються в організмі людини й тварин) і незамінні (не можуть синтезуватися у таких організмах і повинні входити до складу їжі) амінокислоти. До незамінних амінокислот належать валін, ізолейцин, лейцин, лізин, метіонін, треонін, триптофан і фенілаланін. До умовно незамінних амінокислот відноситься гістидин (він лише частково синтезується в організмі людини і тварин при певних умовах). Аргінін, аспарагінова і глутамінова кислоти, серин, амінокислоти пролін і оксипролін - є замінними амінокислотами. За хімічною класифікацією амінокислоти поділяють на ациклічні (моноаміно-монокарбонові, моноаміноди- карбонові, діаміномонокарбонові і діамінодикарбонові) та циклічні (ізо- і гетероциклічні). В ряді випадків користуються електрохімічною класифікацією амінокислот. їх ділять на нейтральні або одноосновні (наприклад гліцерин, валін, серин), кислі (двохосновні аспарагінова і глутамінова кислота) і основні (лізін, оксилізин, аргінін, орнітін).
Таблиця 18
Амінокислоти
Фізичні та хімічні властивості амінокислот
Реакція з нітритною кислотою
При нагріванні (до температури 700С) а-амінокислоти окиснюються нінгідрином і піддаються окиснювальному дезамінуванню з утворенням амоніаку і декарбоксилюванню з утворенням альдегіду і СO2, а нінгідрин відновлюється:
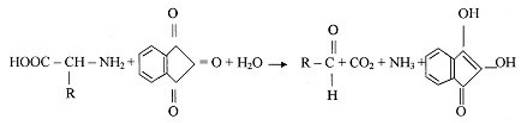
Відновлений ангідрин, конденсуючись з амоніаком і окисненим нінгідрином, утворює сполуку, яка, йонізуючись, переходить в зафарбовану форму, що має синьо-фіолетовий колір:
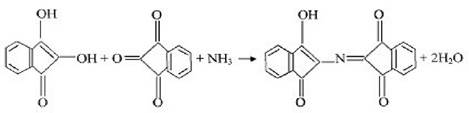
Утворення комплексної солі купруму(ІІ)
При нагріванні амінокислоти з купрум(ІІ) карбонатом утворюється комплексна сполука купруму, що має синє забарвлення. У випадку використання гліцину реакція має вигляд:
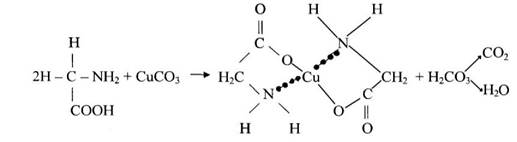
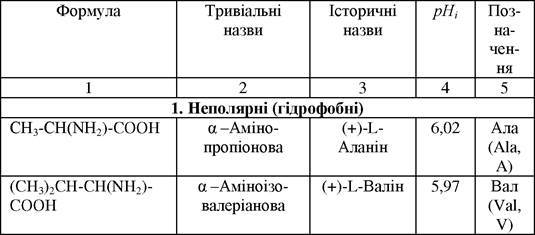
Реакція Адамкевича на триптофан
Триптофан в кислому середовищі вступає в реакцію з гліоксиловою кислотою (альдегідами), утворюючи при цьому забарвлений в червоно-фіолетовий колір продукт конденсації: