Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Организация метаболизма: катаболические пути
Окисление жирных кислот
Бета-окисление
Рассматривая структуру молекулы ацил-СоА и учитывая известные типы биохимических реакций, мы убеждаемся в том, что единственный рациональный путь дальнейшей атаки — это окисление молекулы с помощью флавопротеида, что приводит к отщеплению атомов водорода в а- и ß-положениях с образованием ненасыщенного ацил-СоА-производного (рис. 9-1, а). Одной из немногих возможных реакций, которым может подвергаться образовавшееся ненасыщенное соединение, является нуклеофильное присоединение по ß-положению. В результате присоединения воды (уравнение б) образуется спирт, окисление которого при участии NAD+ приводит к образованию кетона (уравнение в). Эта серия из трех реакций представляет собой хорошо известную последовательность реакций ß-окисления. На рис. 9-1 представлена и другая последовательность, входящая в цикл трикарбоновых кислот, в котором янтарная кислота превращается в щавелевоуксусную.
По аналогии с существованием нескольких активирующих ферментов, специфичных к жирным кислотам с разной длиной цепи, имеется также и несколько ацил-СоА — дегидрогеназ, катализирующих реакцию, описываемую уравнением a (рис. 9-1). Все они содержат FAD. В каждом случае восстановленный FADH2, входящий в состав фермента, затем снова окисляется специальным электронпереносящим флавопротеидом [2, 3], также содержащим FAD. Полагают, что этот белок переносит электроны к внутренней мембране митохондрий, где они поступают в митохондриальную систему переноса электронов.
По завершении реакций ß-окисления ß-кетоацил-СоА-производное расщепляется тиолазой [уравнение (9-2,6); см. также уравнение(7-62)]. Опять-таки имеется семейство ферментов, специфичных к цепям разной длины. Одним из продуктов [уравнение (9-2)] служит ацетил-СоА, который поступает в цикл трикарбоновых кислот и подвергается катаболическому распаду с образованием СО2. Вторым продуктом тиолитического распада является ацил-СоА-производное, которое на два атома углерода короче исходной молекулы. Оно снова вступает в цикл ß-окисления, причем в результате каждого оборота цикла освобождается двухуглеродный фрагмент, уходящий в виде ацетил-СоА [уравнение (9-2)]. Процесс продолжается до полного расщепления жирнокислотной цепи. Если исходная жирная кислота содержала в неразветвленной цепи четное число атомов углерода, то ацетил-СоА будет единственным продуктом ß-окисления. Если же молекула жирной кислоты состоит из нечетного числа атомов углерода, то процесс ß-окисления завершается образованием пропионил-СоА.
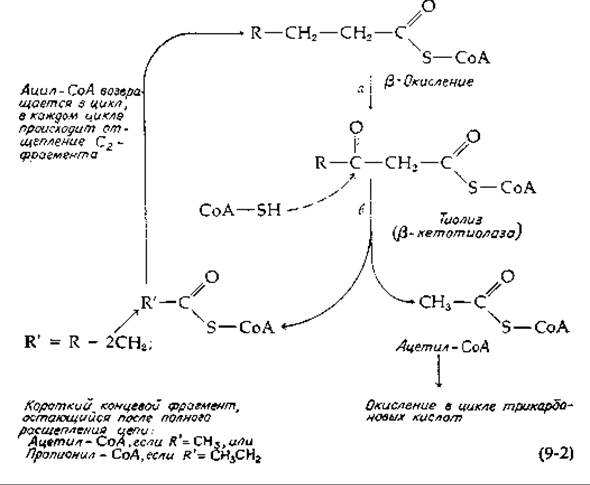

РИС. 9-1. Последовательность реакций ß-окисления. Слева: окисление СоА-производных жирных кислот; справа: окисление сукцината. Обе последовательности реакций протекают внутри митохондрий эукариотических клеток и катализируются специфическими ферментами; по-видимому, все эти ферменты (за одним исключением) растворены в митохондриальном матриксе. FAD* означает особый вид FAD-производного, обнаруженного в сукцинат-дегидрогеназе (гл. 8, разд. И, 3); этот фермент прочно связан с внутренней митохондриальной мембраной.