БИОХИМИЯ - Л. Страйер - 1984
ТОМ 3
Часть IV ИНФОРМАЦИЯ
ГЛАВА 27. СИНТЕЗ БЕЛКА
27.5. В узнавании кодона участвует антикодон, а не активированная аминокислота
Мы уже упоминали, что антикодон тРНК - участок, узнающий кодон мРНК, и что узнавание происходит путем спаривания оснований. Играет ли какую-нибудь роль в этом процессе аминокислота, присоединенная к тРНК? Ответ на этот вопрос был получен следующим путем. Вначале цистеин присоединили к соответствующей тРНК (она обозначается тРНКСуs.Затем присоединенный остаток цистеина превратили в аланин, обработав Cys-тРНКCys никелем Ренея. В результате атом серы отделился от активированного остатка цистеина; связь цистеина с тРНК при этом не затрагивалась.
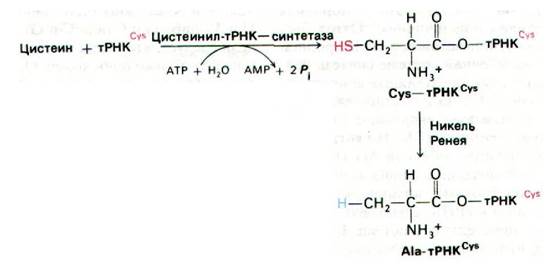
Так была получена гибридная аминоацил- тРНК, в которой аланин ковалентно присоединен к тРНК, специфичной к цистеину.
Какой кодон узнаёт эта гибридная тРНК - аланина или цистеина? Ответ был получен при использовании этой гибридной тРНК в бесклеточной системе синтеза белка. Матрицей служил случайный сополимер, построенный из U и G в соотношении 5:1; в норме он вызывает включение цистеина (UGU), но не аланина (GCX). Но когда в инкубационную смесь добавили Аlа-тРНКСуs, произошло включение аланина в полипептид. Другими словами, аланин включался так, как если бы к тРНК, специфичной к цистеину, был присоединен цистеин. Был сделан вывод, что узнавание кодона не зависит от аминокислоты, прикрепленной к тРНК.
Такой же результат был получен в тех случаях, когда роль матрицы выполняла гемоглобиновая мРНК. В качестве гибридной аминоацил-тРНК использовали 14С-аланил-тРНКСуs. Единственный радиоактивный триптический пептид (т. е. пептид, содержащий 14С-аланин) соответствовал пептиду, который в норме содержит цистеин, а не аланин. С другой стороны, ни в одном пептиде, который в норме содержит аланин, а не цистеин, не было обнаружено метки. Этот эксперимент, равно как и предыдущий, убедительно доказал, что аминокислота в аминоацил-тРНК не играет никакой роли в выборе кодона.
27.6. Молекула транспортной РНК может узнавать более одного кодона благодаря «качаниям»
По каким правилам происходит узнавание кодона антикодоном в тРНК? Проще всего предположить, что каждое из оснований кодона образует уотсон-криковскую пару оснований с комплементарным основанием антикодона. Тогда кодон и антикодон должны полностью соответствовать друг другу с учетом антипараллельности (на схеме штрих обозначает комплементарное основание):
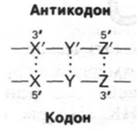
Так, X и X' должны быть либо А и U (или U и А), либо G и С (или С и G). Из этой модели следует, что каждый антикодон может узнавать только один кодон. Однако факты, которыми мы располагаем, противоречат этому. Некоторые выделенные в чистом виде молекулы тРНК могут узнавать более одного кодона. Например, дрожжевая аланиновая тРНК, изученная Холли, связывается с тремя кодонами: GCU, GCC и GCA. Только первые два основания этих кодонов одинаковы, третье различается. Может быть, узнавание третьего основания кодона иногда менее избирательно, чем узнавание двух других? Общая картина вырожденности генетического кода показывает, что дело может обстоять именно так. XYUи XYC всегда кодируют одну и ту же аминокислоту, a XYA и XYG обычно имеют одинаковый смысл. Исходя из этих данных, Крик предположил, что на спаривание третьего основания должны накладываться менее строгие стерические ограничения, чем на спаривание двух других. Были построены модели различных вариантов спаривания оснований, чтобы определить, какие из них сходны со стандартными А-U- и G—С-парами в отношении расстояния и угла между гликозидными связями. В это исследование был включен инозин, так как он встречается в некоторых антикодонах. Если предположить, что в спаривании третьего основания кодона допустима некоторая стерическая свобода («качание», или неоднозначное соответствие), то комбинации, приведенные в табл. 27.2, кажутся вполне возможными.
Таблица 27.2. Допустимые типы спаривания третьего основания кодона в соответствии с гипотезой «качаний»

В настоящее время правомочность гипотезы «качаний» доказана. Антикодоны тРНК с известной последовательностью связываются с теми кодонами, которые предсказывает эта теория. Например, антикодоном дрожжевой аланиновой тРНК является IGC. Эта тРНК узнает кодоны GCU, GCC и GCA:
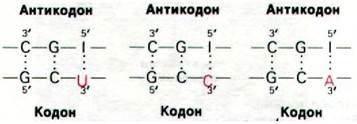
Итак, I спаривается с U, С и А, как и предсказывает теория.
Фенилаланиновая тРНК, имеющая антикодон GAA, узнает кодоны UUU и UUС, но не UUА и UUG:
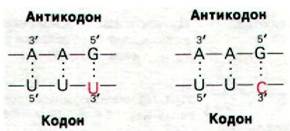
Таким образом, G спаривается с U или с С в третьем положении кодона, как и предсказывает гипотеза качаний.
Можно сделать два обобщения, касающихся кодон-антикодонового взаимодействия.
1. Первые два основания кодона спариваются обычным образом. Узнавание происходит точно. Следовательно, кодоны, которые различаются по одному из первых двух оснований, должны узнаваться различными тРНК. Например, и UUА, и СUА кодируют лейцин, но считываются различными тРНК.
2. Первое основание антикодона определяет, считывает ли данная молекула тРНК один, два или три типа кодонов: С и А узнают по одному кодону, U и G - по два кодона, I - три кодона. Итак, одна из причин вырожденности генетического кода заключается в неточности, или неоднозначности, спаривания («качании») третьего основания кодона. Именно в этом мы усматриваем основную причину распространенности необычного нуклеозида инозина в антикодонах. Инозин увеличивает число кодонов, которые способна считывать данная молекула тРНК (рис. 27.8).
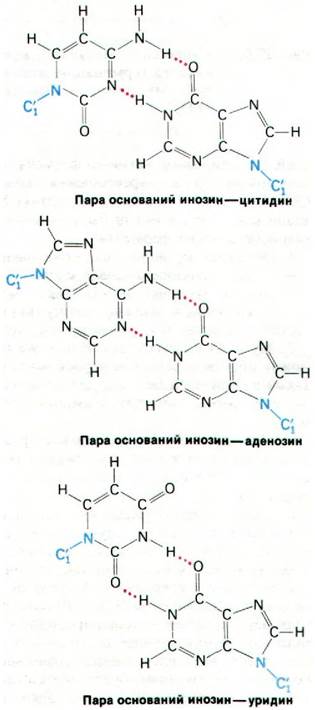
Рис. 27.8. Благодаря «качаниям» инозин может давать пары оснований с цитозином, аденином и урацилом
27.7. Мутантные молекулы транспортных РНК могут подавлять другие мутации
Новый этап в изучении процесса узнавания кодона начался в связи с исследованиями мутантных тРНК, в которых изменено одно
основание в антикодоне. Эти спонтанные события противоположны по своей сути химической модификации in vitro аминокислоты, прикрепленной к тРНК. Любопытна история открытия таких мутантных тРНК. В течение многих лет генетики знали, что повреждающее действие некоторых мутаций может быть подавлено другой мутацией. Предположим, какой-то фермент стал неактивным из-за превращения кодона GCU (аланин) в кодон GAU (аспартат). Мутации какого рода могли бы восстановить активность этого фермента?
1. Обратная мутация того же основания А —> С даст исходное кодовое слово.
2. Другая мутация A → U даст валин (GUU), который, возможно, полностью или частично восстановит активность фермента.
3. Мутация в другом месте того же гена может обратить действие первой мутации. Такой измененный белок будет отличаться от белка дикого типа двумя аминокислотами.
4. Мутация в другом гене может преодолеть повреждающее действие первой мутации. Это явление называется межгенной супрессией.
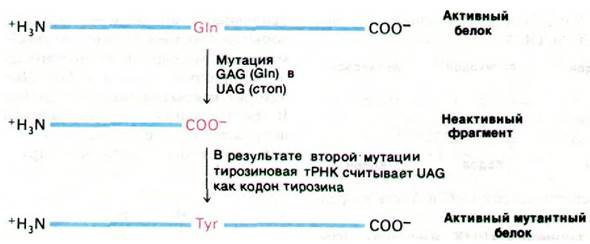
В течение долгого времени механизм действия межгенных супрессоров оставался загадкой. Теперь мы знаем из генетических и биохимических исследований, что большинство таких супрессоров действует, изменяя считывание мРНК. Рассмотрим к примеру мутацию, которая приводит к появлению терминирующего кодона UAG (т. е. стоп-кодона, или сигнала терминации). Результатом мутации будет образование неполных полипептидных цепей. Такие мутации называются нонсенс-мутациями (от англ. nonsense - бессмысленный), так как неполные полипептиды обычно неактивны. Действие нонсенс-мутации UAG может быть подавлено мутациями в нескольких
различных генах. Один из этих супрессоров считывает UAG как кодон тирозина, что может привести к синтезу активного белка вместо неполной полипептидной цепи (рис. 27.9). Почему же эта мутантная РНК вставляет тирозин в ответ на кодон UAG? В норме тирозиновая тРНК узнает кодоны UAC и UAU. Эта мутантная тРНК идентична нормальной тирозиновой тРНК, за исключением одной замены основания в антикодоне: GUA → CUA. Мутация G → С первого основания антикодона меняет специфичность узнавания. Как предсказывает теория «качаний», измененный антикодон может узнавать только UAG.
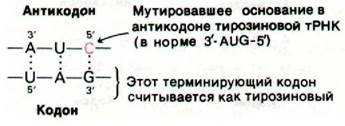
Рис. 27.9. Супрессия мутации, приводящей к терминации цепи, второй мутацией в молекуле тРНК
Супрессорная тРНК этого типа будет закреплена отбором скорее всего в том случае, если мутировавшая тРНК не была необходимой. Иными словами, должна существовать другая разновидность тРНК, которая узнает те же кодоны, что и мутировавшая тРНК. Действительно, у E. coli имеются две различные тРНК, которые в норме узнают кодоны UAC и UAU. Изменяется та тРНК, которая присутствует в небольшом количестве. Функция этой минорной разновидности тирозиновой тРНК в норме неясна. В связи с существованием такой супрессорной мутации возникает еще один вопрос. Если мутантный кодон в UAG считывается как тирозин, а не как сигнал терминации, что происходит при нормальной терминации цепей? Как ни странно, большинство полипептидных цепей в клетках супрессорного мутанта терминируется нормально, возможно, по той причине, что сигнал терминации представляет собой нечто большее, чем просто кодон UAG. Действительно, известно, что некоторые кодирующие последовательности заканчиваются двумя различными стоп-кодонами. Кроме того, супрессия не обладает стопроцентной эффективностью.
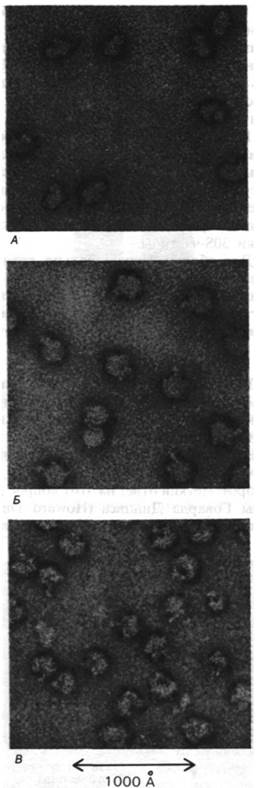
Рис. 27.10. Электронные микрофотографии 70S-рибосом (А), 50S-субчастиц (Б) и 30S-субчастиц (В)
Были обнаружены и другие виды мутантных тРНК. Миссенс-супрессоры изменяют считывание мРНК, так что в ответ на некоторые кодоны вставляется измененная аминокислота (например, глицин вместо аргинина). Особенно интересны супрессоры сдвига рамки. Одна из таких тРНК содержит лишнее основание в антикодоновой петле. Благодаря этому она считывает в качестве кодона четыре основания вместо трех. Например, UUUC считывается как кодон фенилаланина вместо UUU. Такая измененная тРНК может супрессировать вставку лишнего основания.