ОСНОВИ МЕДИЧНОЇ БІОЛОГІЇ - 2012
Основи медичної генетики. Методи вивчення спадковості людини
Антропогенетика (генетика людини) та медична генетика найважливіші розділи в сучасній теоретичній підготовці студентів — майбутніх медиків. Розвиток цих напрямків відбувався майже одночасно з розвитком загальної менделевської генетики. В 1865 році англійський лікар Ф. Гальтон друкує працю «Успадкування таланту і характеру», в якій пропонує свій біометричний метод вивчення спадковості людини. Суттєвий внесок зроблений Герродом, який встановив спадковий характер алькаптонурії (1902) та зробив припущення про генетичну природу порушень обміну речовин. Першою важливою перемогою класичної менделевської генетики стало встановлення успадкування груп крові за системою АВ0 (Берштейн, 1924).
Суттєво вплинуло на розвиток генетики виникнення у 50-х роках нової науки — молекулярної генетики. Засновники Полінг та його колеги у 1949 році встановили причини серпоподібно-клітинної анемії — порушення структури молекули гемоглобіну. Подальший внесок був зроблений цитогенетиками (Д. Тійо, А. Леван, 1956), які в 60-х роках розробили методику вивчення каріотипу людини та дослідження хромосом.
Наступний етап розвитку цих напрямків генетики — це впровадження досягнень генетики у практику охорони здоров’я. У 60-70-х роках набуває швидкого розвитку медико- генетичне консультування (МГК), розробляються та впроваджуються методи консультування та профілактики спадкових хвороб (фенілкетонурія, галактоземія...), а також методи пренатальної діагностики хромосомних і молекулярних хвороб.
Застосування в медичній генетиці нових методів дозволило підняти вивчення спадковості на новий рівень -- вивчати генетичні механізми та процеси їх порушення на клітинному та молекулярному рівнях, підійти до розшифрування генетичних карт хромосом та генетичного коду людини.
Впровадження цитогенетичного методу та методу гібридизації соматичних клітин відкрило нові можливості для аналізу хромосомних хвороб, пов’язаних з порушенням кількості та структури хромосом. Широке застосування біохімічних та імунологічних методів дозволило встановити більш, як 3000 спадкових хвороб — порушень обміну та структури біомолекул. Методи вивчення ДНК (ДНК-аналіз, генна інженерія) дали можливість аналізувати генетичний матеріал на молекулярному рівні.
Як результат в медицині з’являються нові можливості безпосереднього застосування в практичній діяльності медиків не тільки діагностики, а й профілактики та лікування спадкових хвороб. Одним із засновників медичної генетики в нашій країні С.М. Давиденков вперше застосував ідеї генетики у клініці, провів аналіз ряду спадкових хвороб та медико-генетичне консультування в родинах хворих. На даний час вже відкрито більш як 5 тис. моногенних хвороб та 500 хромосомних, встановлені зміни спадкового матеріалу при деяких мультифакторіальних хворобах.
Зрозуміло, що розвиток антропогенетики та медичної генетики визначався практичними потребами людини, зокрема потребами медицини, і необхідність подальшого розвитку цих напрямків генетики не викликає сумніву. На сучасному етапі в генетиці розроблені методи вивчення спадковості людини, які можуть об’єктивно встановити характер успадкування ознаки, визначити на якому рівні організації відбулося порушення спадкового матеріалу, провести повне клініко-генетичне обстеження хворого.
Основні закономірності спадковості та мінливості відкриті завдяки застосуванню гібридологічного методу генетичного аналізу (Г. Мендель, 1865р.). Для людини, як об’єкту генетичних досліджень, даний метод не може бути застосований. По-перше, для людини не може бути застосоване штучно спрямоване схрещування. По-друге, невелика чисельність нащадків призводить до неможливості застосування статистичного підходу. По-третє, довга зміна поколінь (в середньому через 25 років) дає можливість за життя спостерігати зміну лише 3-4 поколінь. Також вивченню генетики людини заважає велика кількість груп зчеплення та генотиповий і фенотиповий поліморфізми, значний вплив факторів середовища на експресивність і пенетрантність ознак.
Всі перелічені особливості призвели до розробки вченими специфічних методів вивчення генетики людини, а сучасні експериментальні методи дозволили встановити групи зчеплення майже за кожною хромосомою, розшифрувати генетичний код. Значно допомагає у вивченні генетики мультифакторіальних ознак біометричний підхід (Ф. Гальтон, 1865), можливості якого зросли внаслідок застосування сучасної комп’ютерної техніки.
Генеалогічний метод (Ф. Гальтон, Дж. Адамс, В. Вейнберг) ґрунтується на простеженні якої-небудь ознаки у ряді поколінь з вказівкою родинних зв'язків між членами родоводу. Генеалогія — родовід людини. Генеалогічний метод - найбільш універсальний метод генетики людини. Технічно він складається з двох етапів: 1) складання родоводу і 2) генеалогічний аналіз родоводу.
Складання родоводу починають від пробанда. Пробанд - це особа, родовід якої необхідно скласти і проаналізувати. Найчастіше це хворий або носій гена досліджуваної ознаки. Діти однієї батьківської пари називаються сибсами (брати-сестри). Зазвичай родовід складається за однією або кількома ознаками. За всіма відомими ознаками він технічно не може бути складений. При складанні родоводу користуються символами, які запропонував у 1931 р. Г. Юст (рис.).
Правила складання родоводів: 1) пробанда на схемі родоводу позначають стрілкою; 2) особи одного покоління займають окремий рядок або коло; 3) покоління позначаються ліворуч римською цифрою; найстарше покоління розташовують зверху родоводу і позначають цифрою І, а наймолодше - внизу родоводу; 4) усі члени одного покоління розміщуються в порядку народження (зліва направо) по горизонталі і позначаються арабськими цифрами.
Для достовірності результатів аналізу слід охопити не менше 3-4-х поколінь. У родовід включають всіх членів сім'ї: здорових, хворих, мертвонароджених і викиднів, дефективних та розумово неповноцінних. Чим більше є достовірних відомостей про здоров'я родичів пробанда, тим інформативнішим буде генеалогічний аналіз. При посиланні на будь-якого члена сім'ї вказують спершу номер покоління, а потім члена сім'ї в тому ж поколінні: ІІ-3 або Ш-7. До схеми родоводу обов'язково додається систематизований опис відомостей про пробанда та його родичів (легенда). У легенді повинні знайти відображення наступні дані: 1) результати клінічного і позаклінічного обстеження пробанда; 2) відомості про особистий огляд родичів пробанда; 3) співставлення результатів особистого огляду пробанда з даними опитування його родичів; 4) письмові відомості про родичів, які проживають в іншій місцевості.
Генеалогічний аналіз родоводу дозволяє встановити: 1) характер ознаки (спадкова чи неспадкова); 2) тип успадкування; 3) зиготність пробанда (гомо- чи гетерозигота) за досліджуваною ознакою; 4) ймовірність ризику прояву спадкової ознаки в нащадків; 5) при наявності родоводу, що включає максимальну кількість родичів, можна також встановити пенетрантність гена, проаналізувати зчеплення генів, проводити картування хромосом, вивчати інтенсивність мутаційного процесу і механізми взаємодії генів; 6) по якій лінії (батьківській або материнській) передається ознака.
Перше завдання генеалогічного аналізу - встановити: досліджувана ознака є спадковою чи неспадковою. Якщо досліджувана ознака (або хвороба) зустрічається в родоводі кілька разів, то можна думати про її спадкову природу. Однак необхідно виключити можливість фенокопій. Наприклад, якщо один і той же шкідливий фактор діяв на жінку під час усіх вагітностей, то в неї можуть народитися діти з однаковими аномаліями. Інший приклад: одні і ті самі професійні шкідливі фактори можуть спричинити схожі захворювання в членів однієї сім'ї. Після встановлення спадкового характеру ознаки (хвороби), необхідно встановити тип успадкування: аутосомно-домінантний, аутосомно-рецесивний, Х-зчеплений-домінантний, Х-зчеплений-рецесивний і Y-зчеплений.
Аутосомно-домінантний тип успадкування (рис.) зумовлений передачею в ряді поколінь домінантного гена, який локалізується в автосомі. Для цього типу успадкування характерні:
1) при достатній кількості потомків ознака (хвороба) проявляється в кожному поколінні (успадкування по вертикалі родоводу);
2) особи чоловічої і жіночої статі успадковують ознаку однаково часто;
3) обоє батьки в однаковій мірі передають ознаку дітям;
4) один або обоє батьки хворої дитини -хворі;
5) імовірність народження хворої дитини в сім'ї, де один з батьків хворий гетерозиготний, а інший здоровий (Аа х аа), складає 50%.
Необхідно враховувати, що при аутосомно-домінантному успадкуванні ознака може бути відсутня в одному поколінні. Це трапляється, коли захворювання проявляються не відразу, а в певному віці, як, наприклад, хорея Гентингтона - (середній вік 38-40 років). У випадку смерті в більш ранньому віці ніяких даних про можливу хворобу цього члена сім'ї не буде, але залишається ймовірність хвороби в нащадків. Існують стерті форми захворювань при малій експресивності мутантного гена, можливе пригнічення останнього якимось епістастичним геном.
Аутосомно-домінантний тип успадкування
Генотипи |
Г енотипи |
Здорові |
Хворі діти, % |
АА х АА |
АА |
- |
100 |
АА х Аа |
АА, Аа |
- |
100 |
Аа х Аа |
АА, Аа, Аа, |
25 |
75 |
Аа х аа |
Аа, аа |
50 |
50 |
аа х аа |
аа |
100 |
- |
Аутосомно-рецесивний тип успадкування зумовлений передачею в ряді поколінь рецесивного гена, який локалізований в аутосомі. Типові ознаки цього типу:
1) навіть при достатній кількості потомків ознака (хвороба) проявляється не в кожному поколінні;
2) хворіють переважно сибси (брати-сестри) (успадкування по горизонталі), а не батьки- діти, як при аутосомно-домінантому типі успадкування;
3) чоловіки і жінки успадковують ознаку однаково часто;
4) Батьки хворої дитини частіше фенотипово здорові (гетерозиготні носії мутантного гену).
5) імовірність народження хворих дітей зростає в родинних шлюбах;
6) хворіють лише рецесивні гомозиготи (аа), гетерозиготи (Аа) не хворіють, але є носіями патологічного гена;
7) імовірність народження хворих дітей у здорових гетерозиготних батьків (Аа х Аа) складає 25 %.
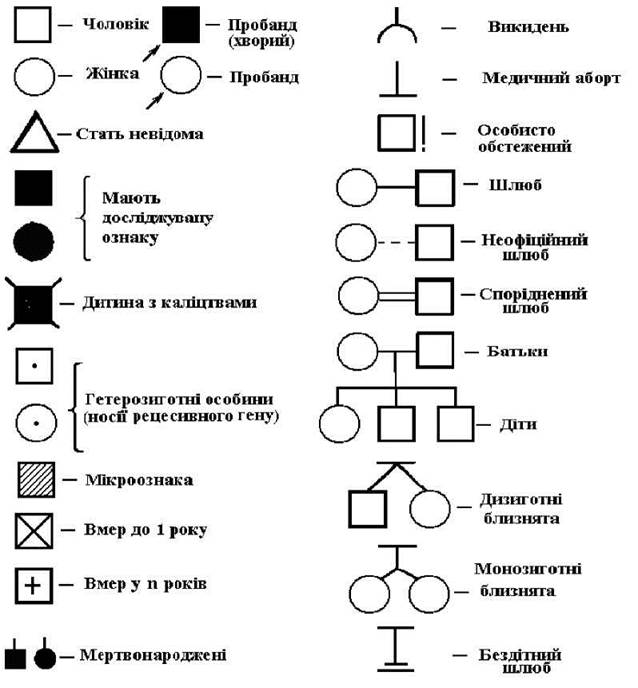
Рис. 24. Стандартні символи для складання родоводів.
Аутономно-рецесивний тип успадкування
Генотипи |
Г енотипи |
Здорові |
Хворі діти, % |
АА х АА |
АА |
100 |
- |
АА х Аа |
АА, Аа |
100 |
- |
Аа х Аа |
АА, Аа, Аа, |
75 |
25 |
Аа х аа |
Аа, аа |
50 |
50 |
аа х аа |
аа |
- |
100 |
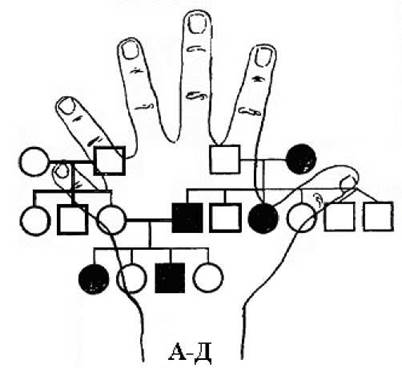
Рис. 25. Аутосомно-домінантний тип успадкування (полідактилія).
Х-зчеплений домінантний тип успадкування (рис.) зумовлений локалізацією домінантного гена в ділянці Х-хромосоми, яка не має гомолога в Y-хромосомі. Для цього типу характерні:
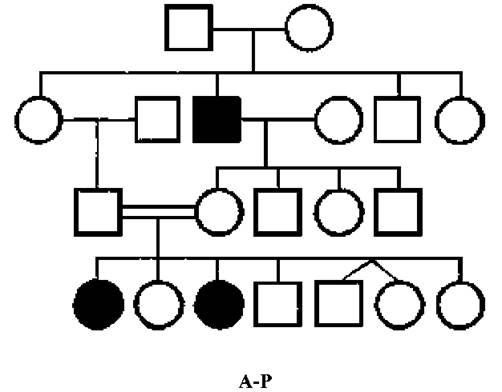
Рис. 26. Аутосомно-рецесивний тип успадкування (фенілкетонурія).
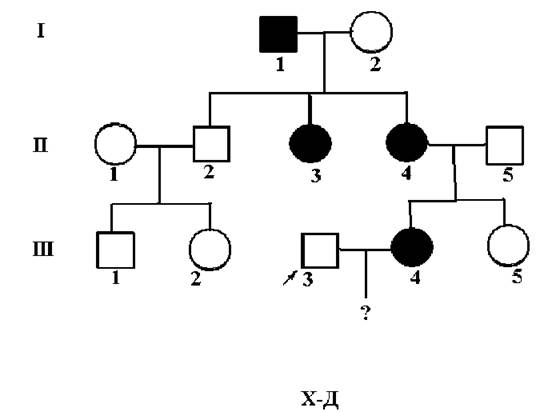
Рис. 27. Х-зчеплений-домінантний тип успадкування (вітамін-D-резистентний рахіт).
1) у хворого батька (XAY) усі дочки будуть хворі, оскільки вони отримують батьківську Х-хромосому з домінантним геном; усі сини народяться здоровими, оскільки успадкують материнську Х-хромосому;
2) якщо мати гомозиготна за аномальним геном (ХАХА), вона передасть ознаку (хворобу) всім дочкам і всім синам;
3) якщо мати гетерозиготна, вона передасть ознаку (хворобу) половині своїх дочок (ХАХа) і половині синів (XaY); імовірність народження здорових дітей 50% незалежно від статі.
4) ознака однаково проявляється як у чоловіків, так і у жінок.
За Х-зчепленим домінантним типом успадковуються: рахіт, який не піддається лікуванню вітаміном D, коричнева емаль зубів.
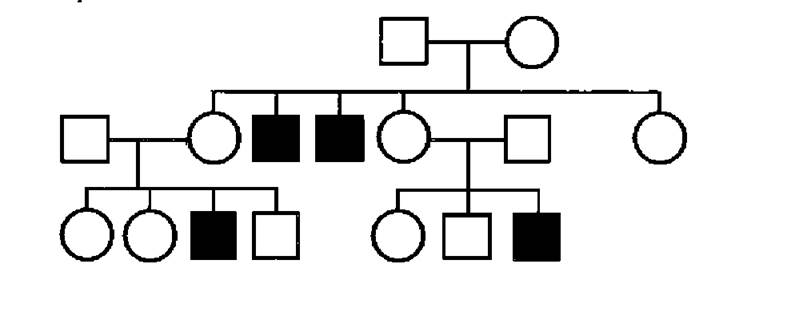
Рис. 28. Х-зчеплений рецесивний тип успадкування (гемофілія).
Х-зчеплений рецесивний тип успадкуваня (рис.) зумовлений локалізацією рецесивного гену ознаки у ділянці X-хромосомі, яка не має гомолога в Y-хромосомі. Типові ознаки цього типу успадкування:
1) ознака спостерігається в родоводі по горизонталі та вертикалі, часто через покоління, хворіють сибси - рідні, двоюрідні, родичі з боку матері (дядьки пробанда).
2) хворіють переважно особи чоловічої статі;
2) відсутня передача ознаки (хвороби) від батька до сина;
3) жінка-носійка (ХАХа) передає хворобу половині своїх синів, усі дочки - здорові, але половина з них - носії;
4) усі дочки хворого батька (XaY) будуть фенотипово здоровими, але гетерозиготними носіями;
5) якщо мати гомозиготна (ХаХа) за даним геном, всі сини будуть хворі.
6) батьки хворої дитини частіше фенотипово здорові, можуть бути хворі з боку матері (жінки гетерозиготні носії мутантного гену).
7) ймовірність прояву ознаки у нащадків становить 25% (при гетерозиготності матері, від гемізиготного батька ознака передається донькам, але фенотипові у них не проявляється).
За Х-зчепленим рецесивним типом успадковуються: гемофілія, дальтонізм, м'язова дистрофія Дюшена, синдром Леша-Ніхана. У родоводах з X-зчепленим рецесивним типом успадкування переважають хворі особи чоловічої статі.
Y-зчеплений тип успадкування (голандричне успадкування) зумовлений локалізацією гена в ділянці Y-хромосоми, яка не має гомолога в Х-хромосомі. При цьому типі ознака успадковується виключно по чоловічій лінії з покоління в покоління - від батька до всіх його синів, бо лише синам батько передає Y-хромосому. За Y-зчепленим типом успадковуються гіпертрихоз краю вушної раковини ("волосаті вуха"), іхтіоз (надмірна кератизація шкіри - "риб'яча луска").
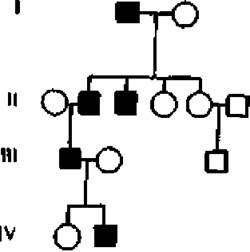
Рис. 29. Родовід успадкування ознаки зчепленої з Y-хромосомою.
Близнюковий метод
Цей метод запропонував у 1875 р. Ф.Гальтон. Сутність близнюкового методу полягає в порівнянні досліджуваних ознак у різних групах близнят, виходячи зі схожості або відмінності їх генотипів і середовища, в якому вони росли. Близнятами називають нащадків однієї матері, які сумісно розвивались і з'явились у процесі одних пологів. Вони бувають монозиготними (МБ) і дизиготними (ДЗ). Монозиготні (однояйцеві, ідентичні) близнята розвинулися з однієї зиготи внаслідок поділу її на 2, 3 і більшу кількість зародків, мають ідентичні генотипи (100 % однакових генів), завжди однакової статі і дуже схожі один на одного. Дизиготні (двояйцеві, неідентичні) близнята розвинулися в одній вагітності з різних зигот (з двох або більше яйцеклітин, запліднених різними сперматозоїдами); вони можуть бути як одностатеві, так і різностатеві; мають приблизно 50 % однакових генів і схожі один на одного не більше братів і сестер, які народилися в різний час. Частота народження близнят у різних країнах дорівнює приблизно 1 на 86-88 пологів. Монозиготні близнята народжуються рідше, ніж дизиготні. У середньому на 2-3 пари ДБ припадає одна пара МБ. Дизиготні близнята частіше народжуються в жінок, які лікувалися гонадотропними гормонами, а також у віці 40-45 років. Схильність до народження близнят передається по материнський лінії.
Близнюковий метод найчастіше застосовують для: 1) оцінки співвідносної ролі спадковості і середовища в розвитку ознаки (хвороби); 2) встановлення спадкового характеру ознаки; 3) визначення експресивності і пенетрантності гена; 4) встановлення ефективності впливу на організм таких зовнішніх факторів, як лікувальні засоби, виховання, навчання.
При застосуванні цього методу проводиться порівняння: 1) монозиготних близнят з дизиготними; 2) партнерів монозиготних пар між собою; 3) даних аналізу близнят з популяцією в цілому.
Для встановлення зиготності (моно- чи дизиготності) близнят запропоновано ряд методів: 1) полісимптоматичний метод-вивчення симптомів фенотипу (пігментація волосся, очей, шкіри, форма волосся і особливості волосяного покриву, форма носа, губ і вушних раковин, пальцеві візерунки); 2) портретна ідентифікація; 3) анкетний метод (анкета містить 12 запитань для близнюків і 4 - для батьків); 4) імунологічні методи. Метод, яким можна встановити зиготність з 100 %-ною достовірністю - це трансплантація шматочка шкіри. Добре приживлення свідчить про монозиготність, відторгнення - про дизиготність. Сучасні методи встановлення зиготності - молекулярно-генетичні.
Для визначення ролі генотипу чи умов середовища в розвитку ознаки порівнюють конкордантність (дискордантність) партнерів за ознаками. Конкордантність — це подібність за досліджуваною ознакою між близнюками (визначається у %). Пару близнят називають конкордантною, якщо досліджувана ознака виявляється в обох партнерів, і дискордантною, якщо досліджувана ознака є лише в одного з них. Чим вище конкордантність, тим більшу роль у розвитку ознаки відіграє спадковість. Такі ознаки, як колір очей і волосся, групи крові повністю визначаються генотипом.
Конкордантність (у %) деяких ознак людини у близнят (MZ, DZ)
Ознаки |
MZ |
DZ |
Нормальні |
||
Групи крові АВО, Rh |
100 |
46 |
Колір очей |
99,5 |
28 |
Колір волосся |
97 |
23 |
Папілярні візерунки |
92 |
40 |
Активність карбоангідрази |
79 |
47 |
Патологічні |
||
Діабет |
84 |
16 |
Коронарний тромбоз |
26 |
13,8 |
Клишоногість |
32 |
3 |
Артеріальна гіпертонія |
25 |
9,4 |
Розщілина губи |
33 |
5 |
Природжений вивих стегна |
41 |
3 |
Паралітичний поліомієліт |
36 |
6 |
Бронхіальна астма |
19 |
4,8 |
Кір |
98 |
94 |
Епідемічний паротит |
82 |
74 |
Туберкульоз |
37 |
15 |
Дифтерит |
50 |
38 |
Епілепсія |
67 |
3 |
Шизофренія |
70 |
13 |
Гіпертонія |
26,2 |
10 |
Ревматизм |
20,3 |
6,1 |
Аналіз успадкування ознак у дизиготних близнят дозволяє проаналізувати інший варіант - вплив однакових умов середовища на фенотиповий прояв ознак при різних генотипах.
Для встановлення впливу генотипу на визначення ознаки застосовують формулу К. Хольцингера, де Н — коефіцієнт спадковості (англ. hеrdity — спадковість), k(MZ), — коефіцієнт парної кореляції для однояйцевих близнят (% конкордантності) і k(DZ) — коефіцієнт парної кореляції для дизиготних близнят (% конкордантності).
![]()
При Н, що дорівнює одиниці, ознака цілком визначається генотипом; при Н, що дорівнює нулю, визначну роль відіграє вплив середовища. Коефіцієнт Н, який становить 0,5 свідчить про однаковий вплив спадковості і середовища на визначення і формування ознаки.
Вплив середовища позначається літерою Е, тоді
Н + Е = 1, Н = 1 - Е, а Е = 1 - Н
Метод дерматогліфіки (Ф. Гальтон, 1892)
Це метод генетики людини, який ґрунтується на вивченні рельєфу шкіри на пальцях, долонях і підошовних поверхнях стоп (грец. derma - шкіра, gliphe - малювати). На відміну від інших частин тіла тут є епідермальні виступи — гребені, які утворюють складні візерунки. Дерматогліфічний малюнок генетично зумовлений, носить індивідуальний характер, як і генотип людини і не міняється протягом життя. На Землі немає людей з однаковими малюнками на пальцях (крім монозиготних близнят). Дерматогліфічні дослідження мають важливе значення у визначенні зиготності близнят, у діагностиці деяких спадкових хвороб, у судовій медицині, для ідентифікації особистості в криміналістиці. Один із розділів дерматогліфіки — дактилоскопія (вивчення візерунків на подушечках пальців). Інші розділи дерматогліфіки — пальмоскопія (вивчення візерунків на долонях) — плантоскопія (вивчення дерматогліфіки підошв).
Дактилоскопія — розділ дерматогліфіки, який вивчає візерунки на пальцях. Гребені на пальцях рук відповідають сосочкам дерми, тому їх називають папілярними лініями (лат. papilla - сосочок). Міжсосочкові заглибини утворюють борозенки. Повне формування деталей будови дотикових візерунків завершується до шести місяців, вони залишаються незмінними до кінця життя. Виділяють три основні типи папілярних візерунків: 1) завитки W (англ. whorl - завиток); 2) петлі L (англ. loop - петля): радіальні Lr і ульнарні Lu і 3) дуги A (arch - дуга) (рис.)
Папілярні лінії різних потоків ніколи не пересікаються, але можуть зближуватися, утворюючи трирадіуси (дельти). Гребеневий рахунок - число папілярних ліній між дельтою і центром візерунка. У нормі він дорівнює в жінок 135, чоловіків - 151, для кожного пальця - 15-20. При синдромі Шерешевського-Тернера (45, Х0) гребеневий рахунок високий (180), при синдромі Клайнфельтера (47, XXY) - низький (до 50).

Рис. 30. Варіанти візерунків пальця:
а) відбитки; б) схематичне розташування гребінців ліній та трирадіусів: 1 - концентричний узор; 2 - петля; 3 - дуга.
Пальмоскопія. Рельєф долоні дуже складний, він має ряд полів, подушечок і долонних ліній. Центральну долонну ямку оточують шість підвищень — подушечок. Біля основи великого пальця — тенар, біля протилежного краю долоні — гіпотенар, навпроти міжпальцевих проміжків знаходяться чотири міжпальцеві подушечки. Біля основи II, III, IV і V пальців знаходяться пальцеві трирадіуси — місця, де сходяться три напрямки папілярних ліній, їх позначають латинськими літерами а, b, с, d. Поблизу браслетної складки, яка відділяє кисть від передпліччя, розташовується головний (осьовий) долонний трирадіус. Якщо провести лінії від трирадіусів а, d до t, то утворюється кут долоні atd, у нормі він не перевищує 57°, а при хромосомних хворобах змінюється.
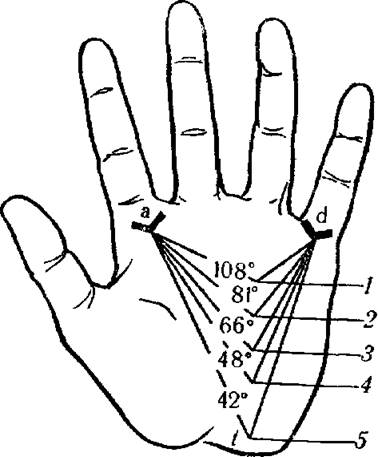
Рис. 31. Кут atd в нормі і при хромосомних хворобах:
1 — синдром Патау; 2 — синдром Дауна; 3 — синдром Шерешевського-Тернера; 4 — норма; 5 — синдром Клайнфельтера.
Частота візерунків змінюється у різних популяціях. Підрахунок величини трирадіусів дає уявлення про інтенсивність візерунка, вона зростає залежно від зменшення дуг і збільшення петель. Індивідуальні особливості шкірних візерунків зумовлені спадково. Це доведено генетичними дослідженнями, зокрема, близнюковим методом на моно- та дизиготних близнятах. Коефіцієнт конкордантності для монозиготних близнюків складає 0,8 - 0,9. У дизиготних близнят конкордантність не перевищує 0,3 - 0,5.
Плантоскопія вивчає візерунки на підошві. При деяких хромосомних хворобах відмічена зміна типових дугових візерунків.
Широкі дослідження з вивчення особливостей дерматогліфіки проведені Т. Д. Гладковою (1966), а по спадковій зумовленості шкірних візерунків — І.С. Гусєвою (1970, 1980). На підставі цих робіт зроблено висновок, що кількісні показники рельєфу гребенів шкіри програмуються полігенною системою, яка включає невелику кількість адитивно діючих генів.
Методи гібридизації соматичних клітин
Соматичні клітини містять увесь об’єм генетичної інформації. Це дає можливість вивчати багато питань генетики людини, які неможливо досліджувати на цілому організмі. Соматичні клітини людини отримують із різних органів (шкіра, кістковий мозок, клітини крові, тканини ембріонів). Найчастіше використовують клітини сполучної тканини і лімфоцити крові.
В 60-х роках були розроблені методики, які дозволяли вирощувати клітини у штучних умовах та вивчати клітинні процеси в експериментальних умовах. Це сприяло розробки методів генетики соматичних клітин (ГСК). За допомогою таких методів вивчають спадковість та мінливість на культурах соматичних клітин, що компенсує неможливість застосування для людини гібридологічного аналізу.
При злитті клітин двох різних типів (під впливом вірусу парагрипу Сендай, який інактивують, але він зберігає здатність впливати на злиття клітин) утворюються клітини, які містять у спільний цитоплазмі ядра обох батьківських клітин - гетерокаріони. Більшість гетерокаріонів гине, але ті, які містять тільки два ядра, часто продовжують свій розвиток, розмножуються поділом. Після мітозу і наступного поділу цитоплазми із двоядерного гетерокаріону утворюється дві одноядерні клітини. Кожна з них являє собою синкаріон - справжню гібридну клітину, яка має хромосоми обох батьківських клітин (рис.).
Гібридізація соматичних клітин проводиться у широких межах не тільки між різними видами, але і типами: людини х миша, людина х комар, муха х курка тощо. Залежно від мети аналізу, дослідження проводять на гетерокаріонних або синкаріонних клітинах. Синкаріони - це справжні гібридні клітини, бо у них відбувається поєднання двох геномів. Наприклад гібридні клітини людини і миші мають 43 пари хромосом: 23 - від людини і 20 - від миші. За допомогою цього методу проводиться картування хромосом у людини.
Методи генетики соматичних клітин дозволяють:
1. вивчати зчеплення генів та їх локалізацію в хромосомах;
2. встановити первинну дію генів та їх взаємодію;
3. встановити генетичну гетерогенність спадкової патології;
4. діагностувати спадкову патологію в пренатальному періоді.
Молекулярно - генетичні методи
Метод «секвенування» (від англ. sequence-послідовність) — методи вивчення нуклеотидної послідовності ДНК, зворотної транскрипції ДНК, розмноження (клонування) окремих фрагментів ДНК, шляхом включення їх у бактеріальні плазміди.
Такі методи дозволяють:
1. вивчати генетичний матеріал (послідовність генів в ДНК), визначати локалізацію порушень на молекулярному рівні (генні мутації);
2. визначати нуклеотидну послідовність ДНК та генів;
3. розмножувати структурні гени (клонування) шляхом включення в бактеріальну клітину;
4. рекомбінувати молекули ДНК для одержання необхідних речовин (генна інженерія) на основі генів людини;
5. визначати точну локалізацію генної мутації (ДНК-зонди).
Подальший розвиток дозволить розшифрувати послідовності нуклеотидів як структурних, так і регуляторних ділянок геному людини, а також в перспективі лікування генних хвороб на молекулярному рівні.
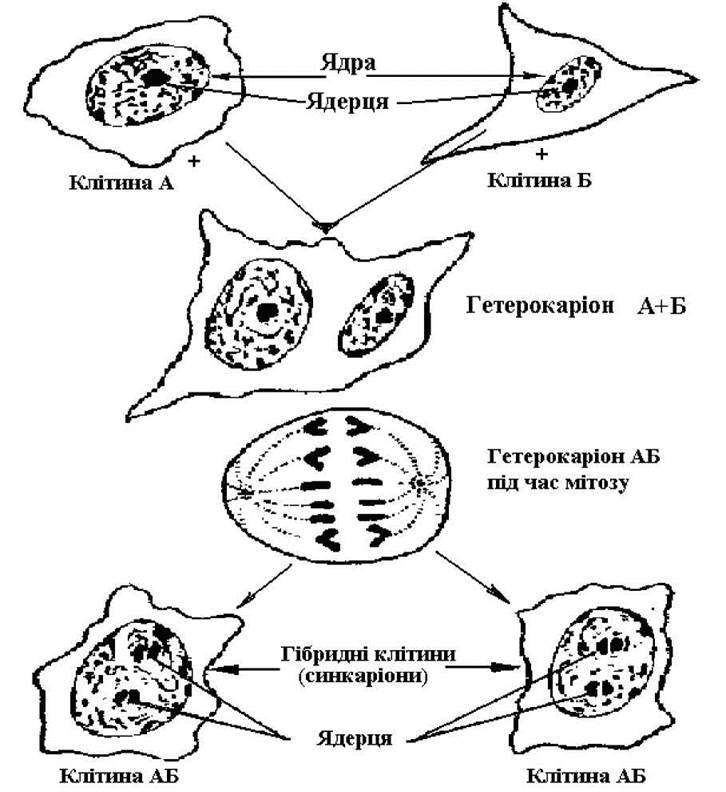
Рис. 32. Схема гібридизації соматичних клітин з утворенням синкаріонів (гетерокаріонів).
Імуногенетичний метод
Це метод вивчення генетичних закономірностей з використанням імунологічних реакцій (взаємодія антиген-антитіло) з утворенням комплексів.
Імуногенетичний метод дозволяє вивчати:
- генетичну детермінованість та поліморфізм імунних систем;
- генетику імуноглобулінів та системи комплімента;
- генетику комплексу гістосумісності, трансплантаційних антигенів факторів імунорегуляції;
- генетику системи HLA (human-leucocyte-asso ciated — антигени гістосумісності) людини і генетичне визначення резистентності до хвороб, які залежать від даної системи;
- поліморфізм еритроцитарних антигенів та генетику груп крові.
Для досліджень використовується:
- біологічні рідини (кров, слина, спинно - мозкова рідина) і тканини;
- культури клітин (HLA, залоз внутрішньої секреції, кісткового мозку, лейкоцитів).
Для встановлення відповідних генів визначають їх генетичні маркери (детермінанти) - антигени.
Імуногенетичні методи важливі для вирішення проблем трансплантації органів на тканини, для діагностики спадкової патології моногенних та мультифакторіальних хвороб; для виявлення генетичної схильності та резистентності до хвороб; для встановлення генетичних карт хромосом людини; кореляції між імунологічними маркерами і захворюваннями.